1 . 下列物质的检验中,其结论一定正确的是
A.向某溶液中加入 溶液,产生白色沉淀,加入稀 溶液,产生白色沉淀,加入稀 后,白色沉淀不溶解,也无其他现象,说明原溶液中一定含有 后,白色沉淀不溶解,也无其他现象,说明原溶液中一定含有 |
B.向某溶液中加入盐酸产生无色气体,该气体能使澄清的石灰水变浑浊,说明该溶液中一定含有 或 或 |
C.取少量久置的 样品于试管中加水溶解,再加足量盐酸酸化,然后加 样品于试管中加水溶解,再加足量盐酸酸化,然后加 溶液,若加盐酸时有气体产生,加 溶液,若加盐酸时有气体产生,加 溶液时有白色沉淀产生,说明 溶液时有白色沉淀产生,说明 样品已部分被氧化 样品已部分被氧化 |
D.将某气体通入品红溶液中,品红溶液褪色,该气体一定是 |
您最近一年使用:0次
2024-05-19更新
|
99次组卷
|
2卷引用:海南省琼中黎族苗族自治县琼中中学2023-2024学年高一下学期3月月考化学试题
2 . 下列叙述不正确的是
A. 分别与熔融氯化镁和氯化镁溶液反应,生成的产物不同 分别与熔融氯化镁和氯化镁溶液反应,生成的产物不同 |
B. 分别与足量 分别与足量 和 和 反应,生成物中金属元素的化合价不同 反应,生成物中金属元素的化合价不同 |
C. 分别与 分别与 和 和 反应,反应的类型不同 反应,反应的类型不同 |
D. 分别与氢氧化钠水溶液和氢氧化钠醇溶液反应,生成的溴化物不同 分别与氢氧化钠水溶液和氢氧化钠醇溶液反应,生成的溴化物不同 |
您最近一年使用:0次
2024-05-16更新
|
135次组卷
|
2卷引用:2024届重庆市南开中学校高三下学期5月月考化学试题
名校
解题方法
3 . 某同学利用W形管和V形管安装了下面微型实验装置,进行 的制备及探究
的制备及探究 的漂白性实验。下列说法正确的是
的漂白性实验。下列说法正确的是
 的制备及探究
的制备及探究 的漂白性实验。下列说法正确的是
的漂白性实验。下列说法正确的是
| A.固体粉末甲为二氧化锰 |
B.鲜花花瓣褪色说明 具有漂白性 具有漂白性 |
| C.W形管和V形管的玻璃泡能防止倒吸 |
D.溶液乙为碱液,与安全气球共同防止 逸出 逸出 |
您最近一年使用:0次
2024-05-14更新
|
161次组卷
|
3卷引用:广东省梅州市部分学校2024届高三下学期5月联考化学试卷
4 . 下列物质存储或使用方法正确的是
| A.新制氯水保存于带玻璃塞的棕色广口瓶中 |
| B.铁与氯气能反应,所以液氯不可用钢瓶储存 |
| C.金属钠着火用二氧化碳灭火器扑灭 |
| D.铝制餐具不宜用来蒸煮或长时间存放酸性或碱性食物 |
您最近一年使用:0次
名校
解题方法
5 . 如图所示是一个制取 并以
并以 为原料进行特定反应的装置,多余的
为原料进行特定反应的装置,多余的 可以贮存在
可以贮存在 瓶中,其中各试剂瓶中所装试剂为:B(氢硫酸)、C(淀粉-KI溶液)、D(水)、F(紫色石蕊试液)。
瓶中,其中各试剂瓶中所装试剂为:B(氢硫酸)、C(淀粉-KI溶液)、D(水)、F(紫色石蕊试液)。 烧瓶中的固体为
烧瓶中的固体为 ,液体为浓盐酸,则其发生反应的化学方程式为
,液体为浓盐酸,则其发生反应的化学方程式为___________
(2) 中的现象为
中的现象为___________ ,发生反应的离子方程式___________ 。
(3)装置 中硬质玻璃管内盛有炭粉,若
中硬质玻璃管内盛有炭粉,若 中发生氧化还原反应,其产物为二氧化碳和氯化氢,写出
中发生氧化还原反应,其产物为二氧化碳和氯化氢,写出 中反应的化学方程式:
中反应的化学方程式:___________ 。
(4)D中溶液的存在微粒有___________ (填化学式)。
(5)在F中紫色石蕊试液的颜色变化是___________ 。
(6)G中应盛放___________ 溶液。
 并以
并以 为原料进行特定反应的装置,多余的
为原料进行特定反应的装置,多余的 可以贮存在
可以贮存在 瓶中,其中各试剂瓶中所装试剂为:B(氢硫酸)、C(淀粉-KI溶液)、D(水)、F(紫色石蕊试液)。
瓶中,其中各试剂瓶中所装试剂为:B(氢硫酸)、C(淀粉-KI溶液)、D(水)、F(紫色石蕊试液)。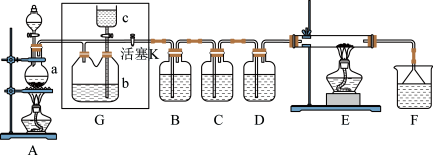
 烧瓶中的固体为
烧瓶中的固体为 ,液体为浓盐酸,则其发生反应的化学方程式为
,液体为浓盐酸,则其发生反应的化学方程式为(2)
 中的现象为
中的现象为(3)装置
 中硬质玻璃管内盛有炭粉,若
中硬质玻璃管内盛有炭粉,若 中发生氧化还原反应,其产物为二氧化碳和氯化氢,写出
中发生氧化还原反应,其产物为二氧化碳和氯化氢,写出 中反应的化学方程式:
中反应的化学方程式:(4)D中溶液的存在微粒有
(5)在F中紫色石蕊试液的颜色变化是
(6)G中应盛放
您最近一年使用:0次
解题方法
6 . 化学来源于生活,服务于生活.下列有关生活中的化学知识叙述正确的是
| A.氯气能使湿润的有色布条褪色,因此氯气有漂白性 |
| B.氯气与烧碱溶液或石灰乳反应都能得到含氯消毒剂 |
| C.洁则灵(主要成分是浓盐酸)与“84”消毒液混用,效果会增强 |
D.测定溶液 的实验中,用干燥 的实验中,用干燥 试纸测定新制氯水的 试纸测定新制氯水的 对测定结果无影响 对测定结果无影响 |
您最近一年使用:0次
解题方法
7 . 氯气常用于自来水的杀菌消毒,实验室常用MnO2和浓盐酸共热制备氯气。
(1)若0.1mol∙L-1 MnO2和25mL12mol∙L-1盐酸混合后缓缓加热,反应完全后向留下的溶液中加入足量AgNO3溶液,生成AgCl沉淀物质的量为___________(不考虑盐酸的挥发)
(2)若改用漂白粉与浓盐酸反应制备氯气,装置如图所示,同时验证氯气性质(其中夹持装置已省略)。___________ 。
②从反应条件看,MnO2和Ca(ClO)2的氧化能力不同,氧化能力较强的是___________ 。
③装置B除了用于除去挥发的HCl,也是安全瓶,目的是监测实验进行时装置C中是否发生堵塞,请写出装置C中发生堵塞时装置B中的实验现象___________ 。
④装置C的作用是验证氯气是否具有漂白性,则装置C中Ⅰ、Ⅱ、Ⅲ处依次应放入的物质是___________ (填字母)。
(3)用氯气对自来水消毒易产生致癌物质,二氧化氯是一种更为高效安全的消毒剂。工业上制备ClO2的反应为2NaClO3+4HCl=2ClO2↑+Cl2↑+2H2O+2NaCl。
①其中氧化剂和还原剂的物质的量之比为___________ 。
②ClO2在杀菌消毒的过程中会生成副产物亚氯酸盐( ),需要将其转化为Cl-除去,下列试剂能实现其转化过程的是
),需要将其转化为Cl-除去,下列试剂能实现其转化过程的是___________ (填序号)。
A.O2 B.FeCl2 C.KI D.KMnO4
③常温常压下,ClO2的消毒能力是等体积Cl2的___________ 倍。(假设ClO2、Cl2全部都被还原为Cl-,没有其它的含氯产物生成)
(1)若0.1mol∙L-1 MnO2和25mL12mol∙L-1盐酸混合后缓缓加热,反应完全后向留下的溶液中加入足量AgNO3溶液,生成AgCl沉淀物质的量为___________(不考虑盐酸的挥发)
| A.等于0.15mol | B.小于0.15mol |
| C.大于0.15mol,小于0.3mol | D.以上结论都不正确 |
(2)若改用漂白粉与浓盐酸反应制备氯气,装置如图所示,同时验证氯气性质(其中夹持装置已省略)。

②从反应条件看,MnO2和Ca(ClO)2的氧化能力不同,氧化能力较强的是
③装置B除了用于除去挥发的HCl,也是安全瓶,目的是监测实验进行时装置C中是否发生堵塞,请写出装置C中发生堵塞时装置B中的实验现象
④装置C的作用是验证氯气是否具有漂白性,则装置C中Ⅰ、Ⅱ、Ⅲ处依次应放入的物质是
| Ⅰ | Ⅱ | Ⅲ | |
| a | 干燥的有色布条 | 碱石灰 | 湿润的有色布条 |
| b | 干燥的有色布条 | 无水硫酸铜 | 湿润的有色布条 |
| c | 湿润的有色布条 | 浓硫酸 | 干燥的有色布条 |
| d | 湿润的有色布条 | 无水氯化钙 | 干燥的有色布条 |
(3)用氯气对自来水消毒易产生致癌物质,二氧化氯是一种更为高效安全的消毒剂。工业上制备ClO2的反应为2NaClO3+4HCl=2ClO2↑+Cl2↑+2H2O+2NaCl。
①其中氧化剂和还原剂的物质的量之比为
②ClO2在杀菌消毒的过程中会生成副产物亚氯酸盐(
 ),需要将其转化为Cl-除去,下列试剂能实现其转化过程的是
),需要将其转化为Cl-除去,下列试剂能实现其转化过程的是A.O2 B.FeCl2 C.KI D.KMnO4
③常温常压下,ClO2的消毒能力是等体积Cl2的
您最近一年使用:0次
名校
解题方法
8 . 下列实验操作、现象和结论都正确的是
| 选项 | 目的 | 实验操作 | 现象和结论 |
| A | 探究胶体和溶液性质的不同 | 在暗处用激光笔照射盛有硫酸铜溶液和氢氧化铁胶体的小烧杯 | 当光束通过胶体时,在垂直于光线的方向可以看到一条光亮的通路,溶液无明显现象。丁达尔效应可以区分溶液和胶体 |
| B | 鉴别某白色固体含有钠元素 | 取一根铜丝,在酒精灯外焰上灼烧,蘸取待检测样品,置于火焰上灼烧,观察火焰颜色 | 火焰颜色呈黄色,证明原样品中含有钠元素 |
| C | 比较 和 和 的氧化性 的氧化性 | 向酸性 溶液中滴入 溶液中滴入 溶液 溶液 | 紫红色溶液变浅,氧化性强弱: |
| D | 探究 是否有漂白性 是否有漂白性 | 将干燥的有色布条和湿润的有色布条分别放入两瓶盛有干燥 的试剂瓶中 的试剂瓶中 | 湿润的有色布条明显褪色,证明干燥的氯气具有漂白性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-04-13更新
|
220次组卷
|
2卷引用:河北省石家庄市河北正定中学2023-2024学年高三下学期第一次月考化学试题
9 . 按下图制取氯气,并检验氯气是否具有漂白性。下列说法正确的是
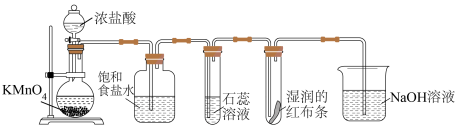
| A.在烧瓶内的反应中,盐酸只表现出还原性 | B.紫色的石蕊溶液先变红,后褪色 |
C.湿润的红布条褪色证明 具有漂白性 具有漂白性 | D.将 溶液改为澄清石灰水,可制备漂白粉 溶液改为澄清石灰水,可制备漂白粉 |
您最近一年使用:0次
名校
解题方法
10 . X、Y、Z、W为原子序数依次增大的短周期主族元素,X、Y同周期位置相邻,Y、Z同主族,Z、W位置相邻。若Y原子的最外层电子数是次外层电子数的3倍,下列说法中正确的是
A.原子半径: |
B.最高价氧化物对应水化物的酸性: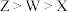 |
| C.4种元素的单质中,Z单质的熔、沸点最高 |
| D.W单质是一种具有漂白性的物质 |
您最近一年使用:0次



