1 . 下列说法中正确的有几项
①钠在空气中燃烧生成淡黄色的Na2O2
②配制480mL0.6mol・L-1的NaOH溶液,需用托盘天平称量氢氧化钠固体11.52g
③盐酸既有氧化性又有还原性
④Fe(OH)3、FeSO4、H2SiO3都不能直接用化合反应制备
⑤SO2能使酸性高锰酸钾溶液褪色,所以它具有漂白性
⑥将质量分数为5%和25%的硫酸等体积混合后,所得溶液中溶质的质量分数小于15%
⑦干燥的C12和氯水均能使鲜花褪色
①钠在空气中燃烧生成淡黄色的Na2O2
②配制480mL0.6mol・L-1的NaOH溶液,需用托盘天平称量氢氧化钠固体11.52g
③盐酸既有氧化性又有还原性
④Fe(OH)3、FeSO4、H2SiO3都不能直接用化合反应制备
⑤SO2能使酸性高锰酸钾溶液褪色,所以它具有漂白性
⑥将质量分数为5%和25%的硫酸等体积混合后,所得溶液中溶质的质量分数小于15%
⑦干燥的C12和氯水均能使鲜花褪色
| A.6项 | B.5项 | C.4项 | D.3项 |
您最近一年使用:0次
解题方法
2 . 化学来源于生活,服务于生活.下列有关生活中的化学知识叙述正确的是
| A.氯气能使湿润的有色布条褪色,因此氯气有漂白性 |
| B.氯气与烧碱溶液或石灰乳反应都能得到含氯消毒剂 |
| C.洁则灵(主要成分是浓盐酸)与“84”消毒液混用,效果会增强 |
D.测定溶液 的实验中,用干燥 的实验中,用干燥 试纸测定新制氯水的 试纸测定新制氯水的 对测定结果无影响 对测定结果无影响 |
您最近一年使用:0次
解题方法
3 . 氯气常用于自来水的杀菌消毒,实验室常用MnO2和浓盐酸共热制备氯气。
(1)若0.1mol∙L-1 MnO2和25mL12mol∙L-1盐酸混合后缓缓加热,反应完全后向留下的溶液中加入足量AgNO3溶液,生成AgCl沉淀物质的量为___________(不考虑盐酸的挥发)
(2)若改用漂白粉与浓盐酸反应制备氯气,装置如图所示,同时验证氯气性质(其中夹持装置已省略)。___________ 。
②从反应条件看,MnO2和Ca(ClO)2的氧化能力不同,氧化能力较强的是___________ 。
③装置B除了用于除去挥发的HCl,也是安全瓶,目的是监测实验进行时装置C中是否发生堵塞,请写出装置C中发生堵塞时装置B中的实验现象___________ 。
④装置C的作用是验证氯气是否具有漂白性,则装置C中Ⅰ、Ⅱ、Ⅲ处依次应放入的物质是___________ (填字母)。
(3)用氯气对自来水消毒易产生致癌物质,二氧化氯是一种更为高效安全的消毒剂。工业上制备ClO2的反应为2NaClO3+4HCl=2ClO2↑+Cl2↑+2H2O+2NaCl。
①其中氧化剂和还原剂的物质的量之比为___________ 。
②ClO2在杀菌消毒的过程中会生成副产物亚氯酸盐( ),需要将其转化为Cl-除去,下列试剂能实现其转化过程的是
),需要将其转化为Cl-除去,下列试剂能实现其转化过程的是___________ (填序号)。
A.O2 B.FeCl2 C.KI D.KMnO4
③常温常压下,ClO2的消毒能力是等体积Cl2的___________ 倍。(假设ClO2、Cl2全部都被还原为Cl-,没有其它的含氯产物生成)
(1)若0.1mol∙L-1 MnO2和25mL12mol∙L-1盐酸混合后缓缓加热,反应完全后向留下的溶液中加入足量AgNO3溶液,生成AgCl沉淀物质的量为___________(不考虑盐酸的挥发)
| A.等于0.15mol | B.小于0.15mol |
| C.大于0.15mol,小于0.3mol | D.以上结论都不正确 |
(2)若改用漂白粉与浓盐酸反应制备氯气,装置如图所示,同时验证氯气性质(其中夹持装置已省略)。

②从反应条件看,MnO2和Ca(ClO)2的氧化能力不同,氧化能力较强的是
③装置B除了用于除去挥发的HCl,也是安全瓶,目的是监测实验进行时装置C中是否发生堵塞,请写出装置C中发生堵塞时装置B中的实验现象
④装置C的作用是验证氯气是否具有漂白性,则装置C中Ⅰ、Ⅱ、Ⅲ处依次应放入的物质是
| Ⅰ | Ⅱ | Ⅲ | |
| a | 干燥的有色布条 | 碱石灰 | 湿润的有色布条 |
| b | 干燥的有色布条 | 无水硫酸铜 | 湿润的有色布条 |
| c | 湿润的有色布条 | 浓硫酸 | 干燥的有色布条 |
| d | 湿润的有色布条 | 无水氯化钙 | 干燥的有色布条 |
(3)用氯气对自来水消毒易产生致癌物质,二氧化氯是一种更为高效安全的消毒剂。工业上制备ClO2的反应为2NaClO3+4HCl=2ClO2↑+Cl2↑+2H2O+2NaCl。
①其中氧化剂和还原剂的物质的量之比为
②ClO2在杀菌消毒的过程中会生成副产物亚氯酸盐(
 ),需要将其转化为Cl-除去,下列试剂能实现其转化过程的是
),需要将其转化为Cl-除去,下列试剂能实现其转化过程的是A.O2 B.FeCl2 C.KI D.KMnO4
③常温常压下,ClO2的消毒能力是等体积Cl2的
您最近一年使用:0次
解题方法
4 . 为除去括号内的杂质,所选用的试剂或方法正确的是
| A.CO2(HCl):将混合气体通过足量的饱和碳酸钠溶液 |
| B.Na2CO3固体粉末(NaHCO3):加热到固体质量不再减轻为止 |
| C.NaHCO3溶液(Na2CO3):向溶液中加入过量Ca(OH)2溶液,过滤 |
| D.Cl2(HCl):将混合气体通过浓硫酸 |
您最近一年使用:0次
2024-04-07更新
|
69次组卷
|
2卷引用:四川省雅安天立学校腾飞高中2023-2024学年高一上学期11月月考化学试题
5 . 由下列实验操作及现象所得结论正确的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 将氯气通入紫色石蕊试液中 | 溶液先变红后褪色 | 氯气具有漂白性 |
| B | 高温加热碳粉和 的混合物 的混合物 | 产物能被磁铁吸引 | 产物中一定含有 单质 单质 |
| C | 用坩埚钳夹住一小块用砂纸仔细打磨过的铝箔在酒精灯上加热 | 金属铝熔化而不滴落下来 | 金属铝的熔点比氧化铝低 |
| D | 分别加热碳酸钠与碳酸氢钠固体 | 试管内壁均出现水珠 | 两种固体均受热分解 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
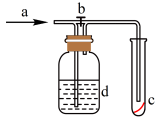
6 . 如图所示,在 处通入未经干燥的氯气。当关闭
处通入未经干燥的氯气。当关闭 阀时,
阀时, 处的红色布条不褪色;当打开
处的红色布条不褪色;当打开 阀后,
阀后, 处的红色布条逐渐褪色。则
处的红色布条逐渐褪色。则 瓶中盛放的溶液可以是
瓶中盛放的溶液可以是
①饱和 溶液 ②
溶液 ② 溶液 ③
溶液 ③ ④浓硫酸
④浓硫酸
 处通入未经干燥的氯气。当关闭
处通入未经干燥的氯气。当关闭 阀时,
阀时, 处的红色布条不褪色;当打开
处的红色布条不褪色;当打开 阀后,
阀后, 处的红色布条逐渐褪色。则
处的红色布条逐渐褪色。则 瓶中盛放的溶液可以是
瓶中盛放的溶液可以是
①饱和
 溶液 ②
溶液 ② 溶液 ③
溶液 ③ ④浓硫酸
④浓硫酸| A.①② | B.①③ | C.②④ | D.③④ |
您最近一年使用:0次
7 . 如图中B为开关,在A处通入氯气。打开B阀时,C中干燥红色布条颜色褪去;当关闭B阀时,C中红色布条颜色无变化。则D瓶中盛有的溶液不可能是
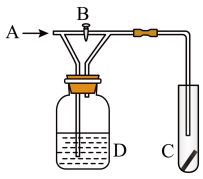

A.浓 | B.饱和NaCl溶液 | C.浓NaOH溶液 | D.浓KI溶液 |
您最近一年使用:0次
名校
8 . 实验室制备 的原理是用亚氯酸钠固体与氯气反应:
的原理是用亚氯酸钠固体与氯气反应: 配平该氧化还原反应方程式,并用单线桥标出电子转移方向和数目
配平该氧化还原反应方程式,并用单线桥标出电子转移方向和数目_______ 。

 与
与 用作消毒剂时均被还原为
用作消毒剂时均被还原为 ,则
,则 的消毒能力是等质量的
的消毒能力是等质量的 的
的_______ 倍(保留小数点后2位,消毒能力可以用氧化剂转移电子数来衡量)。
 的原理是用亚氯酸钠固体与氯气反应:
的原理是用亚氯酸钠固体与氯气反应: 配平该氧化还原反应方程式,并用单线桥标出电子转移方向和数目
配平该氧化还原反应方程式,并用单线桥标出电子转移方向和数目
 与
与 用作消毒剂时均被还原为
用作消毒剂时均被还原为 ,则
,则 的消毒能力是等质量的
的消毒能力是等质量的 的
的
您最近一年使用:0次
名校
9 . 工业氯气通过电解饱和食盐水制得
(1)图(1)中,铁棒作_______ 极,电极反应式是_______ 。
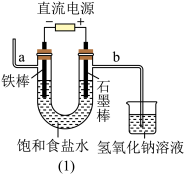
(2)检验导管b出来的气体可以用_______ ,反应的化学方程式是:_______ ;电解饱和食盐水的化学反应方程式为_______ 。
(3)图(1)方法制得的固体烧碱中可能混有少量NaCl,请写出检验是否混有NaCl的实验方法:_______ 。
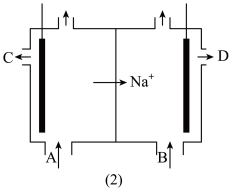
(4)下列关于图(2)的说法正确的是_______。
(5)工业上利用 与
与 反应制盐酸时使用过量的
反应制盐酸时使用过量的 ,理由是
,理由是_______ 。
A.氯气有毒 B.氯气可溶于水 C.氢气密度小
(1)图(1)中,铁棒作

(2)检验导管b出来的气体可以用
(3)图(1)方法制得的固体烧碱中可能混有少量NaCl,请写出检验是否混有NaCl的实验方法:
(4)下列关于图(2)的说法正确的是_______。

| A.A与C、B与D溶质相同 | B.A、B通入的均为浓溶液 |
| C.理论上NaCl利用率可达100% | D.图(2)是负离子交换膜法示意图 |
(5)工业上利用
 与
与 反应制盐酸时使用过量的
反应制盐酸时使用过量的 ,理由是
,理由是A.氯气有毒 B.氯气可溶于水 C.氢气密度小
您最近一年使用:0次
名校
10 . 下列关于氯气与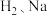 反应的叙述不正确的是
反应的叙述不正确的是
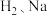 反应的叙述不正确的是
反应的叙述不正确的是| A.都有电子得失 | B.均放出热量 | C.都有白烟产生 | D.反应类型相同 |
您最近一年使用:0次



