1 . 下列说法中正确的有几项
①钠在空气中燃烧生成淡黄色的Na2O2
②配制480mL0.6mol・L-1的NaOH溶液,需用托盘天平称量氢氧化钠固体11.52g
③盐酸既有氧化性又有还原性
④Fe(OH)3、FeSO4、H2SiO3都不能直接用化合反应制备
⑤SO2能使酸性高锰酸钾溶液褪色,所以它具有漂白性
⑥将质量分数为5%和25%的硫酸等体积混合后,所得溶液中溶质的质量分数小于15%
⑦干燥的C12和氯水均能使鲜花褪色
①钠在空气中燃烧生成淡黄色的Na2O2
②配制480mL0.6mol・L-1的NaOH溶液,需用托盘天平称量氢氧化钠固体11.52g
③盐酸既有氧化性又有还原性
④Fe(OH)3、FeSO4、H2SiO3都不能直接用化合反应制备
⑤SO2能使酸性高锰酸钾溶液褪色,所以它具有漂白性
⑥将质量分数为5%和25%的硫酸等体积混合后,所得溶液中溶质的质量分数小于15%
⑦干燥的C12和氯水均能使鲜花褪色
| A.6项 | B.5项 | C.4项 | D.3项 |
您最近一年使用:0次
名校
解题方法
2 . 某学生设计下列实验装置利用 和浓盐酸制备氯气,并用氯气与潮湿的消石灰反应制取少量漂白粉(这是一个放热反应)。回答下列问题:
和浓盐酸制备氯气,并用氯气与潮湿的消石灰反应制取少量漂白粉(这是一个放热反应)。回答下列问题:
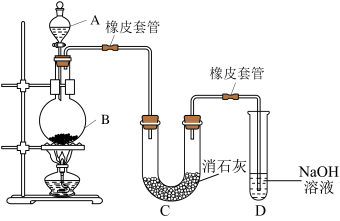
(1)写出装置B中制取氯气的化学方程式:___________ 。
(2)漂白粉在U形管中生成,实验结果所得漂白粉 产率太低。经分析并查阅资料发现,主要原因是在U形管中存在两个副反应:
产率太低。经分析并查阅资料发现,主要原因是在U形管中存在两个副反应:
①温度较高时氯气与消石灰反应生成 ,写出该副反应的化学方程式
,写出该副反应的化学方程式___________ ,为避免发生该反应可采取的措施是___________ 。
②试判断另一个副反应是___________ (写出此反应方程式)。为避免此副反应的发生,可采取的措施是在B、C之间连接一个盛有___________ 的洗气瓶。
 和浓盐酸制备氯气,并用氯气与潮湿的消石灰反应制取少量漂白粉(这是一个放热反应)。回答下列问题:
和浓盐酸制备氯气,并用氯气与潮湿的消石灰反应制取少量漂白粉(这是一个放热反应)。回答下列问题:
(1)写出装置B中制取氯气的化学方程式:
(2)漂白粉在U形管中生成,实验结果所得漂白粉
 产率太低。经分析并查阅资料发现,主要原因是在U形管中存在两个副反应:
产率太低。经分析并查阅资料发现,主要原因是在U形管中存在两个副反应:①温度较高时氯气与消石灰反应生成
 ,写出该副反应的化学方程式
,写出该副反应的化学方程式②试判断另一个副反应是
您最近一年使用:0次
3 . 氯气与水的反应为 。氯水具有多种性质,研究小组同学用氯水分别与紫色石蕊溶液,
。氯水具有多种性质,研究小组同学用氯水分别与紫色石蕊溶液, 溶液反应。请完成下列问题:
溶液反应。请完成下列问题:
(1)向紫色石蕊溶液中滴加氯水的现象是___________ ,证明氯水中含有的微粒有___________ 。
(2)向 溶液中滴加少量氯水,证明氯水有氧化性的实验方案是:取适量反应后溶液于试管中,
溶液中滴加少量氯水,证明氯水有氧化性的实验方案是:取适量反应后溶液于试管中,___________ ,则证明氯水具有氧化性。
(3)氯水光照时黄绿色会逐渐变浅直至消失,并产生无色气体,请用平衡理论解释黄绿色变浅的原因:________ 。
 。氯水具有多种性质,研究小组同学用氯水分别与紫色石蕊溶液,
。氯水具有多种性质,研究小组同学用氯水分别与紫色石蕊溶液, 溶液反应。请完成下列问题:
溶液反应。请完成下列问题:(1)向紫色石蕊溶液中滴加氯水的现象是
(2)向
 溶液中滴加少量氯水,证明氯水有氧化性的实验方案是:取适量反应后溶液于试管中,
溶液中滴加少量氯水,证明氯水有氧化性的实验方案是:取适量反应后溶液于试管中,(3)氯水光照时黄绿色会逐渐变浅直至消失,并产生无色气体,请用平衡理论解释黄绿色变浅的原因:
您最近一年使用:0次
4 .  易升华,易潮解,主要用于金属蚀刻、污水处理、印染滚筒刻花、电子工业线路板及荧光数字筒生产等领域,实验室用下列装置经组合制备无水
易升华,易潮解,主要用于金属蚀刻、污水处理、印染滚筒刻花、电子工业线路板及荧光数字筒生产等领域,实验室用下列装置经组合制备无水 ,下列说法错误的是
,下列说法错误的是

 易升华,易潮解,主要用于金属蚀刻、污水处理、印染滚筒刻花、电子工业线路板及荧光数字筒生产等领域,实验室用下列装置经组合制备无水
易升华,易潮解,主要用于金属蚀刻、污水处理、印染滚筒刻花、电子工业线路板及荧光数字筒生产等领域,实验室用下列装置经组合制备无水 ,下列说法错误的是
,下列说法错误的是
A.装置D中冷水作用是降温促进 的凝华 的凝华 |
| B.装置E的作用是除去氯气中的氯化氢杂质 |
| C.按气流方向,装置的连接顺序为ahibcfgde |
D.装置B的作用是防止空气中的水使 发生潮解并吸收未反应的氯气 发生潮解并吸收未反应的氯气 |
您最近一年使用:0次
名校
5 . 某小组同学探究不同条件下氯气与二价锰化合物的反应,实验记录如下:
资料:水溶液中, 为棕黑色沉淀,
为棕黑色沉淀, 为白色沉淀,
为白色沉淀, 呈绿色;浓碱性条件下,
呈绿色;浓碱性条件下, 可被
可被 还原为
还原为 ;
; 的氧化性随碱性增强而减弱。
的氧化性随碱性增强而减弱。
下列说法错误的是
| 序号 | 实验方案 | 实验现象 | |
| 实验装置 | 试剂a | ||
| ① | 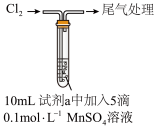 | 水 | 产生黑色沉淀,放置后不发生变化 |
| ② | 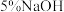 溶液 溶液 | 产生黑色沉淀,放置后溶液变为紫色,仍有沉淀 | |
| ③ | 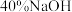 溶液 溶液 | 产生黑色沉淀,放置后溶液变为紫色,仍有沉淀 | |
| ④ | 取③中放置后的悬浊液 ,加入 ,加入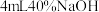 溶液 溶液 | 溶液紫色迅速变为绿色,且绿色缓慢加深 | |
| ⑤ | 取③中放置后的悬浊液 ,加入 ,加入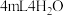 | 溶液紫色缓慢加深 | |
 为棕黑色沉淀,
为棕黑色沉淀, 为白色沉淀,
为白色沉淀, 呈绿色;浓碱性条件下,
呈绿色;浓碱性条件下, 可被
可被 还原为
还原为 ;
; 的氧化性随碱性增强而减弱。
的氧化性随碱性增强而减弱。下列说法错误的是
| A.对比实验①和②可知,碱性环境中,二价锰化合物可被氧化到更高价态 |
B.④中溶液紫色迅速变为绿色的可能原因是: 被 被 还原生成 还原生成 |
C.⑤中紫色缓慢加深的主要原因是: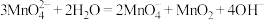 |
D.③中未得到绿色溶液,可能是因为 被氧化为 被氧化为 的反应速率快于 的反应速率快于 被还原为 被还原为 的反应速率 的反应速率 |
您最近一年使用:0次
2023-12-12更新
|
260次组卷
|
2卷引用:安徽省示范高中培优联盟2023-2024学年高二上学期冬季联赛化学试题
名校
解题方法
6 . 自磷(P4)与氯气反应的能量变化如图所示。回答下列问题:
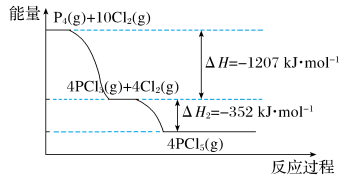
(1)白磷在氯气中燃烧的各度是放热反应,但是启动反应时需要点燃或加热,其原因是_____ 。
(2)PCl5(g)=PCl3(g)+Cl2(g) △H=_____ 88kJ/mol。
(3)写出白磷蒸气在氯气中反应生成五氯化磷气体的热化学方程式:_____ 。
(4)在密闭容器中充入1molPCl3(g)和3molCl2(g),发生反应:PCl3(g)+Cl2(g)=PCl5(g),放出热量Q的范围为_____ 。
(5)白磷在氯气中燃烧,开始引燃之后,停止加热,反应持续进行至一种物质(或两种物质)完全反应,其原因是_____ 。

(1)白磷在氯气中燃烧的各度是放热反应,但是启动反应时需要点燃或加热,其原因是
(2)PCl5(g)=PCl3(g)+Cl2(g) △H=
(3)写出白磷蒸气在氯气中反应生成五氯化磷气体的热化学方程式:
(4)在密闭容器中充入1molPCl3(g)和3molCl2(g),发生反应:PCl3(g)+Cl2(g)=PCl5(g),放出热量Q的范围为
(5)白磷在氯气中燃烧,开始引燃之后,停止加热,反应持续进行至一种物质(或两种物质)完全反应,其原因是
您最近一年使用:0次
名校
7 . 用NA表示阿伏加德罗常数的值,下列叙述中正确的是
| A.1 mol重水比1 mol水多NA个质子 |
| B.120g NaHSO4 和KHSO3的固体混合物中含有的阳离子数为NA |
| C.1mol Cl2与足量Fe反应,转移的电子数为3NA |
| D.0.1mol O2和0.2mol NO于密闭容器中充分反应后,分子总数为0.2NA |
您最近一年使用:0次
名校
8 . 下列物质中,不能 由单质与单质直接化合生成的是
| A.FeCl2 | B.Fe3O4 | C.CuCl2 | D.Na2O |
您最近一年使用:0次
2023-11-06更新
|
270次组卷
|
7卷引用:“贵百河”2023-2024学年高二上学期10月新高考月考测试化学试题
9 . 设 表示阿伏加德罗常数的值。下列叙述正确的是
表示阿伏加德罗常数的值。下列叙述正确的是
 表示阿伏加德罗常数的值。下列叙述正确的是
表示阿伏加德罗常数的值。下列叙述正确的是A.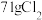 溶于适量水中,所得溶液中 溶于适量水中,所得溶液中 和 和 微粒总数为 微粒总数为 |
B.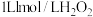 溶液完全反应,转移的电子数目一定为 溶液完全反应,转移的电子数目一定为 |
C.标准状况下,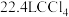 中含有 中含有 键的个数为 键的个数为 |
D.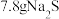 和 和 的混合物中,含有的离子总数为 的混合物中,含有的离子总数为 |
您最近一年使用:0次
名校
解题方法
10 . 利用甲烷与氯气发生取代反应的副产品制取盐酸的设想在工业上已成为现实。某化学兴趣小组在实验室中模拟上述过程,其设计的模拟装置如图:
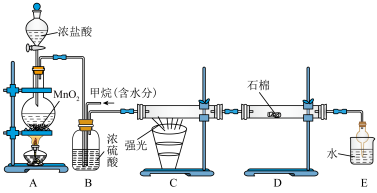
(1)有人认为E中有氯化氢产生,不能证明甲烷与氯气发生了取代反应,你认为他的看法_______ (填“正确”或“不正确”),理由是_______ 。
(2)B有三种功能:①控制气流速度;②混匀混合气体;③________ 。
(3)一段时间后发现D中的棉花由白色变为蓝色,则棉花上可能预先滴有________ 溶液。
(4)E中除盐酸外,还含有机物,从E中分离出盐酸的最佳方法为_______ (选填编号)。

(1)有人认为E中有氯化氢产生,不能证明甲烷与氯气发生了取代反应,你认为他的看法
(2)B有三种功能:①控制气流速度;②混匀混合气体;③
(3)一段时间后发现D中的棉花由白色变为蓝色,则棉花上可能预先滴有
(4)E中除盐酸外,还含有机物,从E中分离出盐酸的最佳方法为
| A.结晶法 | B.蒸馏法 | C.萃取分液法 | D.水洗分液法 |
您最近一年使用:0次



