1 . 氯气是一种重要的化工原料,能与有机物和无机物发生反应生成多种氯化物。现用如图装置制取氯气并进行一系列的实验探究。
(1)装置1用来制备纯净、干燥的氯气。
①制备氯气的化学方程式:___________ 。
②B中溶液为___________ ,作用是___________ ,C中液体为___________ ,B和C的位置能否颠倒?___________ (填“能”或“不能”)。
(2)将装置1与装置2连接起来探究氯气是否具有漂白性。
①装置G和H中分别观察到的现象是___________ 。
② 溶液的作用是
溶液的作用是___________ ,写出相应反应的化学方程式:___________ 。工业上常用廉价的石灰乳吸收氯气制得漂白粉,漂白粉的有效成分是___________ (填化学式)。
(3)氯水具有多种成分(分子和离子):
①氯水呈浅黄绿色,是因为有___________ (写化学式)。
②将紫色石蕊溶液滴入新制氯水中,溶液显___________ 色,起作用的微粒是___________ ,一段时间后,溶液的颜色褪去,颜色褪去过程中起作用的微粒是___________ (写化学式)。
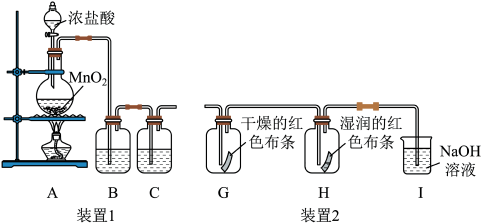
(1)装置1用来制备纯净、干燥的氯气。
①制备氯气的化学方程式:
②B中溶液为
(2)将装置1与装置2连接起来探究氯气是否具有漂白性。
①装置G和H中分别观察到的现象是
②
 溶液的作用是
溶液的作用是(3)氯水具有多种成分(分子和离子):
①氯水呈浅黄绿色,是因为有
②将紫色石蕊溶液滴入新制氯水中,溶液显
您最近一年使用:0次
2 . 氯气、漂白液、漂白粉都是生活中常用的含氯消毒剂。“84”消毒液说明书如图,请回答下列问题:
(1)漂白粉的主要成分为___________ (填化学式,下同),有效成分为___________ 。工业上用石灰乳和氯气制备漂白粉,写出反应的化学方程式:___________ 。
(2)洁厕剂的主要成分为稀盐酸,用化学方程式解释注意事项中不可与洁厕剂混合使用的原因:___________ 。
(3) 可直接用于杀菌消毒,但常常把氯气制成漂白粉或“84”消毒液,主要目的为
可直接用于杀菌消毒,但常常把氯气制成漂白粉或“84”消毒液,主要目的为________ (填标号)。
A.增强漂白能力和消毒作用
B.将 转化为较稳定的物质,便于保存和运输
转化为较稳定的物质,便于保存和运输
C.提高氯的质量分数,有利于漂白、消毒
(4)某小组在实验室制备“84”消毒液,并进行性质探究。
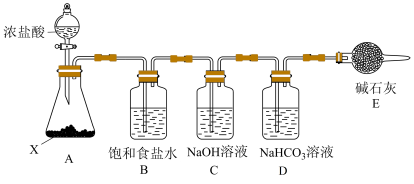
①装置E盛放碱石灰的仪器的名称是___________ ,装置E的作用是___________ 。
②若撤去装置B,则可能产生的后果是___________ 。
③装置C中发生制备消毒液的反应,写出反应的离子方程式:___________ 。
| “84”消毒液说明书 | 药品名称 | “84”消毒液 |
| 主要成分 | NaClO,有效氯含量为 | |
| 注意事项 | 不可与洁厕剂或其他消毒液混合使用 | |
| 用法用量 | 稀释后洗刷白色衣物、浴缸等(1:200水溶液),餐饮具、瓜果等(1:100水溶液) |
(1)漂白粉的主要成分为
(2)洁厕剂的主要成分为稀盐酸,用化学方程式解释注意事项中不可与洁厕剂混合使用的原因:
(3)
 可直接用于杀菌消毒,但常常把氯气制成漂白粉或“84”消毒液,主要目的为
可直接用于杀菌消毒,但常常把氯气制成漂白粉或“84”消毒液,主要目的为A.增强漂白能力和消毒作用
B.将
 转化为较稳定的物质,便于保存和运输
转化为较稳定的物质,便于保存和运输C.提高氯的质量分数,有利于漂白、消毒
(4)某小组在实验室制备“84”消毒液,并进行性质探究。

①装置E盛放碱石灰的仪器的名称是
②若撤去装置B,则可能产生的后果是
③装置C中发生制备消毒液的反应,写出反应的离子方程式:
您最近一年使用:0次
2023-12-07更新
|
124次组卷
|
2卷引用:辽宁省葫芦岛市协作校2023-2024学年高一上学期第二次考试化学试题
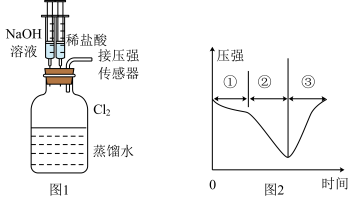
3 . 用图1所示装置向装有一瓶氯气的集气瓶中添加适量的蒸馏水,振荡,先利用注射器滴加 溶液,再利用注射器滴加稀盐酸,用压强传感器测得集气瓶内的压强随时间变化的曲线如图2所示。下列说法正确的是
溶液,再利用注射器滴加稀盐酸,用压强传感器测得集气瓶内的压强随时间变化的曲线如图2所示。下列说法正确的是
 溶液,再利用注射器滴加稀盐酸,用压强传感器测得集气瓶内的压强随时间变化的曲线如图2所示。下列说法正确的是
溶液,再利用注射器滴加稀盐酸,用压强传感器测得集气瓶内的压强随时间变化的曲线如图2所示。下列说法正确的是
| A.阶段①说明氯气溶于水,溶于水的氯气全部与水反应 |
| B.阶段②的压强变小,可利用该过程发生的反应制备漂白粉 |
C.阶段③发生反应的离子方程式为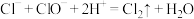 |
D.若将 换成 换成 ,则压强变化不会出现图2趋势 ,则压强变化不会出现图2趋势 |
您最近一年使用:0次
2023-11-15更新
|
437次组卷
|
2卷引用:辽宁省鞍山市第一中学2023-2024学年高一上学期期中考试化学试题
4 .  在现代工业生产中应用广泛。某化学研究性学习小组模拟工业流程制备无水
在现代工业生产中应用广泛。某化学研究性学习小组模拟工业流程制备无水 ,再用副产品
,再用副产品 溶液吸收有毒的
溶液吸收有毒的 。
。
已知:无水 在空气中易潮解,加热易升华。他们设计了制备无水
在空气中易潮解,加热易升华。他们设计了制备无水 的实验方案,装置示意图(加热及夹持装置略去)及操作步骤如下:
的实验方案,装置示意图(加热及夹持装置略去)及操作步骤如下:
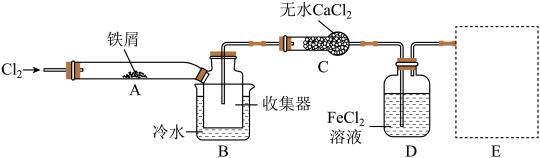
①检验装置的气密性;
②通入干燥的 ,赶尽装置中的空气;
,赶尽装置中的空气;
③用酒精灯在铁屑下方加热至反应完成;
④……
⑤体系冷却后,停止通入 ,并用干燥的
,并用干燥的 赶尽
赶尽 ,将收集器密封。
,将收集器密封。
请回答下列问题:
(1)装置A中发生反应的化学方程式为_______ 。第③步加热后,生成的烟状 大部分进入收集器,少量沉积在反应管A右端,要使沉积的
大部分进入收集器,少量沉积在反应管A右端,要使沉积的 进入收集器,第④步操作是
进入收集器,第④步操作是_______ 。
(2)操作步骤中,为防止 潮解所采取的措施有
潮解所采取的措施有_______ (填步骤序号)。
(3)装置B中冷水浴的作用为_______ ;装置C的名称为_______ 。
(4)为将尾气吸收完全,在虚线框中可以使用的装置有_______ 。

(5)①装置D吸收氯气属于化合反应,写出该反应的化学方程式:_______ 。
②若用装置D反应后得到的溶液吸收 ,得到单质硫,对应的离子方程式为
,得到单质硫,对应的离子方程式为_______ 。
 在现代工业生产中应用广泛。某化学研究性学习小组模拟工业流程制备无水
在现代工业生产中应用广泛。某化学研究性学习小组模拟工业流程制备无水 ,再用副产品
,再用副产品 溶液吸收有毒的
溶液吸收有毒的 。
。已知:无水
 在空气中易潮解,加热易升华。他们设计了制备无水
在空气中易潮解,加热易升华。他们设计了制备无水 的实验方案,装置示意图(加热及夹持装置略去)及操作步骤如下:
的实验方案,装置示意图(加热及夹持装置略去)及操作步骤如下:
①检验装置的气密性;
②通入干燥的
 ,赶尽装置中的空气;
,赶尽装置中的空气;③用酒精灯在铁屑下方加热至反应完成;
④……
⑤体系冷却后,停止通入
 ,并用干燥的
,并用干燥的 赶尽
赶尽 ,将收集器密封。
,将收集器密封。请回答下列问题:
(1)装置A中发生反应的化学方程式为
 大部分进入收集器,少量沉积在反应管A右端,要使沉积的
大部分进入收集器,少量沉积在反应管A右端,要使沉积的 进入收集器,第④步操作是
进入收集器,第④步操作是(2)操作步骤中,为防止
 潮解所采取的措施有
潮解所采取的措施有(3)装置B中冷水浴的作用为
(4)为将尾气吸收完全,在虚线框中可以使用的装置有

(5)①装置D吸收氯气属于化合反应,写出该反应的化学方程式:
②若用装置D反应后得到的溶液吸收
 ,得到单质硫,对应的离子方程式为
,得到单质硫,对应的离子方程式为
您最近一年使用:0次
名校
解题方法
5 . 氯气是一种重要的化工原料,在工农业生产、生活中有着重要的应用。某化学兴趣小组同学对氯气的性质进行如下探究:
(1)兴趣小组同学按下图装置进行实验,探究Cl2 的漂白性。
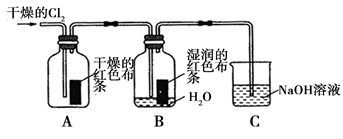
①通入Cl2 后,观察到的现象是_______ 根据现象可得出的结论是_____ 。
②集气瓶B发生反应的离子方程式是_____ 。
③C装置的作用是___________ ,若有2.24L(标准状况下)Cl2被NaOH溶液完全吸收,则反应过程中转移的电子为_______ mol。
(2)兴趣小组同学按下图装置进行实验,探究Cl2的氧化性。
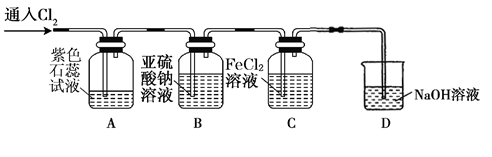
①实验开始后,观察装置A 中的现象是_____ 。
②装置C中发生反应的离子方程式是______ 。
③停止通入氯气,取装置B中少量溶液于洁净的试管中,向其中滴加足量稀盐酸,再向其中滴加氯化钡溶液,有白色沉淀生成。则通入Cl2 时装置B中发生 反应的离子方程式是__________ 。
(1)兴趣小组同学按下图装置进行实验,探究Cl2 的漂白性。

①通入Cl2 后,观察到的现象是
②集气瓶B发生反应的离子方程式是
③C装置的作用是
(2)兴趣小组同学按下图装置进行实验,探究Cl2的氧化性。

①实验开始后,观察装置A 中的现象是
②装置C中发生反应的离子方程式是
③停止通入氯气,取装置B中少量溶液于洁净的试管中,向其中滴加足量稀盐酸,再向其中滴加氯化钡溶液,有白色沉淀生成。则通入Cl2 时装置B中发生 反应的离子方程式是
您最近一年使用:0次
2016-12-09更新
|
718次组卷
|
4卷引用:辽宁省六校协作体2017-2018学年高一下学期开学考试化学试题
辽宁省六校协作体2017-2018学年高一下学期开学考试化学试题(已下线)2014-2015学年山东省潍坊三县市高一上学期联考化学试卷2015-2016学年青海省平安县第一高中高一入学化学试卷四川省广安友谊中学2018-2019学年高一上学期期末模拟化学试题
解题方法
6 . 氯气(Cl2)是一种重要的化工原料,大量用于制造盐酸、有机溶剂、农药、燃料和药品等。氯气在实验室中可通过MnO2和浓盐酸混合加热制备,实验装置见图;
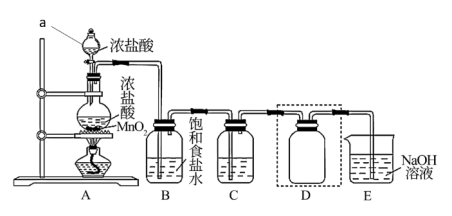
(1)Cl2的电子式为__________ 。
(2)仪器a的名称_______ ,装置B的作用是_______ 。
(3)装置D用于收集Cl2,请将装置D中的导气管补充完整:_______ 。
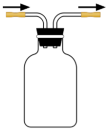
(4)装置E用于吸收尾气Cl2,E中发生反应的化学方程式是____________ 。
(5)可用Cl2和冷的石灰乳反应制备漂白粉,漂白粉中的有效成分是_______ 。(填化学式)

(1)Cl2的电子式为
(2)仪器a的名称
(3)装置D用于收集Cl2,请将装置D中的导气管补充完整:

(4)装置E用于吸收尾气Cl2,E中发生反应的化学方程式是
(5)可用Cl2和冷的石灰乳反应制备漂白粉,漂白粉中的有效成分是
您最近一年使用:0次
7 . 为探究氯气的某些性质,设计如下装置。下列有关说法和反应的离子方程式中都正确的是
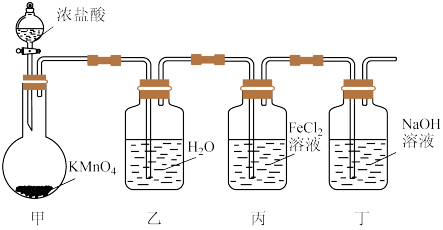

A.甲产生黄绿色气体:2MnO +10Cl-+16H+=2Mn2++5Cl2↑+8H2O +10Cl-+16H+=2Mn2++5Cl2↑+8H2O |
B.乙可制得饱和氯水:Cl2+H2O H++Cl-+HClO H++Cl-+HClO |
| C.丙中溶液显棕黄色:Cl2+Fe2+=2Cl-+Fe3+ |
| D.丁可用于制备漂白粉:Cl2+2OH-=H2O+Cl-+ClO- |
您最近一年使用:0次
8 . 某学习小组查阅资料并用以下装置制备次氯酸溶液,回答下列问题:
查阅资料:
Ⅰ、25℃时,1体积的水可溶解约2体积的氯气,氯气更易溶于有机溶剂,如四氯化碳中;
Ⅱ、常温常压下, 为棕黄色气体,沸点为3.8℃,42℃以上会分解生成
为棕黄色气体,沸点为3.8℃,42℃以上会分解生成 和
和 ,高浓度的
,高浓度的 易爆炸;
易爆炸;
Ⅲ、将氯气和空气(不参与反应)按体积比1:3混合通入潮湿的碳酸钠中发生反应: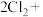
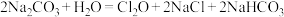 ,可制得
,可制得 ,
, 易溶于水,用水吸收
易溶于水,用水吸收 (不含
(不含 )制得次氯酸溶液。
)制得次氯酸溶液。

(1)f仪器的名称是___________ 。
(2)各装置的连接顺序为___________→___________→___________→___________→E。___________
(3)装置B中多孔球泡和搅拌棒的作用是___________ ,反应过程中,装置B需放在冷水中,其目的是___________ 。
(4)装置C的主要作用是___________ 。
(5)装置D中通入空气的主要目的是___________ 。
(6)分别用等物质的量的 和
和 杀菌消毒,转移电子的物质的量之比为
杀菌消毒,转移电子的物质的量之比为___________ 。
查阅资料:
Ⅰ、25℃时,1体积的水可溶解约2体积的氯气,氯气更易溶于有机溶剂,如四氯化碳中;
Ⅱ、常温常压下,
 为棕黄色气体,沸点为3.8℃,42℃以上会分解生成
为棕黄色气体,沸点为3.8℃,42℃以上会分解生成 和
和 ,高浓度的
,高浓度的 易爆炸;
易爆炸;Ⅲ、将氯气和空气(不参与反应)按体积比1:3混合通入潮湿的碳酸钠中发生反应:
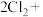
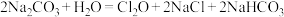 ,可制得
,可制得 ,
, 易溶于水,用水吸收
易溶于水,用水吸收 (不含
(不含 )制得次氯酸溶液。
)制得次氯酸溶液。
(1)f仪器的名称是
(2)各装置的连接顺序为___________→___________→___________→___________→E。
(3)装置B中多孔球泡和搅拌棒的作用是
(4)装置C的主要作用是
(5)装置D中通入空气的主要目的是
(6)分别用等物质的量的
 和
和 杀菌消毒,转移电子的物质的量之比为
杀菌消毒,转移电子的物质的量之比为
您最近一年使用:0次
名校
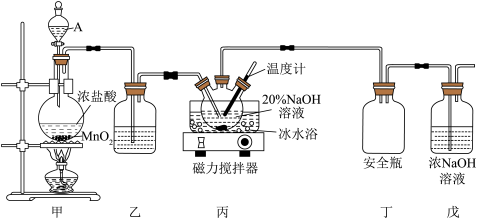
9 . “84消毒液”是以NaClO为主要成分的含氯消毒剂,由于其消毒效果理想、使用方便等特点被一直沿用至今。某化学兴趣小组利用如图所示装置制备含一定游离碱(NaOH)的“84消毒液”。
已知:①氯气与氢氧化钠溶液反应过程中有一定热量放出
②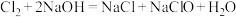 (温度低于35℃)
(温度低于35℃)
 (温度70~80℃)
(温度70~80℃)
回答下列问题:
(1)仪器A的名称为_______ ,装置甲中发生反应的化学方程式为_______ 。
(2)装置乙中盛装试剂为_______ ,若省去装置乙,产生的后果是_______ 。
(3)制备NaClO的反应装置丙需要采用冰水浴且要用温度计控制反应温度,其原因为_______ 。
(4)装置戊的作用为_______ 。
(5)某游泳馆工作人员将“84消毒液”与双氧水两种消毒剂混用,导致游泳池藻类快速生长,池水变绿。一种原因可能是NaClO与 反应产生
反应产生 促进藻类快速生长。该反应说明氧化性:NaClO
促进藻类快速生长。该反应说明氧化性:NaClO_______  (填“>”或“<”);当有0.1 mol
(填“>”或“<”);当有0.1 mol  生成时,转移电子的物质的量为
生成时,转移电子的物质的量为_______ mol。

已知:①氯气与氢氧化钠溶液反应过程中有一定热量放出
②
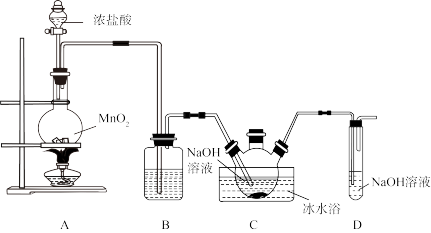
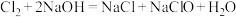 (温度低于35℃)
(温度低于35℃) (温度70~80℃)
(温度70~80℃)回答下列问题:
(1)仪器A的名称为
(2)装置乙中盛装试剂为
(3)制备NaClO的反应装置丙需要采用冰水浴且要用温度计控制反应温度,其原因为
(4)装置戊的作用为
(5)某游泳馆工作人员将“84消毒液”与双氧水两种消毒剂混用,导致游泳池藻类快速生长,池水变绿。一种原因可能是NaClO与
 反应产生
反应产生 促进藻类快速生长。该反应说明氧化性:NaClO
促进藻类快速生长。该反应说明氧化性:NaClO (填“>”或“<”);当有0.1 mol
(填“>”或“<”);当有0.1 mol  生成时,转移电子的物质的量为
生成时,转移电子的物质的量为
您最近一年使用:0次
2022-11-16更新
|
399次组卷
|
4卷引用:辽宁省沈阳、大连、丹东、本溪等协作校2022-2023学年高一上学期期中考试化学试题
2022·安徽合肥·二模
名校
解题方法
10 . 二氯异氰尿酸钠[(CNO)3Cl2Na]是常用的杀菌消毒剂,常温下为白色固体,难溶于冷水。利用高浓度的NaClO溶液和异氰尿酸[(CNO) 3H3]固体制备二氯异氰尿酸钠,实验装置如下图所示(部分夹持装置略)。
已知:①3Cl2+6NaOH 5NaCl+NaClO3+3H2O
5NaCl+NaClO3+3H2O
②2NaClO+(CNO)3H3=(CNO) 3Cl2Na+NaOH+H2O
回答下列问题:
(1)装置A中发生反应的离子方程式为_______ 。
(2)装置B中盛放的试剂为_______ ,若撤去该装置,对C中制备实验产生的影响是_______ 。
(3)三颈烧瓶液面上出现黄绿色气体时,由上口加入(CNO) 3H3固体,反应过程中仍需不断通入Cl2,原因是_______ 。
(4)装置C中冰水浴的目的是_______ 。
(5)通过下列实验可测定二氯异氰尿酸钠样品中有效氯的含量(样品中不含NaClO):
反应原理:
[(CNO)3Cl2]-+H++2H2O=(CNO)3H3+2HClO
HClO+2I-+H+=I2+Cl-+H2O
I2+2S2O =S4O
=S4O +2I-
+2I-
实验步骤:准确称取wg样品配成100mL溶液,取25.00mL于碘量瓶中,加入适量稀硫酸和过量KI溶液,暗处静置充分反应后,用0.1000 mol·L-1Na2S2O3标准溶液滴定至溶液呈微黄色,加入淀粉指示剂继续滴定至终点,消耗Na2S2O3溶液VmL。
①滴定终点的现象是_______ 。
②该样品中有效氯含量的表达式为_______ 。(有效氯=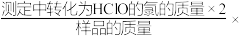 100%)。
100%)。
③若滴定前滴定管尖嘴有气泡,滴定后气泡消失,则有效氯的测定值将_______ (填“偏高”、“偏低”或“无影响”)。

已知:①3Cl2+6NaOH
 5NaCl+NaClO3+3H2O
5NaCl+NaClO3+3H2O②2NaClO+(CNO)3H3=(CNO) 3Cl2Na+NaOH+H2O
回答下列问题:
(1)装置A中发生反应的离子方程式为
(2)装置B中盛放的试剂为
(3)三颈烧瓶液面上出现黄绿色气体时,由上口加入(CNO) 3H3固体,反应过程中仍需不断通入Cl2,原因是
(4)装置C中冰水浴的目的是
(5)通过下列实验可测定二氯异氰尿酸钠样品中有效氯的含量(样品中不含NaClO):
反应原理:
[(CNO)3Cl2]-+H++2H2O=(CNO)3H3+2HClO
HClO+2I-+H+=I2+Cl-+H2O
I2+2S2O
 =S4O
=S4O +2I-
+2I-实验步骤:准确称取wg样品配成100mL溶液,取25.00mL于碘量瓶中,加入适量稀硫酸和过量KI溶液,暗处静置充分反应后,用0.1000 mol·L-1Na2S2O3标准溶液滴定至溶液呈微黄色,加入淀粉指示剂继续滴定至终点,消耗Na2S2O3溶液VmL。
①滴定终点的现象是
②该样品中有效氯含量的表达式为
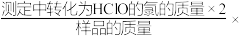 100%)。
100%)。③若滴定前滴定管尖嘴有气泡,滴定后气泡消失,则有效氯的测定值将
您最近一年使用:0次
2022-04-11更新
|
899次组卷
|
8卷引用:化学-2022年高考押题预测卷01(辽宁卷)
(已下线)化学-2022年高考押题预测卷01(辽宁卷)安徽省合肥市2022届高三第二次教学质量检测理综化学试题(已下线)必刷卷03-2022年高考化学考前信息必刷卷(全国甲卷)山东省泰安市2022届高三下学期三轮验收考试化学试题湖南省衡山县岳云中学2021-2022学年高三下学期期中考试化学试卷山东省泰安市2022-2023学年高三上学期开学考试化学试题山东省济宁邹城市第二中学2022-2023学年高三9月月考化学试题甘肃省武威第六中学2022-2023学年高三上学期第三次过关考试化学试题



