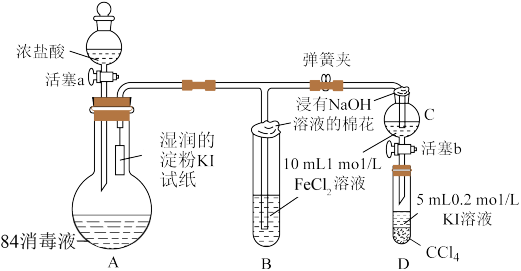
1 . 已知Cl2+2I-=2C1-+I2。为验证Fe3+、I2氧化性的相对强弱。某小组用下图所示装置进行实验(夹持仪器已略去,气密性已检验)。
实验过程:
I.打开弹簧夹,打开活塞a,滴加浓盐酸。
II.当B和C中的溶液都变为黄色时,夹紧弹簧夹。
III.向B中加入一定量KSCN溶液,混合液显红色,关闭活塞a。
IV.打开活塞b,将C中的溶液滴入D中,关闭活塞b,取下D振荡、静置。
请回答下列问题:
(1)A中产生黄绿色气体,写出A中发生反应的离子方程式_______ 。
(2)验证氯气的氧化性强于碘单质的实验现象是_______ 。
(3)B中通入氯气溶液变黄再向B中滴加KSCN溶液,溶液变红的离子方程式是_______ 。
(4)C中的溶液滴入D中,振荡、静置,若产生_______ 现象,则说明Fe3+的氧化性强于碘单质,对应反应的离子方程式是_______ 。有人认为这个实验设计存在缺陷,其理由是_______ 。
(5)浸有氢氧化钠溶液的棉花作用是_______ 。

实验过程:
I.打开弹簧夹,打开活塞a,滴加浓盐酸。
II.当B和C中的溶液都变为黄色时,夹紧弹簧夹。
III.向B中加入一定量KSCN溶液,混合液显红色,关闭活塞a。
IV.打开活塞b,将C中的溶液滴入D中,关闭活塞b,取下D振荡、静置。
请回答下列问题:
(1)A中产生黄绿色气体,写出A中发生反应的离子方程式
(2)验证氯气的氧化性强于碘单质的实验现象是
(3)B中通入氯气溶液变黄再向B中滴加KSCN溶液,溶液变红的离子方程式是
(4)C中的溶液滴入D中,振荡、静置,若产生
(5)浸有氢氧化钠溶液的棉花作用是
您最近一年使用:0次
解题方法
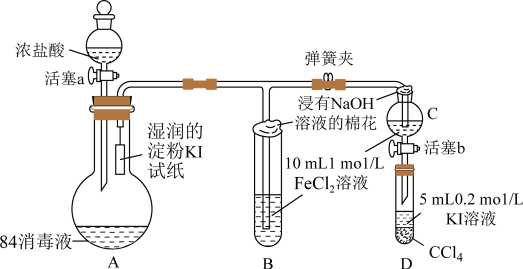
2 . 已知Cl2+2I=2C1-+I2为验证Fe3+、I2氧化性的相对强弱。某小组用如图所示装置进行实验(夹持仪器已略去,气密性已检验)。
实验过程:
I.打开弹簧夹,打开活塞a,滴加浓盐酸。
II.当B和C中的溶液都变为黄色时,夹紧弹簧夹。
III.向B中加入一定量KSCN溶液,混合液显红色,关闭活塞a。
IV.打开活塞b,将C中的溶液滴入D中,关闭活塞b,取下D振荡、静置。
请回答下列问题:
(1)A中产生黄绿色气体,写出A中发生反应的离子方程式_______ 。
(2)验证氯气的氧化性强于碘单质的实验现象是_______ 。
(3)B中通入氯气溶液变黄的离子方程式是______ ;再向B中滴加KSCN溶液,溶液变红的离子方程式是_______ 。
(4)C中的溶液滴入D中,振荡、静置,若产生__________ 现象,则说明Fe3+的氧化性强于碘单质,对应反应的离子方程式是____ 。有人认为这个实验设计存在缺陷,其理由是_______ 。
(5)浸有氢氧化钠溶液的棉花作用是_______ 。

实验过程:
I.打开弹簧夹,打开活塞a,滴加浓盐酸。
II.当B和C中的溶液都变为黄色时,夹紧弹簧夹。
III.向B中加入一定量KSCN溶液,混合液显红色,关闭活塞a。
IV.打开活塞b,将C中的溶液滴入D中,关闭活塞b,取下D振荡、静置。
请回答下列问题:
(1)A中产生黄绿色气体,写出A中发生反应的离子方程式
(2)验证氯气的氧化性强于碘单质的实验现象是
(3)B中通入氯气溶液变黄的离子方程式是
(4)C中的溶液滴入D中,振荡、静置,若产生
(5)浸有氢氧化钠溶液的棉花作用是
您最近一年使用:0次
3 . 高铁酸钠(Na2FeO4)是一种新型绿色消毒剂,主要用于饮用水处理。如图所示物质转化关系为高铁酸钠的一种制备方法及有关性质实验(部分反应产物已略去)。已知A、F为非金属单质气体,B为常见金属单质,E为生活中最常见的调味品,F在标准状况下密度为0.090 。
。

请回答下列问题:
(1)写出D的名称___________ ,E的俗称___________ 。Na2FeO4中Fe元素的化合价为___________ 。
(2)写出反应②的离子方程式:___________ 。
(3)反应③,F在A中点燃的反应现象为:___________ 。
(4)反应④中各物质的反应比例关系如下,请填入相应的反应物和生成物的化学式,并标明电子转移的方向和数目:_____
2 +3
+3 +10NaOH =2Na2FeO4+9
+10NaOH =2Na2FeO4+9 +5H2O
+5H2O
(5)写出反应⑤的化学方程式:___________ 。
 。
。
请回答下列问题:
(1)写出D的名称
(2)写出反应②的离子方程式:
(3)反应③,F在A中点燃的反应现象为:
(4)反应④中各物质的反应比例关系如下,请填入相应的反应物和生成物的化学式,并标明电子转移的方向和数目:
2
 +3
+3 +10NaOH =2Na2FeO4+9
+10NaOH =2Na2FeO4+9 +5H2O
+5H2O(5)写出反应⑤的化学方程式:
您最近一年使用:0次
2021-11-20更新
|
1460次组卷
|
4卷引用:安徽省六安第二中学2023-2024学年高一上学期期末考试化学试题
名校
4 . 实验室用如图装置制备并收集干燥、纯净的Cl2.已知碳酸的酸性比次氯酸的强,回答下列问题:
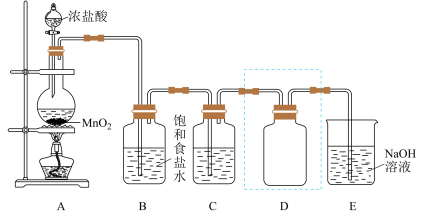
(1)装置A中发生反应的离子方程式是___________ 。
(2)装置B的作用是___________ 。
(3)装置C中盛放的物质是___________ 。
(4)装置D用于收集Cl2,装置D中进气方向为___________ (填“甲”或“乙”),若在D中放入干燥的布条,布条___________ 。(填“褪色”或“不褪色”)
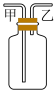
(5)装置E用于吸收尾气,E中发生反应的离子方程式是___________ 。
(6)可用Cl2和冷的石灰乳反应制备漂白粉,写出化学方程式___________ 。

(1)装置A中发生反应的离子方程式是
(2)装置B的作用是
(3)装置C中盛放的物质是
(4)装置D用于收集Cl2,装置D中进气方向为

(5)装置E用于吸收尾气,E中发生反应的离子方程式是
(6)可用Cl2和冷的石灰乳反应制备漂白粉,写出化学方程式
您最近一年使用:0次
2023-09-17更新
|
137次组卷
|
2卷引用:安徽省马鞍山市第二十二中学2022-2023学年高一上学期11月期中考试化学试题
5 . 氯气、“84”消毒液、漂白粉等都是含氯的消毒剂,某化学兴趣小组利用如图装置制备“84”消毒液、漂白粉,并收集纯净干燥的氯气。回答下列问题:
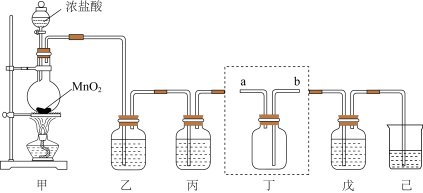
(1)装置甲中发生反应的化学方程式为___________ ,盛装浓盐酸的仪器的名称为____________ 。
(2)装置丁用来收集纯净且干燥的氯气,进气口为______________ (填a或b);装置乙和丙盛装的试剂分别是________________________ 。(填名称)
(3)将氯气通入装置己中制备“84”漂白液,则装置己中发生反应的离子方程式为______ ,有同学认为装置己还有一个作用,该作用为______ ,发挥该作用进_______ (填“能”或“不能”)用澄清石灰水代替。
(4)装置戊中盛装石灰乳用来制备漂白粉,则装置戊中发生反应的化学方程式为____________ ;漂白粉长时间暴露在空气中容易发生变质的原因为_____________ (结合化学方程式说明)。

(1)装置甲中发生反应的化学方程式为
(2)装置丁用来收集纯净且干燥的氯气,进气口为
(3)将氯气通入装置己中制备“84”漂白液,则装置己中发生反应的离子方程式为
(4)装置戊中盛装石灰乳用来制备漂白粉,则装置戊中发生反应的化学方程式为
您最近一年使用:0次
2023-09-08更新
|
298次组卷
|
2卷引用:安徽工业大学附属中学2022-2023学年高一上学期11月期中考试化学试题
名校
6 . 84消毒液是常用消毒剂,主要成分为NaClO,某化学小组在实验室制备84消毒液并探究其相关性质。回答下列问题:
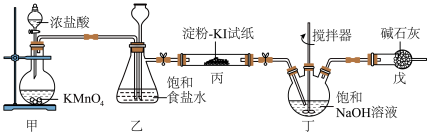
(1)装置甲中盛放浓盐酸的仪器名称是___________ ,装置甲中反应的离子方程式为___________ 。
(2)装置丙中淀粉-KI试纸变蓝,所发生反应的化学方程式为___________ 。
(3)装置丁制备 的反应中,氧化产物和还原产物的物质的量之比为1:1,若要制取
的反应中,氧化产物和还原产物的物质的量之比为1:1,若要制取 ,理论上反应中转移电子数为
,理论上反应中转移电子数为___________ 。
(4)装置戊的作用是___________ 。
(5)为了进一步研究消毒液的性质,兴趣小组向盛有2mL84消毒液的试管中,逐滴加入10%的双氧水,发现有大量的气泡产生,对此作出以下猜测。
猜测1:双氧水与消毒液发生反应产生氧气。
猜测2:……
①猜测1中反应的化学方程式为___________ ;猜测2可能为___________ 。
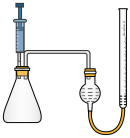
②为了验证猜想,某探究小组设计用如图装置进行实验。操作如下:在相同条件下,用注射器取等量的双氧水,分别加入盛有足量84消毒液和二氧化锰的锥形瓶中,做对照实验,若观察到___________ ,则证明猜测1正确。

(1)装置甲中盛放浓盐酸的仪器名称是
(2)装置丙中淀粉-KI试纸变蓝,所发生反应的化学方程式为
(3)装置丁制备
 的反应中,氧化产物和还原产物的物质的量之比为1:1,若要制取
的反应中,氧化产物和还原产物的物质的量之比为1:1,若要制取 ,理论上反应中转移电子数为
,理论上反应中转移电子数为(4)装置戊的作用是
(5)为了进一步研究消毒液的性质,兴趣小组向盛有2mL84消毒液的试管中,逐滴加入10%的双氧水,发现有大量的气泡产生,对此作出以下猜测。
猜测1:双氧水与消毒液发生反应产生氧气。
猜测2:……
①猜测1中反应的化学方程式为
②为了验证猜想,某探究小组设计用如图装置进行实验。操作如下:在相同条件下,用注射器取等量的双氧水,分别加入盛有足量84消毒液和二氧化锰的锥形瓶中,做对照实验,若观察到

您最近一年使用:0次
2024-01-13更新
|
142次组卷
|
2卷引用:安徽省合肥市第一中学2023-2024学年高一上学期期中考试化学试题
解题方法
7 . 水合肼( ,沸点118℃,有强还原性)是最重要的精细化工原料,实验室用次氯酸钠与尿素 [CO(NH2)2]反应制备水合肼,实验原理为
,沸点118℃,有强还原性)是最重要的精细化工原料,实验室用次氯酸钠与尿素 [CO(NH2)2]反应制备水合肼,实验原理为 。实验装置如图所示(部分装置已省略)。
。实验装置如图所示(部分装置已省略)。

回答下列问题:
(1)仪器a的名称为_______ 。
(2)装置A中发生反应的化学方程式为_______ 。
(3)装置C的作用是制备 ,反应过程中温度需控制在0℃,若温度高则易产生副产物
,反应过程中温度需控制在0℃,若温度高则易产生副产物 ,实验时可采取的控温方式为
,实验时可采取的控温方式为_______ 。反应完成后关闭K,装置B的作用为储存多余的 ,B中盛放的试剂为
,B中盛放的试剂为_______ 。
(4)将装置C中制备的溶液转移到装置D的分液漏斗中,并缓缓滴入,原因是_______ 。
(5)装置D是用蒸馏法获得水合肼( )粗品,通入冷却水的入口为
)粗品,通入冷却水的入口为_______ (填“b”或“c”)。
(6)称取 水合肼样品,加水配成
水合肼样品,加水配成 溶液,从中取出
溶液,从中取出 溶液于锥形瓶中,逐滴加入
溶液于锥形瓶中,逐滴加入 的
的 溶液,恰好完全反应时,测得消耗
溶液,恰好完全反应时,测得消耗 溶液的体积为
溶液的体积为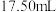 ,则样品中水合肼(
,则样品中水合肼( )的质量百分数为
)的质量百分数为_______ (已知: )。
)。
 ,沸点118℃,有强还原性)是最重要的精细化工原料,实验室用次氯酸钠与尿素 [CO(NH2)2]反应制备水合肼,实验原理为
,沸点118℃,有强还原性)是最重要的精细化工原料,实验室用次氯酸钠与尿素 [CO(NH2)2]反应制备水合肼,实验原理为 。实验装置如图所示(部分装置已省略)。
。实验装置如图所示(部分装置已省略)。
回答下列问题:
(1)仪器a的名称为
(2)装置A中发生反应的化学方程式为
(3)装置C的作用是制备
 ,反应过程中温度需控制在0℃,若温度高则易产生副产物
,反应过程中温度需控制在0℃,若温度高则易产生副产物 ,实验时可采取的控温方式为
,实验时可采取的控温方式为 ,B中盛放的试剂为
,B中盛放的试剂为(4)将装置C中制备的溶液转移到装置D的分液漏斗中,并缓缓滴入,原因是
(5)装置D是用蒸馏法获得水合肼(
 )粗品,通入冷却水的入口为
)粗品,通入冷却水的入口为(6)称取
 水合肼样品,加水配成
水合肼样品,加水配成 溶液,从中取出
溶液,从中取出 溶液于锥形瓶中,逐滴加入
溶液于锥形瓶中,逐滴加入 的
的 溶液,恰好完全反应时,测得消耗
溶液,恰好完全反应时,测得消耗 溶液的体积为
溶液的体积为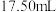 ,则样品中水合肼(
,则样品中水合肼( )的质量百分数为
)的质量百分数为 )。
)。
您最近一年使用:0次
名校
解题方法
8 . 下图是实验室模拟制备“84”消毒液的过程,其中装置和描述错误的是
| 选项 | A | B | C | D |
| 装置 | 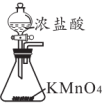 | 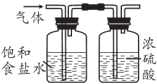 |  |  |
| 描述 | 制备 | 净化氯气 | 制备“84”消毒液 | 尾气的处理 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-11-15更新
|
225次组卷
|
3卷引用:安徽省A10联盟2022-2023学年高三上学期11月段考化学试题
9 . 有关氯气制备的装置如图所示,下列有关说法不正确的是


| A.图中气体通入浓硫酸时导管连接错误,应该是长管进气,短管出气 |
| B.可用饱和碳酸氢钠溶液代替饱和NaCl溶液 |
| C.制备氯气时,二氧化锰做氧化剂 |
| D.图中采用了向上排空气法收集氯气 |
您最近一年使用:0次
2022-09-19更新
|
1028次组卷
|
6卷引用:安徽省宿州北方中学2021-2022学年高一上学期期中考试化学试题
安徽省宿州北方中学2021-2022学年高一上学期期中考试化学试题(已下线)海水中的重要元素—钠和氯——进阶学习上海市金山中学2022-2023学年高一上学期期中考试化学试题新疆昌吉州行知学校2022-2023学年高一上学期第一次线上月考化学试题河南省开封市新世纪高级中学2022-2023学年高一上学期期末考试化学试题(已下线)【精品卷】2.2.2 氯气的制法课堂例题-人教版2023-2024学年必修第一册
名校
10 . 某小组同学研究氯及其化合物的制备和性质。
Ⅰ.氯水具有多种性质,该小组同学用氯水分别与紫色石蕊溶液, 溶液反应。完成下列问题:
溶液反应。完成下列问题:
(1)向紫色石蕊溶液中滴加氯水的现象是___________ ,证明氯水中含有的微粒有___________ 。
(2)向 溶液中滴加少量氯水,证明氯水有氧化性的实验方案为:取适量反应后溶液于试管中,先加入足量的稀盐酸,再滴加
溶液中滴加少量氯水,证明氯水有氧化性的实验方案为:取适量反应后溶液于试管中,先加入足量的稀盐酸,再滴加___________ ,若出现白色沉淀,则证明氯水具有氧化性。
Ⅱ.某学生设计下列实验装置利用 和浓盐酸制备氯气,并用氯气与潮湿的消石灰反应制取少量漂白粉(这是一个放热反应):
和浓盐酸制备氯气,并用氯气与潮湿的消石灰反应制取少量漂白粉(这是一个放热反应):

请回答下列问题:
(3)写出装置B中制取氯气的化学方程式:___________ 。
(4)漂白粉在U形管中生成,实验结果所得漂白粉 产率太低。经分析并查阅资料发现,主要原因是在U形管中存在两个副反应:
产率太低。经分析并查阅资料发现,主要原因是在U形管中存在两个副反应:
①温度较高时氯气与消石灰反应生成 ,为避免发生该反应可采取的措施是
,为避免发生该反应可采取的措施是___________ 。
②试判断另一个副反应是___________ (写出此反应的化学方程式)。为避免此副反应的发生,可采取的措施是在B、C之间连接一个盛有___________ 的洗气瓶。
Ⅰ.氯水具有多种性质,该小组同学用氯水分别与紫色石蕊溶液,
 溶液反应。完成下列问题:
溶液反应。完成下列问题:(1)向紫色石蕊溶液中滴加氯水的现象是
(2)向
 溶液中滴加少量氯水,证明氯水有氧化性的实验方案为:取适量反应后溶液于试管中,先加入足量的稀盐酸,再滴加
溶液中滴加少量氯水,证明氯水有氧化性的实验方案为:取适量反应后溶液于试管中,先加入足量的稀盐酸,再滴加Ⅱ.某学生设计下列实验装置利用
 和浓盐酸制备氯气,并用氯气与潮湿的消石灰反应制取少量漂白粉(这是一个放热反应):
和浓盐酸制备氯气,并用氯气与潮湿的消石灰反应制取少量漂白粉(这是一个放热反应):
请回答下列问题:
(3)写出装置B中制取氯气的化学方程式:
(4)漂白粉在U形管中生成,实验结果所得漂白粉
 产率太低。经分析并查阅资料发现,主要原因是在U形管中存在两个副反应:
产率太低。经分析并查阅资料发现,主要原因是在U形管中存在两个副反应:①温度较高时氯气与消石灰反应生成
 ,为避免发生该反应可采取的措施是
,为避免发生该反应可采取的措施是②试判断另一个副反应是
您最近一年使用:0次
2024-01-20更新
|
43次组卷
|
2卷引用:安徽省合肥市第三中学2023-2024学年高一上学期12月份学情调研化学试题



