名校
解题方法
1 . 某化学兴趣小组为探究Cl2的性质并制备氯水,用如图所示装置进行实验。装置Ⅲ中夹持装置已略去,其中a为干燥的品红试纸,b为湿润的品红试纸。
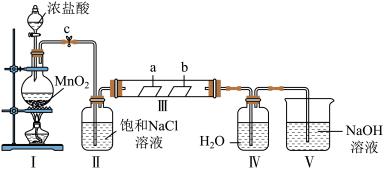
回答下列问题:
(1)加入药品前,必须先___________ 。
(2)装置Ⅰ中发生反应的化学方程式为___________ 。
(3)实验结束后,该组同学在装置Ⅲ中观察到b的红色褪去,但是并未观察到“a无明显变化”这一预期现象。为了达到这一实验目的,你认为应在___________ 和___________ (填装置序号)之间添加洗气装置,该装置的作用是___________ 。
(4)装置Ⅴ中NaOH溶液的作用是___________ ,相关反应的化学方程式为___________ 。
(5)反应完毕,为探究装置Ⅳ中溶质的成分,需要的试剂主要有___________ 。

回答下列问题:
(1)加入药品前,必须先
(2)装置Ⅰ中发生反应的化学方程式为
(3)实验结束后,该组同学在装置Ⅲ中观察到b的红色褪去,但是并未观察到“a无明显变化”这一预期现象。为了达到这一实验目的,你认为应在
(4)装置Ⅴ中NaOH溶液的作用是
(5)反应完毕,为探究装置Ⅳ中溶质的成分,需要的试剂主要有
您最近一年使用:0次
名校
2 . 某校化学兴趣小组为研究 的性质,设计如图所示装置进行实验。装置Ⅲ中夹持装置已略去,其中a为干燥的红色试纸,b为湿润的红色试纸。
的性质,设计如图所示装置进行实验。装置Ⅲ中夹持装置已略去,其中a为干燥的红色试纸,b为湿润的红色试纸。
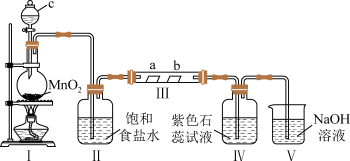
(1)装置Ⅰ中仪器c的名称是___________ ,实验室以二氧化锰和浓盐酸制备氯气的化学方程式为___________ 。
(2)装置V的作用是___________ 。
(3)若产生 足量,实验过程中装置Ⅳ中的实验现象
足量,实验过程中装置Ⅳ中的实验现象___________ 。
(4)实验结束后,该组同学在装置Ⅲ中观察到b的红色褪去,但是并未观察到“a无明显变化”这一预期现象。为了达到这一实验目的,你认为还需在图中装置Ⅱ与Ⅲ之间添加图中的___________ 装置(填序号)。
① ②
②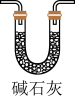 ③
③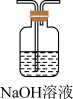 ④
④
(5)有一种“地康法”制取氯气的反应原理如图所示:
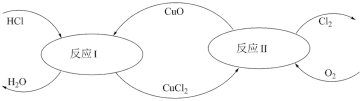
在450℃条件下,反应Ⅱ的化学方程式为___________ 。
 的性质,设计如图所示装置进行实验。装置Ⅲ中夹持装置已略去,其中a为干燥的红色试纸,b为湿润的红色试纸。
的性质,设计如图所示装置进行实验。装置Ⅲ中夹持装置已略去,其中a为干燥的红色试纸,b为湿润的红色试纸。
(1)装置Ⅰ中仪器c的名称是
(2)装置V的作用是
(3)若产生
 足量,实验过程中装置Ⅳ中的实验现象
足量,实验过程中装置Ⅳ中的实验现象(4)实验结束后,该组同学在装置Ⅲ中观察到b的红色褪去,但是并未观察到“a无明显变化”这一预期现象。为了达到这一实验目的,你认为还需在图中装置Ⅱ与Ⅲ之间添加图中的
①
 ②
② ③
③ ④
④
(5)有一种“地康法”制取氯气的反应原理如图所示:

在450℃条件下,反应Ⅱ的化学方程式为
您最近一年使用:0次
2021-11-10更新
|
154次组卷
|
2卷引用:安徽师范大学附属中学2021-2022学年高一上学期期中考查化学试题
解题方法
3 . 84消毒液是常用消毒剂,主要成分为 ,某化学小组在实验室制备84消毒液并探究其相关性质。回答下列问题:
,某化学小组在实验室制备84消毒液并探究其相关性质。回答下列问题:
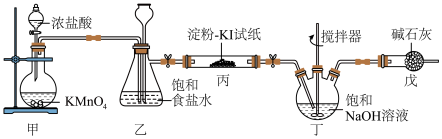
(1)装置甲中盛放浓盐酸的仪器名称是_______ 。
(2)配平方程式:_______ 。
_______MnO +_______Cl-+ _______= _______Mn2++_______Cl2↑+_______
+_______Cl-+ _______= _______Mn2++_______Cl2↑+_______
(3)装置丙中现象_______ 所发生反应的化学方程_______ 。
(4)装置丁制备 的反应中,氧化产物和还原产物的物质的量之比为1∶1,若要制取
的反应中,氧化产物和还原产物的物质的量之比为1∶1,若要制取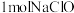 ,理论上反应中转移电子数为
,理论上反应中转移电子数为___ 。
(5)装置戊的作用是_______ 装置乙饱和食盐水作用_______ 。
 ,某化学小组在实验室制备84消毒液并探究其相关性质。回答下列问题:
,某化学小组在实验室制备84消毒液并探究其相关性质。回答下列问题:
(1)装置甲中盛放浓盐酸的仪器名称是
(2)配平方程式:
_______MnO
 +_______Cl-+ _______= _______Mn2++_______Cl2↑+_______
+_______Cl-+ _______= _______Mn2++_______Cl2↑+_______(3)装置丙中现象
(4)装置丁制备
 的反应中,氧化产物和还原产物的物质的量之比为1∶1,若要制取
的反应中,氧化产物和还原产物的物质的量之比为1∶1,若要制取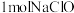 ,理论上反应中转移电子数为
,理论上反应中转移电子数为(5)装置戊的作用是
您最近一年使用:0次
4 . 已知氯气与碱反应时,产物受温度的影响。实验室中利用如图装置(部分装置省略)制备KClO3和NaClO,并探究其氧化还原性质。
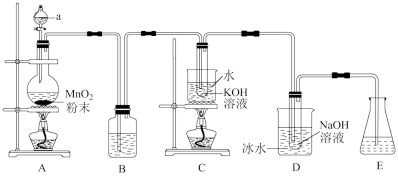
回答下列问题:
(1)仪器a的名称是___________ ;
(2)装置A产生氯气的化学方程式为___________ ;
(3)装置B中的试剂为___________ ;
(4)装置C采用的加热方式是___________ ;
(5)装置E选用试剂___________ (填标号);
A.NaCl溶液 B.NaOH溶液 C.澄清石灰水 D.稀硫酸
(6)探究KClO3、NaClO的氧化能力
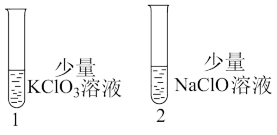
操作:向1号(KClO3)和2号(NaClO)试管中,滴加中性KI溶液。
现象:1号试管溶液颜色不变,2号试管溶液变为棕色。
结论:该条件下氧化能力KClO3___________ NaClO(填“大于”或“小于”)。

回答下列问题:
(1)仪器a的名称是
(2)装置A产生氯气的化学方程式为
(3)装置B中的试剂为
(4)装置C采用的加热方式是
(5)装置E选用试剂
A.NaCl溶液 B.NaOH溶液 C.澄清石灰水 D.稀硫酸
(6)探究KClO3、NaClO的氧化能力

操作:向1号(KClO3)和2号(NaClO)试管中,滴加中性KI溶液。
现象:1号试管溶液颜色不变,2号试管溶液变为棕色。
结论:该条件下氧化能力KClO3
您最近一年使用:0次
5 . “84”消毒液可有效灭活 2019 新型冠状病毒,某学习小组对“84”消毒液的性质展开探究。
一:制备“84”消毒液
(1)“84”消毒液的有效成分为_____ (填化学式),在实验室可用氯气和氢氧化钠溶液反应制得,其离子方程式为_________ 。
二:探究“84”消毒液的性质
I.氧化性
资料显示:洁厕灵(含盐酸)和“84”消毒液不能混合使用,否则容易产生有毒气体。利用如图装置探究上述资料的“真实性”。
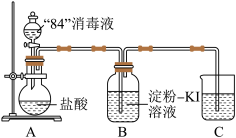
(2)盛装“84”消毒液的仪器的名称是_____ ,C 装置中可盛装_____ (填化学式)溶液。
(3)若B装置_____ (填实验现象),则证明上述资料真实可靠。
II.漂白性
(4)一定体积和浓度的“84”消毒液的漂白效率与温度的关系如图所示,已知,升高温度,NaClO可水解生成HClO的程度增大,温度高于T1℃时漂白效率降低的原因可能是_____ 。

(5)为了探究“84”消毒液的漂白效率与 pH 的关系,设计了如表所示实验:
a. 由上述实验可得出的结论是________ 。
b. 比较实验③、④和⑤,实验现象不同的主要原因是_____ 。
一:制备“84”消毒液
(1)“84”消毒液的有效成分为
二:探究“84”消毒液的性质
I.氧化性
资料显示:洁厕灵(含盐酸)和“84”消毒液不能混合使用,否则容易产生有毒气体。利用如图装置探究上述资料的“真实性”。

(2)盛装“84”消毒液的仪器的名称是
(3)若B装置
II.漂白性
(4)一定体积和浓度的“84”消毒液的漂白效率与温度的关系如图所示,已知,升高温度,NaClO可水解生成HClO的程度增大,温度高于T1℃时漂白效率降低的原因可能是

(5)为了探究“84”消毒液的漂白效率与 pH 的关系,设计了如表所示实验:
| 编号 | 3%的“84” 消毒液/ml | 0.1mol/L NaOH 溶液/ml | 0.1mol/L 盐酸溶液/ml | 5% 的 品 红 溶液/滴 | 蒸馏水/ml | 实验现象 |
| ① | 0 | 0 | 2 | 5 | 13 | 不褪色 |
| ② | 0 | 2 | 0 | 5 | 13 | 不褪色 |
| ③ | 10 | 0 | 0 | 5 | 5 | 较快褪色 |
| ④ | 10 | 2 | 0 | 5 | 3 | 缓慢褪色 |
| ⑤ | 10 | 0 | 2 | 5 | 3 | 很快褪色 |
a. 由上述实验可得出的结论是
b. 比较实验③、④和⑤,实验现象不同的主要原因是
您最近一年使用:0次
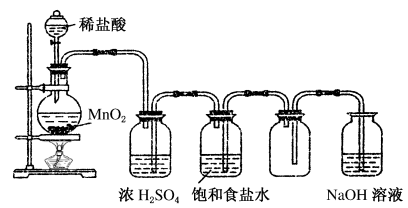
6 . 下图是某学生设计的实验室制备干燥Cl2及吸收多余氯气的实验装置图,请回答:
(1)指出上述图中的各处错误:
①_________________________________________________________ ;
②_________________________________________________________ 。
(2)在改过后的装置中,下列物质的作用分别是:
①饱和食盐水_________________________________________ ;
②浓硫酸____________________________________________ ;
③NaOH溶液_________________________________________ 。
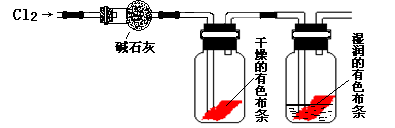
(3)甲同学设计了如下图所示的实验装置并进行实验:
①甲同学实验后并没有得到预期的实验现象,请你帮助他分析实验失败的原因_____________________ 。
②甲同学在实验失败后对设计的实验装置进行了改进,并重新进行了实验,结果得到了预期的实验现象。你认为他预期的实验现象是______________________________________ ,由此得出Cl2使有色物质褪色的机理是________ 
________________________________ ;
(4)如果将过量二氧化锰与20mL12mol/L的浓盐酸混合加热,充分反应后生成的氯气明显少于0.06mol,其主要原因有①_______________________ ,②_____________________________ 。
(5)为了提高浓盐酸的利用率,你对该实验的建议是___________________________________ 。
(6)写出圆底烧瓶中发生反应的离子方程式__________________________________________ 。
实验结束清洗仪器时,为了减少烧瓶中残留氯气对环境的污染,可以向烧瓶中加入的溶液是_________ ,有关的离子方程式是______________________________________ 。
(1)指出上述图中的各处错误:
①
②
(2)在改过后的装置中,下列物质的作用分别是:
①饱和食盐水
②浓硫酸
③NaOH溶液
(3)甲同学设计了如下图所示的实验装置并进行实验:
①甲同学实验后并没有得到预期的实验现象,请你帮助他分析实验失败的原因
②甲同学在实验失败后对设计的实验装置进行了改进,并重新进行了实验,结果得到了预期的实验现象。你认为他预期的实验现象是

(4)如果将过量二氧化锰与20mL12mol/L的浓盐酸混合加热,充分反应后生成的氯气明显少于0.06mol,其主要原因有①
(5)为了提高浓盐酸的利用率,你对该实验的建议是
(6)写出圆底烧瓶中发生反应的离子方程式
实验结束清洗仪器时,为了减少烧瓶中残留氯气对环境的污染,可以向烧瓶中加入的溶液是
您最近一年使用:0次
7 . 已知Cl2+2I-=2C1-+I2。为验证Fe3+、I2氧化性的相对强弱。某小组用下图所示装置进行实验(夹持仪器已略去,气密性已检验)。
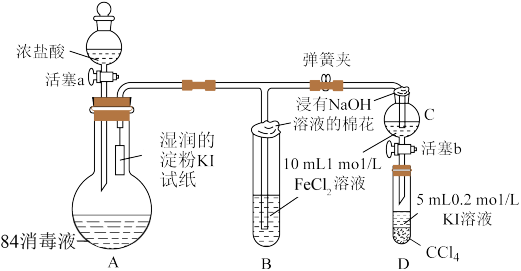
实验过程:
I.打开弹簧夹,打开活塞a,滴加浓盐酸。
II.当B和C中的溶液都变为黄色时,夹紧弹簧夹。
III.向B中加入一定量KSCN溶液,混合液显红色,关闭活塞a。
IV.打开活塞b,将C中的溶液滴入D中,关闭活塞b,取下D振荡、静置。
请回答下列问题:
(1)A中产生黄绿色气体,写出A中发生反应的离子方程式_______ 。
(2)验证氯气的氧化性强于碘单质的实验现象是_______ 。
(3)B中通入氯气溶液变黄再向B中滴加KSCN溶液,溶液变红的离子方程式是_______ 。
(4)C中的溶液滴入D中,振荡、静置,若产生_______ 现象,则说明Fe3+的氧化性强于碘单质,对应反应的离子方程式是_______ 。有人认为这个实验设计存在缺陷,其理由是_______ 。
(5)浸有氢氧化钠溶液的棉花作用是_______ 。

实验过程:
I.打开弹簧夹,打开活塞a,滴加浓盐酸。
II.当B和C中的溶液都变为黄色时,夹紧弹簧夹。
III.向B中加入一定量KSCN溶液,混合液显红色,关闭活塞a。
IV.打开活塞b,将C中的溶液滴入D中,关闭活塞b,取下D振荡、静置。
请回答下列问题:
(1)A中产生黄绿色气体,写出A中发生反应的离子方程式
(2)验证氯气的氧化性强于碘单质的实验现象是
(3)B中通入氯气溶液变黄再向B中滴加KSCN溶液,溶液变红的离子方程式是
(4)C中的溶液滴入D中,振荡、静置,若产生
(5)浸有氢氧化钠溶液的棉花作用是
您最近一年使用:0次
8 . 高铁酸钠(Na2FeO4)是一种新型绿色消毒剂,主要用于饮用水处理。如图所示物质转化关系为高铁酸钠的一种制备方法及有关性质实验(部分反应产物已略去)。已知A、F为非金属单质气体,B为常见金属单质,E为生活中最常见的调味品,F在标准状况下密度为0.090 。
。

请回答下列问题:
(1)写出D的名称___________ ,E的俗称___________ 。Na2FeO4中Fe元素的化合价为___________ 。
(2)写出反应②的离子方程式:___________ 。
(3)反应③,F在A中点燃的反应现象为:___________ 。
(4)反应④中各物质的反应比例关系如下,请填入相应的反应物和生成物的化学式,并标明电子转移的方向和数目:_____
2 +3
+3 +10NaOH =2Na2FeO4+9
+10NaOH =2Na2FeO4+9 +5H2O
+5H2O
(5)写出反应⑤的化学方程式:___________ 。
 。
。
请回答下列问题:
(1)写出D的名称
(2)写出反应②的离子方程式:
(3)反应③,F在A中点燃的反应现象为:
(4)反应④中各物质的反应比例关系如下,请填入相应的反应物和生成物的化学式,并标明电子转移的方向和数目:
2
 +3
+3 +10NaOH =2Na2FeO4+9
+10NaOH =2Na2FeO4+9 +5H2O
+5H2O(5)写出反应⑤的化学方程式:
您最近一年使用:0次
2021-11-20更新
|
1460次组卷
|
4卷引用:安徽省六安第二中学2023-2024学年高一上学期期末考试化学试题
解题方法
9 . 已知Cl2+2I=2C1-+I2为验证Fe3+、I2氧化性的相对强弱。某小组用如图所示装置进行实验(夹持仪器已略去,气密性已检验)。
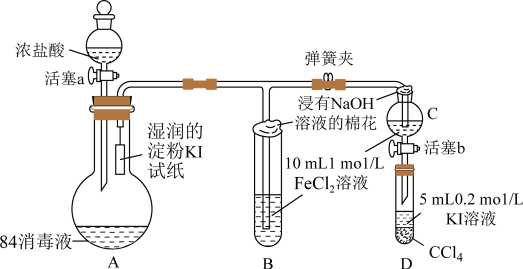
实验过程:
I.打开弹簧夹,打开活塞a,滴加浓盐酸。
II.当B和C中的溶液都变为黄色时,夹紧弹簧夹。
III.向B中加入一定量KSCN溶液,混合液显红色,关闭活塞a。
IV.打开活塞b,将C中的溶液滴入D中,关闭活塞b,取下D振荡、静置。
请回答下列问题:
(1)A中产生黄绿色气体,写出A中发生反应的离子方程式_______ 。
(2)验证氯气的氧化性强于碘单质的实验现象是_______ 。
(3)B中通入氯气溶液变黄的离子方程式是______ ;再向B中滴加KSCN溶液,溶液变红的离子方程式是_______ 。
(4)C中的溶液滴入D中,振荡、静置,若产生__________ 现象,则说明Fe3+的氧化性强于碘单质,对应反应的离子方程式是____ 。有人认为这个实验设计存在缺陷,其理由是_______ 。
(5)浸有氢氧化钠溶液的棉花作用是_______ 。

实验过程:
I.打开弹簧夹,打开活塞a,滴加浓盐酸。
II.当B和C中的溶液都变为黄色时,夹紧弹簧夹。
III.向B中加入一定量KSCN溶液,混合液显红色,关闭活塞a。
IV.打开活塞b,将C中的溶液滴入D中,关闭活塞b,取下D振荡、静置。
请回答下列问题:
(1)A中产生黄绿色气体,写出A中发生反应的离子方程式
(2)验证氯气的氧化性强于碘单质的实验现象是
(3)B中通入氯气溶液变黄的离子方程式是
(4)C中的溶液滴入D中,振荡、静置,若产生
(5)浸有氢氧化钠溶液的棉花作用是
您最近一年使用:0次
名校
10 . 实验室用如图装置制备并收集干燥、纯净的Cl2.已知碳酸的酸性比次氯酸的强,回答下列问题:
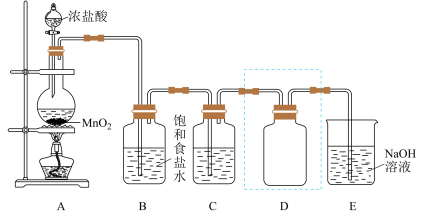
(1)装置A中发生反应的离子方程式是___________ 。
(2)装置B的作用是___________ 。
(3)装置C中盛放的物质是___________ 。
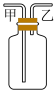
(4)装置D用于收集Cl2,装置D中进气方向为___________ (填“甲”或“乙”),若在D中放入干燥的布条,布条___________ 。(填“褪色”或“不褪色”)
(5)装置E用于吸收尾气,E中发生反应的离子方程式是___________ 。
(6)可用Cl2和冷的石灰乳反应制备漂白粉,写出化学方程式___________ 。

(1)装置A中发生反应的离子方程式是
(2)装置B的作用是
(3)装置C中盛放的物质是
(4)装置D用于收集Cl2,装置D中进气方向为

(5)装置E用于吸收尾气,E中发生反应的离子方程式是
(6)可用Cl2和冷的石灰乳反应制备漂白粉,写出化学方程式
您最近一年使用:0次
2023-09-17更新
|
137次组卷
|
2卷引用:安徽省马鞍山市第二十二中学2022-2023学年高一上学期11月期中考试化学试题



