解题方法
1 . 化学工业为疫情防控提供了强有力的物质支撑。氯的许多化合物既是重要化工原料,又是高效、广谱的灭菌消毒剂。回答下列问题:
(1)实验室制Cl2的反应中,浓盐酸所起的作用有_______ (填序号)。
①氧化性 ②还原性 ③碱性 ④酸性
(2)“84消毒液”的有效成分是NaClO,可由Cl2与NaOH溶液反应得到,其离子方程式为_______ (用离子方程式表示,)。
(3)在实验室中用二氧化锰与浓盐酸反应制备干燥纯净的氯气。进行此实验,所用仪器如图:
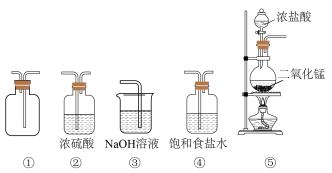
A.上述仪器的正确顺序(用序号表示):_______ ;
B.②装置中,浓硫酸的作用是_______ ;
C.⑤装置中发生反应的离子方程式为:_______ 。
(1)实验室制Cl2的反应中,浓盐酸所起的作用有
①氧化性 ②还原性 ③碱性 ④酸性
(2)“84消毒液”的有效成分是NaClO,可由Cl2与NaOH溶液反应得到,其离子方程式为
(3)在实验室中用二氧化锰与浓盐酸反应制备干燥纯净的氯气。进行此实验,所用仪器如图:

A.上述仪器的正确顺序(用序号表示):
B.②装置中,浓硫酸的作用是
C.⑤装置中发生反应的离子方程式为:
您最近一年使用:0次
2023-02-10更新
|
62次组卷
|
2卷引用:宁夏银川市贺兰县景博中学2022-2023学年高一下学期第一次质量检测化学试题
名校
解题方法
2 . 下图是实验室制备氯气并进行一系列相关实验的部分装置(夹持设备已略)。
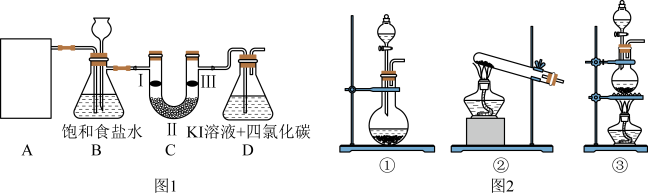
(1)实验室可以用 与浓盐酸反应制备氯气,发生反应的化学方程式为
与浓盐酸反应制备氯气,发生反应的化学方程式为_______ 。该实验中,A部分的发生装置可选图2中的_______ (填序号)。
(2)装置B中饱和食盐水的作用是_______ ;同时装置B亦是安全瓶,监测实验进行时C中是否发生堵塞,写出发生堵塞时B中的现象_______ 。
(3)装置C的实验目的是验证氯气是否具有漂白性,则C中I、Ⅱ、Ⅲ应依次放入_______ (填字母)。
(4)设计装置D的目的是比较氯、碘单质的氧化性。当向D中缓缓通入一定量氯气时,观察到D中_______ ,即可证明 氧化性大于
氧化性大于 。
。
(5)该实验装置存在明显的缺陷,应进行的改进措施是_______ (用离子方程式表示)。

(1)实验室可以用
 与浓盐酸反应制备氯气,发生反应的化学方程式为
与浓盐酸反应制备氯气,发生反应的化学方程式为(2)装置B中饱和食盐水的作用是
(3)装置C的实验目的是验证氯气是否具有漂白性,则C中I、Ⅱ、Ⅲ应依次放入
| 选项 | a | b | c | d |
| I | 干燥的有色布条 | 干燥的有色布条 | 湿润的有色布条 | 湿润的有色布条 |
| Ⅱ | 碱石灰 | 浓硫酸 | 碱石灰 | 无水氯化钙 |
| Ⅲ | 湿润的有色布条 | 湿润的有色布条 | 干燥的有色布条 | 干燥的有色布条 |
 氧化性大于
氧化性大于 。
。(5)该实验装置存在明显的缺陷,应进行的改进措施是
您最近一年使用:0次
2023-07-31更新
|
303次组卷
|
3卷引用:宁夏回族自治区银川市宁夏育才中学2023-2024学年高一上学期1月期末考试化学试题
宁夏回族自治区银川市宁夏育才中学2023-2024学年高一上学期1月期末考试化学试题陕西省汉中市2020-2021学年高一上学期期末考试化学试题(已下线)期末测试卷02-【好题汇编】备战2023-2024学年高一化学上学期期末真题分类汇编(人教版2019必修第一册)
3 . 下列叙述不正确的是
①Cl-和Cl2的性质相同
②Cl-比Cl多一个电子
③Cl2的氧化性比MnO2的强
④Cl2只有氧化性而没有还原性
①Cl-和Cl2的性质相同
②Cl-比Cl多一个电子
③Cl2的氧化性比MnO2的强
④Cl2只有氧化性而没有还原性
| A.①②④ | B.①② | C.②③④ | D.①③④ |
您最近一年使用:0次
名校
4 . 下列有关含氯物质的叙述中错误的是
| A.ClO2具有氧化性,是一种新型的消毒剂 |
| B.贮氯罐意外泄漏时,应当往高处跑 |
| C.实验室出现氯气泄露,应该用浸泡了NaOH的毛巾捂住口鼻 |
| D.氯元素主要以盐的形式存在于海水中 |
您最近一年使用:0次
名校
解题方法
5 . 氯气和漂白粉是现代工业和生活中常用的杀菌消毒剂,某兴趣小组利用所给仪器在实验室制备纯净干燥的氯气。请回答下列问题:

(1)Ⅰ中所盛试剂为_______ (填序号,下同),Ⅱ中所盛试剂为_______ 。
A.氢氧化钠溶液 B.饱和食盐水 C.浓硫酸 D.硝酸银溶液
(2)实验室用MnO2和浓盐酸加热反应制取Cl2,反应的离子方程式为_______ ,体现了浓盐酸的_______ 性和_______ 性。
(3)请按正确的顺序连接装置:H→_______、_______、→_______、_______→_______,_________ ;选择最后一个装置的目的是_______ 。
(4)实验室还可用KMnO4和浓盐酸反应制取氯气,反应原理如下:2KMnO4+l6HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O,由此反应可以推断氧化性强弱KMnO4_______ MnO2(填“>”、“<”、“=”)。
(5)写出工业制取漂白粉的化学方程式_______ 。

(1)Ⅰ中所盛试剂为
A.氢氧化钠溶液 B.饱和食盐水 C.浓硫酸 D.硝酸银溶液
(2)实验室用MnO2和浓盐酸加热反应制取Cl2,反应的离子方程式为
(3)请按正确的顺序连接装置:H→_______、_______、→_______、_______→_______,
(4)实验室还可用KMnO4和浓盐酸反应制取氯气,反应原理如下:2KMnO4+l6HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O,由此反应可以推断氧化性强弱KMnO4
(5)写出工业制取漂白粉的化学方程式
您最近一年使用:0次
名校
解题方法
6 . 图所示为利用分类法对一组物质进行的分类。回答下列问题

(1)按照分类法, 属于
属于______  填“酸性”或“碱性”
填“酸性”或“碱性” 氧化物,书写
氧化物,书写 与
与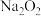 反应的化学方程式
反应的化学方程式_____________ ,依据该反应,可以说明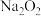
________  填“属于”或“不属于”
填“属于”或“不属于” 碱性氧化物。
碱性氧化物。
(2)上述物质中属于电解质的是_________ 。
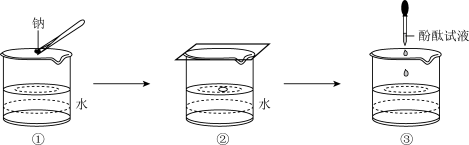
(3)某学生完成钠与水反应的实验,实验过程如图 、
、 、
、 所示,下列有关实验现象及结论的叙述
所示,下列有关实验现象及结论的叙述不正确 的是_____。 填序号
填序号
(4)工业上常用 与
与 溶液反应制取消毒液,该反应的化学方程式为
溶液反应制取消毒液,该反应的化学方程式为_________ 。
(5)向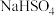 溶液中加入NaOH溶液,对应的离子方程式为
溶液中加入NaOH溶液,对应的离子方程式为_________ 。
(6)用一种试剂除去下列各物质的杂质(括号内为杂质,填写试剂名称):
CO2(HCl),试剂:___________ ; ,试剂:
,试剂:___________ 。

(1)按照分类法,
 属于
属于 填“酸性”或“碱性”
填“酸性”或“碱性” 氧化物,书写
氧化物,书写 与
与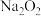 反应的化学方程式
反应的化学方程式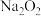
 填“属于”或“不属于”
填“属于”或“不属于” 碱性氧化物。
碱性氧化物。(2)上述物质中属于电解质的是
(3)某学生完成钠与水反应的实验,实验过程如图
 、
、 、
、 所示,下列有关实验现象及结论的叙述
所示,下列有关实验现象及结论的叙述 填序号
填序号

A.图 中钠熔成小球,说明钠与水反应放热且钠的熔点低 中钠熔成小球,说明钠与水反应放热且钠的熔点低 |
B.图 中钠四处游动并嘶嘶作响,说明反应产生了气体 中钠四处游动并嘶嘶作响,说明反应产生了气体 |
C.图 中滴加酚酞试液后溶液变红,说明有碱性物质生成 中滴加酚酞试液后溶液变红,说明有碱性物质生成 |
D.钠与水反应的离子方程式是: 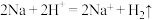 |
 与
与 溶液反应制取消毒液,该反应的化学方程式为
溶液反应制取消毒液,该反应的化学方程式为(5)向
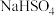 溶液中加入NaOH溶液,对应的离子方程式为
溶液中加入NaOH溶液,对应的离子方程式为(6)用一种试剂除去下列各物质的杂质(括号内为杂质,填写试剂名称):
CO2(HCl),试剂:
 ,试剂:
,试剂:
您最近一年使用:0次



