解题方法
1 . 除了上面的金属钠之外,白风还发现了以前一位学弟留下的实验报告。
只是,这实验报告怎么看着这么像数学题……?
“看来这个学弟很喜欢5啊……”
一定条件下将一定量氯气通入KOH溶液中,生成 m mol氯酸钾、n mol次氯酸钾以及其他常见物质。用NA代表阿伏加德罗常数的值:
(1)若m + n = 5,则反应中转移的电子的物质的量最大为___________ 。
(2)若m - n = 5,则反应中被还原的氯原子和被氧化的氯原子物质的量的比值的最大值为___________ 。
(3)若mn = 5,则反应中转移的电子数量最小为___________ 。
(4)若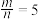 ,则反应中被还原的氯原子和被氧化的氯原子数目之比为
,则反应中被还原的氯原子和被氧化的氯原子数目之比为___________ 。
(5)我们可以用一个转化系数α来近似描述混合液的漂白性,其中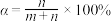 ,白风根据实验报告选用不同的温度测定了对应时刻的α,并绘制出了T-α图像:
,白风根据实验报告选用不同的温度测定了对应时刻的α,并绘制出了T-α图像:
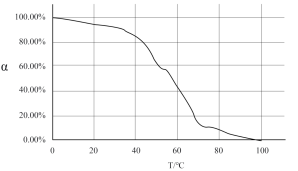
Ⅰ.由图像我们可以得出的结论是:______________________ 。
Ⅱ.试推测为什么图像会有这种趋势:______________________ 。
只是,这实验报告怎么看着这么像数学题……?
“看来这个学弟很喜欢5啊……”
一定条件下将一定量氯气通入KOH溶液中,生成 m mol氯酸钾、n mol次氯酸钾以及其他常见物质。用NA代表阿伏加德罗常数的值:
(1)若m + n = 5,则反应中转移的电子的物质的量最大为
(2)若m - n = 5,则反应中被还原的氯原子和被氧化的氯原子物质的量的比值的最大值为
(3)若mn = 5,则反应中转移的电子数量最小为
(4)若
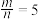 ,则反应中被还原的氯原子和被氧化的氯原子数目之比为
,则反应中被还原的氯原子和被氧化的氯原子数目之比为(5)我们可以用一个转化系数α来近似描述混合液的漂白性,其中
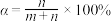 ,白风根据实验报告选用不同的温度测定了对应时刻的α,并绘制出了T-α图像:
,白风根据实验报告选用不同的温度测定了对应时刻的α,并绘制出了T-α图像:
Ⅰ.由图像我们可以得出的结论是:
Ⅱ.试推测为什么图像会有这种趋势:
您最近一年使用:0次
2 . 用图1所示装置向装有一瓶氯气的集气瓶中添加适量的蒸馏水,振荡,先利用注射器滴加 溶液,再利用注射器滴加稀盐酸,用压强传感器测得集气瓶内的压强随时间变化的曲线如图2所示。下列说法正确的是
溶液,再利用注射器滴加稀盐酸,用压强传感器测得集气瓶内的压强随时间变化的曲线如图2所示。下列说法正确的是
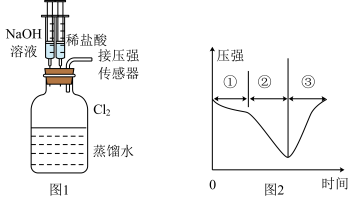
 溶液,再利用注射器滴加稀盐酸,用压强传感器测得集气瓶内的压强随时间变化的曲线如图2所示。下列说法正确的是
溶液,再利用注射器滴加稀盐酸,用压强传感器测得集气瓶内的压强随时间变化的曲线如图2所示。下列说法正确的是
| A.阶段①说明氯气溶于水,溶于水的氯气全部与水反应 |
| B.阶段②的压强变小,可利用该过程发生的反应制备漂白粉 |
C.阶段③发生反应的离子方程式为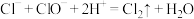 |
D.若将 换成 换成 ,则压强变化不会出现图2趋势 ,则压强变化不会出现图2趋势 |
您最近一年使用:0次
2023-11-15更新
|
437次组卷
|
2卷引用:广东省广州市黄广中学2023-2024学年高一上学期化学竞赛选拔考试
解题方法
3 . 在实验室中用二氧化锰与浓盐酸反应制备干燥纯净的氯气。进行此实验,所用仪器如图:
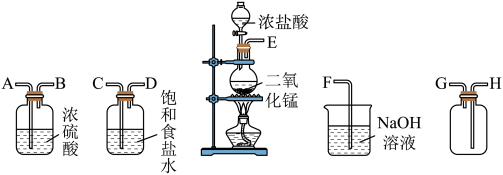
(1)上述仪器的正确连接顺序为(填各接口处的字母):___________ 。
(2)装置中,饱和食盐水的作用是___________ ;NaOH溶液的作用是___________ 。
(3)化学实验中常用湿润的淀粉碘化钾试纸检验是否有Cl2产生。如果有Cl2产生,可观察到___________ ,反应的化学方程式为___________ 。
(4)写出下列反应的化学方程式
①气体发生装置中进行反应的化学方程式:___________ ;
②NaOH溶液中发生反应的化学方程式:___________ 。
(5)实验室用10mL 12mol/L的浓盐酸和过量二氧化锰反应制取氯气,最终得到224mL的氯气(标准状况),计算该过程中氯气的产率(精确到0.01)___________ 。( )
)

(1)上述仪器的正确连接顺序为(填各接口处的字母):
(2)装置中,饱和食盐水的作用是
(3)化学实验中常用湿润的淀粉碘化钾试纸检验是否有Cl2产生。如果有Cl2产生,可观察到
(4)写出下列反应的化学方程式
①气体发生装置中进行反应的化学方程式:
②NaOH溶液中发生反应的化学方程式:
(5)实验室用10mL 12mol/L的浓盐酸和过量二氧化锰反应制取氯气,最终得到224mL的氯气(标准状况),计算该过程中氯气的产率(精确到0.01)
 )
)
您最近一年使用:0次
4 . 某实验小组以石灰粉【主要成分为 和
和 】为原料
】为原料 的流程如图所示。
的流程如图所示。

(1)“打浆”的目的是______ 。
(2)“氯化”过程控制氯气不过量,在75℃左右进行。氯化时,氯气与氢氧化钙生成次氯酸钙,次氯酸钙进一步分解为氯酸钙,少量次氯酸钙分解产生氯化钙和氧气;“氯化”温度较低时,Cl2易与 反应而生成漂白粉,写出该反应的化学方程式:
反应而生成漂白粉,写出该反应的化学方程式:______ 。露置在空气中一段时间的漂白粉,加稀盐酸后产生的气体除了可能有O2和HCl外,还可能含有______ (填化学式)。
(3)“氯化”过程中Cl2与浆水反应生成 的总反应为
的总反应为 ,反应中还原产物为
,反应中还原产物为______ (填化学式)。
(4)由于在“氯化”过程中易发生副反应,则“氯化”后溶液中
______ (填“>”、“<”或“=”)5。
 和
和 】为原料
】为原料 的流程如图所示。
的流程如图所示。
(1)“打浆”的目的是
(2)“氯化”过程控制氯气不过量,在75℃左右进行。氯化时,氯气与氢氧化钙生成次氯酸钙,次氯酸钙进一步分解为氯酸钙,少量次氯酸钙分解产生氯化钙和氧气;“氯化”温度较低时,Cl2易与
 反应而生成漂白粉,写出该反应的化学方程式:
反应而生成漂白粉,写出该反应的化学方程式:(3)“氯化”过程中Cl2与浆水反应生成
 的总反应为
的总反应为 ,反应中还原产物为
,反应中还原产物为(4)由于在“氯化”过程中易发生副反应,则“氯化”后溶液中

您最近一年使用:0次
2021-02-06更新
|
135次组卷
|
2卷引用:广东省海珠区2022-2023学年高一上学期1月化学竞赛试题
名校
解题方法
5 . 某温度下将氯气通入过量 KOH 溶液中,反应后得到 KCl、KClO 和 KClO3的混合溶液。 下列说法中,不正确的是
| A.反应消耗的Cl2与生成的 H2O 的物质的量之比始终为 1:1,与产物组成无关 |
| B.反应消耗的Cl2与 KOH 的物质的量之比取决于反应产物的组成 |
C.若n(ClO-):n( )=11:1,则反应中被还原与被氧化的氯元素的物质的量之比为 4:3 )=11:1,则反应中被还原与被氧化的氯元素的物质的量之比为 4:3 |
D.若n(ClO-):n( )=1:1,则反应消耗的氯气与转移电子数的物质的量之比为 2:3 )=1:1,则反应消耗的氯气与转移电子数的物质的量之比为 2:3 |
您最近一年使用:0次
2020-08-20更新
|
946次组卷
|
5卷引用:2017年广东和广西高中学生化学竞赛试题
2017年广东和广西高中学生化学竞赛试题河南省信阳市罗山县2020届高三毕业班第一次调研化学试题(已下线)小题必刷18 氯及其化合物——2021年高考化学一轮复习小题必刷(通用版)(已下线)押新高考卷10题 氧化还原反应-备战2022年高考化学临考题号押题(新高考通版)四川省泸县第五中学2023-2024学年高三上学期开学考试理综化学试题
名校
解题方法
6 . 大胆、科学的假设与猜想是科学探究的先导和价值所在。在下列假设(猜想)引导下的探究肯定没有意义的是
| A.探究SO2与Na2O2反应可能有Na2SO4生成 |
| B.探究Na与水的反应可能有O2生成 |
| C.探究浓硫酸与铜在一定条件下反应产生的黑色物质中可能有CuS |
| D.探究向滴有酚酞试液的NaOH溶液中通入Cl2,酚酞红色褪去的现象是溶液的酸碱性改变所致,还是HClO的漂白性所致 |
您最近一年使用:0次
2020-02-12更新
|
640次组卷
|
12卷引用:第29届(2015年)全国中学生化学竞赛(湖南省)初赛试题(A卷)
第29届(2015年)全国中学生化学竞赛(湖南省)初赛试题(A卷)2014-2015江苏省泰州市姜堰区高一上学期期末化学试卷2017届陕西省宝鸡市岐山县高三上期中化学试卷四川省雅安中学2018届高三12月月考化学试题2020届人教版本高三化学第一轮复习第十章《化学实验热点》测试卷2020届人教版高三专题基础复习专题10《化学实验热点》测试卷2020届高中化学第一轮复习第十章《化学实验热点》测试卷B上海市2016届高考化学模拟试卷(压轴卷)(已下线)上海市奉贤区2010届高三第二次模拟考试化学试题山东省邹城市兖矿第一中学2021届高三上学期9月份月考化学试题山东省济宁市兖州一中2021届高三10月月考化学试题陕西省西安市蓝田县田家炳中学大学区联考2023-2024学年高一下学期4月期中考试化学试题
7 . 某温度下,将Cl2通入NaOH溶液中,反应得到NaCl、NaClO、NaClO3的混合溶液,经测定ClO-与 的浓度之比为1∶3,则反应时被还原的氯元素与被氧化的氯元素的质量之比为
的浓度之比为1∶3,则反应时被还原的氯元素与被氧化的氯元素的质量之比为
 的浓度之比为1∶3,则反应时被还原的氯元素与被氧化的氯元素的质量之比为
的浓度之比为1∶3,则反应时被还原的氯元素与被氧化的氯元素的质量之比为 | A.4∶1 | B.3∶1 | C.11∶3 | D.21∶5 |
您最近一年使用:0次
2016-12-01更新
|
330次组卷
|
2卷引用:广东省海珠区2022-2023学年高一上学期1月化学竞赛试题



