19-20高一下·浙江·阶段练习
名校
解题方法
1 . 氮及其化合物的转化关系如下图所示,则下列说法不正确的是
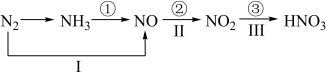
| A.路线①②③是工业生产硝酸的主要途径 | B.路线Ⅰ、Ⅱ、Ⅲ是雷电固氮生成硝酸的主要途径 |
| C.上述所有反应都是氧化还原反应 | D.氮气可在足量的氧气中通过一步反应生成 |
您最近一年使用:0次
2024-03-12更新
|
1150次组卷
|
45卷引用:考点12 氮及其化合物-备战2022年高考化学一轮复习考点帮(全国通用)
(已下线)考点12 氮及其化合物-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点12 氮及其化合物-备战2022年高考化学一轮复习考点帮(浙江专用)山东省济宁市泗水县2020-2021学年高一下学期期中考试化学试题广东省珠海市第二中学2020-2021学年高一下学期期中考试化学试题河北保定市博野县实验中学2020-2021学年高一下学期期中考试化学试题山西省怀仁市大地学校2020-2021学年高一下学期第三次月考化学试题黑龙江省宾县第二中学2020-2021学年高一下学期第二次月考化学试题江苏省镇江中学2020-2021学年高一下学期期中检测化学试题吉林省长春市第二实验中学2020-2021学年高一下学期期末考试化学试题河北省大名县第一中学2021-2022学年高二上学期开学考试化学试题江苏省常熟市2021-2022学年高二学生暑期自主学习调查化学试题(已下线)考点11 氮及其化合物-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)第12讲 氮及其化合物(练)-2023年高考化学一轮复习讲练测(新教材新高考)黑龙江省哈尔滨市第十九中学2021-2022学年高三上学期第一次月考化学试题(已下线)3.3.2 氮循环-【帮课堂】2022-2023学年高一化学同步精品讲义(沪科版2020必修第一册)广西百色民族高级中学2021-2022学年高二上学期9月月考化学试题(已下线)第四章 非金属及其化合物 第23练 硝酸 含氮化合物的转化关系(已下线)第6讲 硝酸 含氮化合物之间的转化陕西省延安市新区高级中学2021-2022学年高一上学期期末考试化学试题(已下线)【浙江新东方】双师185高一下(已下线)【期中复习】必刷题-【帮课堂】2021-2022学年高一化学同步精品讲义(人教版2019必修第二册)上海市晋元高级中学2021-2022学年高一下学期期中考试化学试题(已下线)【期末复习】必刷题(1)-【帮课堂】2021-2022学年高一化学同步精品讲义(人教版2019必修第二册)黑龙江省哈尔滨师范大学附属中学2021-2022学年高一下学期期中考试化学试题上海市同济大学第一附属中学2021-2022学年高一下学期等级阶段性测试2化学试题云南省普洱市第一中学2021-2022学年高一下学期3月份考试化学试题安徽省亳州市第二中学2021-2022学年高一下学期期末考试化学试题湖北省襄阳市第三中学2021-2022学年高一下学期期中考试化学试题江苏省盐城市响水县清源高级中学2021-2022学年高一下学期期中考试化学试题河南省周口经济开发区黄泛区高级中学2021-2022学年高一下学期第一次月考化学试题宁夏银川外国语实验学校2023届高三上学期第二次月考化学试题河南省郑州市第七高级中学2022-2023 学年高一上学期期末考试化学试题广东省茂名市电白区2021-2022学年高一下学期期中(选择性)考试化学试题广东省佛山市顺德区罗定邦中学2022-2023学年高一下学期3月第一次月考化学试题贵州省松桃民族中学2022-2023学年高一下学期3月月考化学试题广东省顺德市李兆基中学2022-2023学年高一下学期4月期中考试化学试题浙江省余姚中学2022-2023学年高一下学期期中考试 (选考)化学试题广西钦州市浦北县2022-2023学年高一下学期4月期中考试化学试题陕西省安康市2023-2024学年高二上学期开学考化学试题江苏省徐州市王杰中学2023-2024学年高一下学期第一次月考化学试题宁夏石嘴山市第三中学2023-2024学年高一下学期3月月考化学试题14 2024年苏州昆山柏庐高级中学高一3月月考广西南宁一中2023-2024学年高一下学期3月教学质量调研化学试卷福建省福州市闽侯县第一中学2023-2024学年高一下学期3月月考化学试题天津市实验中学滨海学校2023-2024学年高一下学期第一次月考化学试题
名校
2 . 在给定条件下,下列物质间的转化均能一步实现的是
A.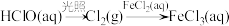 |
B.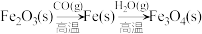 |
C.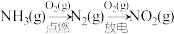 |
D.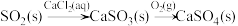 |
您最近一年使用:0次
2022-03-22更新
|
807次组卷
|
12卷引用:考向05 氧化还原反应-备战2022年高考化学一轮复习考点微专题
(已下线)考向05 氧化还原反应-备战2022年高考化学一轮复习考点微专题广东省揭阳普宁二中2021届上学期高三第三次月考化学试题广东省广州市华南师范大学附属中学2021-2022学年高三上学期第三次月考(11月)化学试题广东省肇庆市2021届高三毕业班第一次统一检测化学试卷湖南省百所学校2021-2022学年高三3月联考化学试题河北省邯郸市2022届高三下学期一模考试化学试题湖南省长沙市第一中学2021-2022学年高一下学期期中考试化学试题河北省张家口市第一中学2022届高三下学期4月月考化学试题黑龙江省哈尔滨市第六中学2021-2022学年高一下学期期中考试(选考)化学试题宁夏平罗中学2022-2023学年高三上学期第一次月考化学试题广东省开平市忠源纪念中学2022-2023学年高三上学期一轮复习阶段性检测化学试题广东省揭阳市普宁市第二中学2023-2024学年高三上学期10月期中考试化学试题
名校
解题方法
3 . 含氮化合物过多蓄积会导致水体富营养化,需将其从水体中除去,该过程称为脱氮。常用的脱氮方法有吹脱法和折点氯化法。
吹脱法:调节水体 至8左右,然后持续向水中吹入空气。
至8左右,然后持续向水中吹入空气。
折点氯化法:调节水体 至6左右,向水中加入适量
至6左右,向水中加入适量 。
。
下列分析不正确的是
吹脱法:调节水体
 至8左右,然后持续向水中吹入空气。
至8左右,然后持续向水中吹入空气。折点氯化法:调节水体
 至6左右,向水中加入适量
至6左右,向水中加入适量 。
。下列分析不正确的是
A.含氨和铵盐的水体中存在平衡: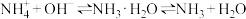 |
B.吹脱法的原理是通过鼓气降低 浓度,从而降低水中 浓度,从而降低水中 与 与 的含量 的含量 |
C.折点氯化法除 的原理为: 的原理为: |
D.吹脱法无法对含 的水体脱氮,但折点氯化法可以对含 的水体脱氮,但折点氯化法可以对含 的水体脱氮 的水体脱氮 |
您最近一年使用:0次
2021-10-19更新
|
1056次组卷
|
17卷引用:课时24 环境污染与保护-2022年高考化学一轮复习小题多维练(全国通用)
(已下线)课时24 环境污染与保护-2022年高考化学一轮复习小题多维练(全国通用)(已下线)考点24 元素与理论综合——《备战2020年高考精选考点专项突破题集》北京市北京中国人民大学附属中学2022届高三10月检测化学试卷(已下线)2022年新高考化学时事热点情境化考题---化学与文化生活(已下线)备战2022年高考化学精准检测卷【全国卷】11(已下线)章末综合评价(四)(已下线)通关练02 重要无机化合物的性质及应用-【查漏补缺】2024年高考化学复习冲刺过关(新高考专用)2020届高三化学海淀区高三第一学期期中练习北京市海淀区2019-2020学年高三期中考试化学试题湖北省龙泉中学、潜江中学2020届高三12月联考理综化学试题山东省济宁市泗水县2021届高三上学期期中考试化学试题(已下线)二轮拔高卷2-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(北京专用)天津市五校2022-2023学年高三上学期期中联考化学试题天津市咸水沽第一中学2022-2023学年高三上学期线上期末考试化学试题THUSSAT新高考地区2022年12月诊断性测试化学试题北京市交通大学附属中学2023-2024学年高一上学期12月月考化学试题 重庆市2023-2024学年高三下学期2月月度质量检测化学试题
名校
解题方法
4 . 工业上制硝酸的原理是将氨经过一系列反应得到硝酸,如下图所示:
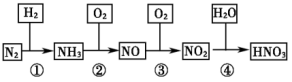
下列说法错误的是

下列说法错误的是
| A.过程①属于氮的固定 |
| B.氮气在足量氧气中也可以通过一步反应生成NO2 |
| C.过程④反应中氧化剂与还原剂的物质的量之比为1:2 |
| D.常温下可用铁质容器储存浓硝酸 |
您最近一年使用:0次
2021-08-23更新
|
1051次组卷
|
7卷引用:《新教材变化解读及考法剖析 》—第五章 化工生产中的重要非金属元素(人教版2019必修第二册)
(已下线)《新教材变化解读及考法剖析 》—第五章 化工生产中的重要非金属元素(人教版2019必修第二册)山东省聊城市2020-2021学年高一下学期期末考试化学试题江苏省淮安市车桥中学2022届高三上学期入学调研(A)化学试题(已下线)第07讲 硝酸(word讲义)-【帮课堂】2021-2022学年高一化学同步精品讲义(人教版2019必修第二册)(已下线)第05讲 硝酸(讲义)-【寒假自学课】2022年高一化学寒假精品课(人教版2019必修第二册)浙江省杭州学军中学2021-2022学年高一下学期期中考试化学试题江苏省盐城市三校(盐城一中、亭湖高中、大丰中学)2022-2023学年高一下学期期中联考化学试卷
名校
解题方法
5 . 如图是含氮化合物及单质的“类别一价态”二维图,结合二维图及氧化还原反应原理的基本规律,下列相关分析或预测错误的是
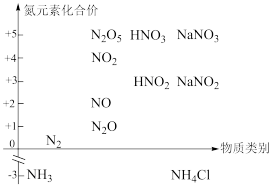
| A.硝酸具有较强的氧化性,可用稀硝酸清洗“银镜实验”后的试管 |
B. 、 、 和 和 在一定条件下均能反应,可用氨气处理氮氧化物 在一定条件下均能反应,可用氨气处理氮氧化物 |
C.可加热 和 和 制备氨气 制备氨气 |
D.联氨( )可能被亚硝酸( )可能被亚硝酸( )氧化生成氢叠氮酸 )氧化生成氢叠氮酸 |
您最近一年使用:0次
2021-07-06更新
|
541次组卷
|
4卷引用:专题01 氮元素拓展之实验大题-【微专题·大素养】备战2022年高考化学核心突破(元素拓展综合题)
(已下线)专题01 氮元素拓展之实验大题-【微专题·大素养】备战2022年高考化学核心突破(元素拓展综合题)天津市第一中学2020-2021学年高一下学期期末考试化学试题山西省晋中市平遥县第二中学校2021-2022学年高二下学期升级化学试题(已下线)专题01 硫、氮及其化合物-【好题汇编】备战2023-2024学年高一化学下学期期末真题分类汇编(天津专用)
名校
6 . 在一定温度和催化剂作用下,NO跟NH3可以发生反应生成N2和H2O。现有NO和NH3的混合物1mol,充分反应后所得产物中,经还原得到的N2比经氧化得到的N2多1.4g。已知反应的化学方程式:4NH3+6NO 5N2+6H2O,则下列说法正确的是
5N2+6H2O,则下列说法正确的是
 5N2+6H2O,则下列说法正确的是
5N2+6H2O,则下列说法正确的是| A.当转移的电子数约为3.612×1023时,则标况下有4.48L氨气被还原 |
| B.氧化产物和还原产物的物质的量比为3:2 |
| C.若以上反应进行完全,原混合物中NO与NH3的物质的量之比为可能为3:7 |
| D.若有混合物中有0.2molNH3,则参与反应的NO为0.8mol |
您最近一年使用:0次
2021-06-21更新
|
1003次组卷
|
7卷引用:考点12 氮及其化合物-备战2022年高考化学一轮复习考点帮(全国通用)
(已下线)考点12 氮及其化合物-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点12 氮及其化合物-备战2022年高考化学一轮复习考点帮(浙江专用)内蒙古鄂尔多斯市第一中学2020-2021学年高一下学期第一次月考化学试题(已下线)考点11 氮及其化合物-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)3.3.2 氮循环-【帮课堂】2022-2023学年高一化学同步精品讲义(沪科版2020必修第一册)(已下线)考点11 氮及其化合物(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)辽宁省沈阳市三十一中学2021-2022学年高一下学期4月月考化学试题
名校
7 . 研究氮及其化合物的性质,可以有效改善人类的生存环境。氮元素化合价-物质类别关系图如图
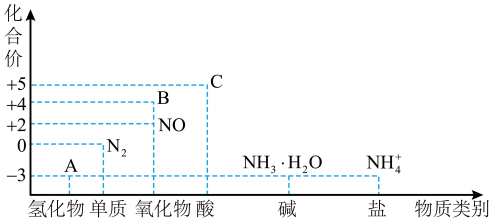
回答下列问题:
(1)在催化剂和加热的条件下,物质A生成NO是工业制硝酸的重要反应,化学方程式是_______ 。
(2)在加热条件下,物质C的浓溶液与碳单质反应,写出反应的化学方程式:_______ 。
(3)实验室中,检验溶液中含有N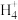 的操作方法是
的操作方法是_______ 。
(4)物质B为红棕色气体,写出该物质与水反应的离子方程式:_______ ,当反应消耗0.15 mol物质B时,转移电子的物质的量为_______ 。

回答下列问题:
(1)在催化剂和加热的条件下,物质A生成NO是工业制硝酸的重要反应,化学方程式是
(2)在加热条件下,物质C的浓溶液与碳单质反应,写出反应的化学方程式:
(3)实验室中,检验溶液中含有N
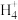 的操作方法是
的操作方法是(4)物质B为红棕色气体,写出该物质与水反应的离子方程式:
您最近一年使用:0次
2021-06-08更新
|
701次组卷
|
12卷引用:考点12 氮及其化合物-备战2022年高考化学一轮复习考点帮(全国通用)
(已下线)考点12 氮及其化合物-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点12 氮及其化合物-备战2022年高考化学一轮复习考点帮(浙江专用)黑龙江省牡丹江市海林市朝鲜族中学2020-2021学年高一5月月考化学试题(已下线)考点11 氮及其化合物-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)3.3.2 氮循环-【帮课堂】2022-2023学年高一化学同步精品讲义(沪科版2020必修第一册)第四章 非金属及其化合物 第23讲 硝酸 含氮化合物的转化关系(已下线)考点11 氮及其化合物(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)第6讲 硝酸 含氮化合物之间的转化(已下线)专题02 氮及其化合物的性质及转化(专题过关)-2022-2023学年高一化学下学期期中期末考点大串讲(人教版2019必修第二册)山东省济宁市微山县第二中学2023-2024学年高一下学期第一次月考化学试题湖南省湘楚名校2023-2024学年高一下学期期中考试化学试题(已下线)猜想03 气体的制取、无机实验探究、无机综合应用(考题猜想)-2023-2024学年高一化学下学期期末考点大串讲(人教版2019必修第二册)
名校
解题方法
8 . 一种新型的合成氨的方法如图所示.下列说法正确的是
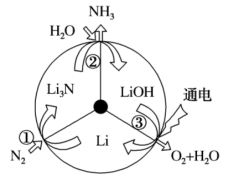

A.反应①中 发生了氧化反应 发生了氧化反应 | B.反应①和②均属于“氮的固定” |
C.反应③为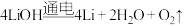 | D.三步循环的总结果为 |
您最近一年使用:0次
2021-05-22更新
|
1271次组卷
|
16卷引用:专题13 氮及其化合物 (热点讲义)-2022年高三毕业班化学常考点归纳与变式演练
(已下线)专题13 氮及其化合物 (热点讲义)-2022年高三毕业班化学常考点归纳与变式演练 贵州省贵阳、铜仁、六盘水市、黔南州2021届高三5月适应性考试(二)理综化学试题安徽省淮北市树人高级中学2020-2021学年高二下学期期末考试化学试题安徽省皖南八校2022届高三上学期摸底联考化学试题山东省潍坊市临朐县实验中学2022届高三9月摸底考试化学试题宁夏平罗中学2021-2022学年高三上学期第一次月考化学试题辽宁省沈阳市郊联体2022届高三10月月考化学试题四川省广安友谊中学2021-2022学年上学期高二10月月考化学试题河北省安平中学2021-2022学年高三上学期第二次月考化学试题江西省九校2021-2022学年高三上学期期中联考化学试题湖南省长沙市雅礼中学2023届高三上学期月考(二)化学试题安徽省亳州市蒙城第一中学东校区2022-2023学年高三上学期第四次月考化学试题安徽省/安庆市怀宁县第二中学2022-2023学年高三第二次化学月考化学试题湖南省常德市第一中学2023届高三第五次月考化学试题湖南省衡阳市第一中学2023届高三下学期第四次月考化学试题黑龙江省齐齐哈尔普高联谊校2023-2024学年高三上学期11月期中考试化学试题
名校
9 . 氨是一种重要的化工原料,主要用于化肥工业,也广泛用于硝酸、纯碱、制药等工业。实验室用加热NH4Cl和Ca(OH)2固体混合物的方法制取少量氨气。下列有关氨的说法正确的是
| A.NH3的空间构型为平面三角形 | B.NH3与H2O能形成分子间氢键 |
| C.NH3 的水溶液不能导电 | D.氨催化氧化制硝酸是利用了NH3的氧化性 |
您最近一年使用:0次
解题方法
10 . 氮氧化物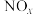 已经成为大气污染的主要污染源,其中NO的含量约占氮氧化物总含量的90%,目前选择性催化还原技术是脱除
已经成为大气污染的主要污染源,其中NO的含量约占氮氧化物总含量的90%,目前选择性催化还原技术是脱除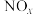 最普遍最有效的方法之一,请回答:
最普遍最有效的方法之一,请回答:
(1)实验室制取一氧化氮的化学方程式是_______ 。
(2)下列说法不正确的是_______ 。
A.上述反应的现象是铜片表面有无色气体产生,溶液由无色慢慢变蓝色
B.可通过排水法或排空气法收集一氧化氮
C.NO与 可与水反应,方程式为
可与水反应,方程式为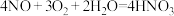 ,可用以制硝酸
,可用以制硝酸
D.工业上,氨在钯或铂催化下被氧气氧化成一氧化氮
(3)在一定温度下,利用CO为还原剂在催化剂作用下将NO脱除并转化为 和
和 ,主要的反应方程式如下:
,主要的反应方程式如下:
Ⅰ.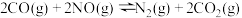
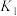
Ⅱ.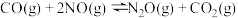
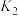
Ⅲ.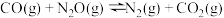

①如图是不同铈锆比例掺杂量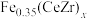 ,催化剂的催化性能结果。试分析脱除NO的最佳的催化剂样品和温度是
,催化剂的催化性能结果。试分析脱除NO的最佳的催化剂样品和温度是____ 。选择该催化剂样品的原因是____ 。


②CO、NO的起始物质的量均为1mol,反应在恒定温度和1L的密闭容器中进行,假设体系以反应Ⅰ和Ⅱ为主,达平衡时NO的转化率为80%, 的选择性为50%,则
的选择性为50%,则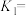
___ 。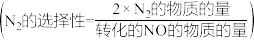
(4)已知NO可直接分解: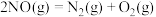 。常温常压下,该反应的平衡常数为
。常温常压下,该反应的平衡常数为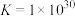 ,NO是可以分解的,但是实际上该反应是很难发生的,以碰撞理论说明原因:
,NO是可以分解的,但是实际上该反应是很难发生的,以碰撞理论说明原因:_______ 。
(5)工业上,在一定温度下,当 存在下用
存在下用 催化去除NO,会发生如下主反应:
催化去除NO,会发生如下主反应: ,
, 。下列说法不正确的是
。下列说法不正确的是_______ 。
A.通入适量 有利于主反应的发生
有利于主反应的发生
B. 量过多会限制脱除NO的活性
量过多会限制脱除NO的活性
C.当 通入过多会严重限制脱除NO的活性
通入过多会严重限制脱除NO的活性
D.气体组成中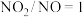 时,发生
时,发生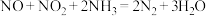
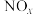 已经成为大气污染的主要污染源,其中NO的含量约占氮氧化物总含量的90%,目前选择性催化还原技术是脱除
已经成为大气污染的主要污染源,其中NO的含量约占氮氧化物总含量的90%,目前选择性催化还原技术是脱除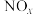 最普遍最有效的方法之一,请回答:
最普遍最有效的方法之一,请回答:(1)实验室制取一氧化氮的化学方程式是
(2)下列说法不正确的是
A.上述反应的现象是铜片表面有无色气体产生,溶液由无色慢慢变蓝色
B.可通过排水法或排空气法收集一氧化氮
C.NO与
 可与水反应,方程式为
可与水反应,方程式为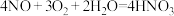 ,可用以制硝酸
,可用以制硝酸D.工业上,氨在钯或铂催化下被氧气氧化成一氧化氮
(3)在一定温度下,利用CO为还原剂在催化剂作用下将NO脱除并转化为
 和
和 ,主要的反应方程式如下:
,主要的反应方程式如下:Ⅰ.
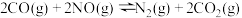
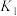
Ⅱ.
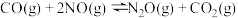
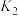
Ⅲ.
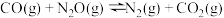

①如图是不同铈锆比例掺杂量
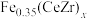 ,催化剂的催化性能结果。试分析脱除NO的最佳的催化剂样品和温度是
,催化剂的催化性能结果。试分析脱除NO的最佳的催化剂样品和温度是

②CO、NO的起始物质的量均为1mol,反应在恒定温度和1L的密闭容器中进行,假设体系以反应Ⅰ和Ⅱ为主,达平衡时NO的转化率为80%,
 的选择性为50%,则
的选择性为50%,则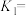
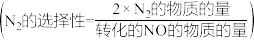
(4)已知NO可直接分解:
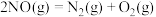 。常温常压下,该反应的平衡常数为
。常温常压下,该反应的平衡常数为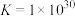 ,NO是可以分解的,但是实际上该反应是很难发生的,以碰撞理论说明原因:
,NO是可以分解的,但是实际上该反应是很难发生的,以碰撞理论说明原因:(5)工业上,在一定温度下,当
 存在下用
存在下用 催化去除NO,会发生如下主反应:
催化去除NO,会发生如下主反应: ,
, 。下列说法不正确的是
。下列说法不正确的是A.通入适量
 有利于主反应的发生
有利于主反应的发生B.
 量过多会限制脱除NO的活性
量过多会限制脱除NO的活性C.当
 通入过多会严重限制脱除NO的活性
通入过多会严重限制脱除NO的活性D.气体组成中
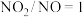 时,发生
时,发生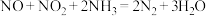
您最近一年使用:0次



