解题方法
1 . N元素的单质及其化合物之间的转化关系如图所示:
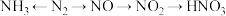
回答下列问题:
(1)N元素在元素周期表中的位置为__________ ,画出N原子结构示意图_________ 。
(2)工业上用氮气和氢气合成氨气,请写出NH3的电子式_____________ 。
(3)实验室可以利用氢氧化钙固体和氯化铵固体制备氨气,请写出该反应的化学方程式___________
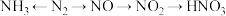
回答下列问题:
(1)N元素在元素周期表中的位置为
(2)工业上用氮气和氢气合成氨气,请写出NH3的电子式
(3)实验室可以利用氢氧化钙固体和氯化铵固体制备氨气,请写出该反应的化学方程式
您最近一年使用:0次
2 . 下图表示由元素周期表中1到20号且不同主族的元素组成的单质及化合物之间的转化关系(产物中的水已略去)。其中A为黄绿色气体单质,D有漂白性;在实验室中常用固体B和固体C加热制取刺激性气味F;F和G的组成元素相同,G与H分子所含电子数相同。

请回答
(1)单质A的组成元素在周期表中的位置是________ ;
(2)B的化学式为________ ,F的电子式为________ ,C中所含化学键类型有_______ ;
(3)写出反应②的化学方程式_____________ ;
(4)反应④中F和气体H在空气中相遇时的实验现象为__________ 写出的F一种具体用途_______________ ;
(5)向具有漂白作用的D溶液中加入H的浓溶液有A生成,其反应的离子方程式为______________ 。
(6)砷元素(As)与上述某元素处于同一主族。砷酸铅可用作杀虫剂。已知:
①在砷酸铅中,砷处于最高价态,铅处于稳定价态。
②砷酸铅是正砷酸对应的盐,1mol正砷酸分子中含有8mol原子.
砷的最高价氧化物的化学式为___________ 砷酸铅的化学式为________

请回答
(1)单质A的组成元素在周期表中的位置是
(2)B的化学式为
(3)写出反应②的化学方程式
(4)反应④中F和气体H在空气中相遇时的实验现象为
(5)向具有漂白作用的D溶液中加入H的浓溶液有A生成,其反应的离子方程式为
(6)砷元素(As)与上述某元素处于同一主族。砷酸铅可用作杀虫剂。已知:
①在砷酸铅中,砷处于最高价态,铅处于稳定价态。
②砷酸铅是正砷酸对应的盐,1mol正砷酸分子中含有8mol原子.
砷的最高价氧化物的化学式为
您最近一年使用:0次
名校
解题方法
3 . 镓是一种低熔点、高沸点的稀有金属,有“电子工业脊梁”的美誉,被广泛应用到光电子工业和微波通信工业。回答下列问题:
(1)镓 的原子结构示意图为
的原子结构示意图为 ,镓元素在元素周期表中的位置是
,镓元素在元素周期表中的位置是_______ 。
(2) 的熔点为1238℃,且熔融状态不导电,据此判断,该化合物是
的熔点为1238℃,且熔融状态不导电,据此判断,该化合物是_______ (填“共价化合物”或“离子化合物”)。
(3)已知 与
与 同周期,
同周期, 与N同主族。
与N同主族。
①用原子结构理论推测, 中
中 元素的化合价为
元素的化合价为_______ ;
②下列事实不能用元素周期律解释的是_______ (填标序号);
a.原子半径: b.热稳定性:
b.热稳定性: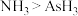
c.碱性: d.酸性:
d.酸性: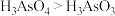
(4) 是一种直接能隙(directbandgap)的半导体,自1990年起常用在发光二极管中。一种镍催化法生产
是一种直接能隙(directbandgap)的半导体,自1990年起常用在发光二极管中。一种镍催化法生产 的工艺如图。
的工艺如图。

①“热转化”时 转化为
转化为 的化学方程式是
的化学方程式是_______ 。
②某学校化学兴趣小组在实验室利用如图装置模拟制备氮化镓:
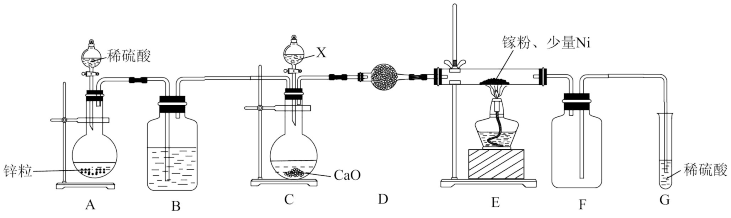
仪器X中的试剂是_______ ;加热前需先通入一段时间的 ,原因是
,原因是_______ ;装置G的作用是_______ 。
(1)镓
 的原子结构示意图为
的原子结构示意图为 ,镓元素在元素周期表中的位置是
,镓元素在元素周期表中的位置是(2)
 的熔点为1238℃,且熔融状态不导电,据此判断,该化合物是
的熔点为1238℃,且熔融状态不导电,据此判断,该化合物是(3)已知
 与
与 同周期,
同周期, 与N同主族。
与N同主族。①用原子结构理论推测,
 中
中 元素的化合价为
元素的化合价为②下列事实不能用元素周期律解释的是
a.原子半径:
 b.热稳定性:
b.热稳定性: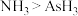
c.碱性:
 d.酸性:
d.酸性: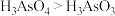
(4)
 是一种直接能隙(directbandgap)的半导体,自1990年起常用在发光二极管中。一种镍催化法生产
是一种直接能隙(directbandgap)的半导体,自1990年起常用在发光二极管中。一种镍催化法生产 的工艺如图。
的工艺如图。
①“热转化”时
 转化为
转化为 的化学方程式是
的化学方程式是②某学校化学兴趣小组在实验室利用如图装置模拟制备氮化镓:

仪器X中的试剂是
 ,原因是
,原因是
您最近一年使用:0次
解题方法
4 . 十种元素A~J在元素周期表中的相对位置如表所示:
回答下列问题:
(1)A、C元素组成的常见化合物分别为M和N,其中M含有18个电子。
①M的电子式为______ 。
②实验室制取N的化学方程式为______ 。
(2)元素C、H、J的最高价含氧酸的酸性从强到弱的顺序为______ (用相应酸的化学式表示)。
(3)不同价态的I元素可以相互转化,若反应前后存在4种价态的I元素,写出该反应的化学方程式:______ 。
(4)请用一个化学方程式证明元素D和E的非金属性强弱关系:______ 。
(5)某研究学习小组用如图装置探究F、G的金属性强弱。

当试管(Ⅰ)出现______ 的现象、且试管(Ⅱ)出现______ 的现象时,能说明金属性F大于G,写出试管(Ⅱ)依次发生反应的离子方程式:______ 、_____ 。
| 族 周期 | ⅠA | 0 | ||||||
| 1 | A | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | B | C | D | E | ||||
| 3 | F | G | H | Ⅰ | J | |||
(1)A、C元素组成的常见化合物分别为M和N,其中M含有18个电子。
①M的电子式为
②实验室制取N的化学方程式为
(2)元素C、H、J的最高价含氧酸的酸性从强到弱的顺序为
(3)不同价态的I元素可以相互转化,若反应前后存在4种价态的I元素,写出该反应的化学方程式:
(4)请用一个化学方程式证明元素D和E的非金属性强弱关系:
(5)某研究学习小组用如图装置探究F、G的金属性强弱。

当试管(Ⅰ)出现
您最近一年使用:0次
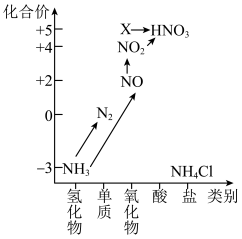
5 . 依据图中氮元素及其化合物的转化关系,回答下列问题:______ 。
(2)回答下列关于 的问题:
的问题:
①利用下列方法制氨气,其中合理的是______ (填字母)。
A.将浓氨水滴入氢氧化钠固体中
B.将氯化铵稀溶液滴入氧化钙固体中
C.将氯化铵固体加热分解
D.加热浓氨水
E.将浓氨水滴入碱石灰固体中
②氨气是重要的化工原料,可以合成多种物质,写出其催化氧化的化学方程式:______ 。
③ 、
、 合成
合成 的反应中,当分别用以下各种物质表示反应速率时,则反应速率最快的是
的反应中,当分别用以下各种物质表示反应速率时,则反应速率最快的是______ 。
A. B.
B.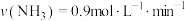
C.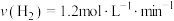 D.
D.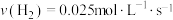
(3)下列关于NO、 的问题:
的问题:
①汽车排气管上装有催化转化器可减少尾气对环境的污染,汽车尾气中的有害气体C0和NO反应可转化为无害气体排放,写出相关反应的化学方程式:______ 。
②NO和 按一定比例混合可以被NaOH溶液完全吸收生成一种正盐,写出相关反应的化学方程式:
按一定比例混合可以被NaOH溶液完全吸收生成一种正盐,写出相关反应的化学方程式:______ 。
(2)回答下列关于
 的问题:
的问题:①利用下列方法制氨气,其中合理的是
A.将浓氨水滴入氢氧化钠固体中
B.将氯化铵稀溶液滴入氧化钙固体中
C.将氯化铵固体加热分解
D.加热浓氨水
E.将浓氨水滴入碱石灰固体中
②氨气是重要的化工原料,可以合成多种物质,写出其催化氧化的化学方程式:
③
 、
、 合成
合成 的反应中,当分别用以下各种物质表示反应速率时,则反应速率最快的是
的反应中,当分别用以下各种物质表示反应速率时,则反应速率最快的是A.
 B.
B.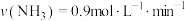
C.
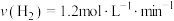 D.
D.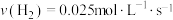
(3)下列关于NO、
 的问题:
的问题:①汽车排气管上装有催化转化器可减少尾气对环境的污染,汽车尾气中的有害气体C0和NO反应可转化为无害气体排放,写出相关反应的化学方程式:
②NO和
 按一定比例混合可以被NaOH溶液完全吸收生成一种正盐,写出相关反应的化学方程式:
按一定比例混合可以被NaOH溶液完全吸收生成一种正盐,写出相关反应的化学方程式:
您最近一年使用:0次
名校
解题方法
6 . 氨是重要的化工原料,也被认为是一种具有潜在应用前景的能源载体。
(1) 是1754年研究人员加热氯化铵和石灰的混合物时发现的,反应的化学方程式是
是1754年研究人员加热氯化铵和石灰的混合物时发现的,反应的化学方程式是___________ 。
(2)现在依然利用上述原理制取少量 ,实验室可用下图所示装置(夹持仪器略)制备并收集
,实验室可用下图所示装置(夹持仪器略)制备并收集 。
。___________ 。
②采用倒置的漏斗是为了___________ ,一段时间后向蒸馏水中滴加酚酞,溶液变红,用化学用语表示原因___________ 。
(3)由 和
和 直接合成氨是获得大量氨的主要途径。科研人员采用表面科学技术手段,从原子层面上较为清晰的揭示了该反应的微观历程,示意如下:
直接合成氨是获得大量氨的主要途径。科研人员采用表面科学技术手段,从原子层面上较为清晰的揭示了该反应的微观历程,示意如下:___________ (填“吸收能量”或“放出能量”)。
②上述过程中,形成化学键的是___________ (填过程序号)。
(4)以 和
和 为原料直接合成
为原料直接合成 能耗高。最近,我国科研人员报道了一种氯化镁循环法,可进一步降低能耗。该方法的总反应为
能耗高。最近,我国科研人员报道了一种氯化镁循环法,可进一步降低能耗。该方法的总反应为 。转化关系如下:
。转化关系如下:___________ 。
②将X与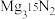 混合反应,证实了氮化镁中氮元素能转化为氨。不考虑其他副反应,产物中
混合反应,证实了氮化镁中氮元素能转化为氨。不考虑其他副反应,产物中
___________ 。
(1)
 是1754年研究人员加热氯化铵和石灰的混合物时发现的,反应的化学方程式是
是1754年研究人员加热氯化铵和石灰的混合物时发现的,反应的化学方程式是(2)现在依然利用上述原理制取少量
 ,实验室可用下图所示装置(夹持仪器略)制备并收集
,实验室可用下图所示装置(夹持仪器略)制备并收集 。
。
②采用倒置的漏斗是为了
(3)由
 和
和 直接合成氨是获得大量氨的主要途径。科研人员采用表面科学技术手段,从原子层面上较为清晰的揭示了该反应的微观历程,示意如下:
直接合成氨是获得大量氨的主要途径。科研人员采用表面科学技术手段,从原子层面上较为清晰的揭示了该反应的微观历程,示意如下:
②上述过程中,形成化学键的是
(4)以
 和
和 为原料直接合成
为原料直接合成 能耗高。最近,我国科研人员报道了一种氯化镁循环法,可进一步降低能耗。该方法的总反应为
能耗高。最近,我国科研人员报道了一种氯化镁循环法,可进一步降低能耗。该方法的总反应为 。转化关系如下:
。转化关系如下:
②将X与
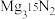 混合反应,证实了氮化镁中氮元素能转化为氨。不考虑其他副反应,产物中
混合反应,证实了氮化镁中氮元素能转化为氨。不考虑其他副反应,产物中
您最近一年使用:0次
7 . 依据图中氮元素及其化合物的转化关系,回答问题:
I.如图为氮元素的价类二维图,根据图中信息回答下列问题:_______ ,从化合价上看,X具有_______ 性(填“氧化”或“还原”)。
(2)写出工业制硝酸的反应原理_______ ,其中氧化剂与还原剂的比例为_______ 。
II.实验室采用铵盐及碱石灰制备氨气,根据下图回答下列关于NH3的问题:_______ 。
(4)下列试剂不能用于干燥NH3的是_______ (填字母)。
A.浓硫酸 B.碱石灰 C.NaOH固体
(5)氨气是重要的化工原料,可以合成多种物质,写出氨气催化氧化的化学方程式_______ 。
I.如图为氮元素的价类二维图,根据图中信息回答下列问题:

(2)写出工业制硝酸的反应原理
II.实验室采用铵盐及碱石灰制备氨气,根据下图回答下列关于NH3的问题:

(4)下列试剂不能用于干燥NH3的是
A.浓硫酸 B.碱石灰 C.NaOH固体
(5)氨气是重要的化工原料,可以合成多种物质,写出氨气催化氧化的化学方程式
您最近一年使用:0次
名校
解题方法
8 . 依据图中氮元素及其化合物的转化关系,回答问题:

(1)图中,X的化学式为______ ,从化合价上看,X具有______ (填“氧化”或“还原”)性。
(2)回答下列关于NH3的问题:
①实验室常用NH4Cl与 制取氨气,该反应的化学方程式为
制取氨气,该反应的化学方程式为____________________ 。
下列试剂能用于干燥产物的是______ (填序号)。
A.浓硫酸 B.碱石灰 C.无水氯化钙 D.五氧化二磷固体
②氨气是重要化工原料,可以合成多种物质,写出其催化氧化的化学方程式:____________________ 。
(3)回答下列关于NO、NO2的问题:
①汽车尾气中的有害气体CO和NO反应通过催化转化器可转化为无害气体排放,如果标准状况下有22.4 L CO被转化,则转移的电子数为______ 。
②NO和NO2按一定比例混合可以被NaOH溶液完全吸收,写出相关化学方程式:_______________ 。

(1)图中,X的化学式为
(2)回答下列关于NH3的问题:
①实验室常用NH4Cl与
 制取氨气,该反应的化学方程式为
制取氨气,该反应的化学方程式为下列试剂能用于干燥产物的是
A.浓硫酸 B.碱石灰 C.无水氯化钙 D.五氧化二磷固体
②氨气是重要化工原料,可以合成多种物质,写出其催化氧化的化学方程式:
(3)回答下列关于NO、NO2的问题:
①汽车尾气中的有害气体CO和NO反应通过催化转化器可转化为无害气体排放,如果标准状况下有22.4 L CO被转化,则转移的电子数为
②NO和NO2按一定比例混合可以被NaOH溶液完全吸收,写出相关化学方程式:
您最近一年使用:0次
名校
解题方法
9 . 依据图中氮元素及其化合物的转化关系,回答问题:
(1)图1中,X的化学式为________ ,从化合价上看,X具有___________ 性(填“氧化”或“还原”)。
(2)根据图2回答下列关于NH3的问题:
①实验室常用NH4Cl与Ca(OH)2制取氨气,该反应的化学方程式为________ 。
②下列试剂不能用于干燥NH3的是________ (填字母)。
A.浓硫酸 B.碱石灰 C.NaOH固体
③氨气是重要的化工原料,可以合成多种物质,写出氨气催化氧化的化学方程式________ 。
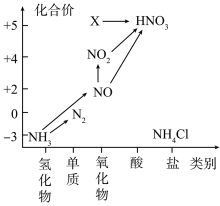
(1)图1中,X的化学式为
(2)根据图2回答下列关于NH3的问题:

①实验室常用NH4Cl与Ca(OH)2制取氨气,该反应的化学方程式为
②下列试剂不能用于干燥NH3的是
A.浓硫酸 B.碱石灰 C.NaOH固体
③氨气是重要的化工原料,可以合成多种物质,写出氨气催化氧化的化学方程式
您最近一年使用:0次
名校
10 . 依据下图中氮元素及其化合物的转化关系,回答问题:

(1)图1中, 的化学式为
的化学式为___________ ,从化合价上看, 具有
具有___________ (填“氧化性”或“还原性”)。
(2)回答下列关于 的问题:
的问题:
①实验室常用 与
与 制取氨气,该反应的化学方程式为
制取氨气,该反应的化学方程式为___________ 。
②下列试剂不能用于干燥 的是
的是___________ (填字母)。
A.浓硫酸 B.碱石灰 C. 固体 D.
固体 D. E.
E.
(3)若要收集一瓶氨气,请将上述装置补充完整,在图2虚框内画出连接图_________ 。

(4)氨气是重要的化工原料,可以合成多种物质,写出其催化氧化的化学方程式:___________ 。
(5)回答下列关于 的问题:
的问题:
①汽车排气管上装有催化转化器可减少尾气对环境的污染,汽车尾气中的有害气体 和
和 反应可转化为无害气体排放,写出相关反应的化学方程式:
反应可转化为无害气体排放,写出相关反应的化学方程式:___________ 。
② 和
和 按一定比例混合可以被
按一定比例混合可以被 溶液完全吸收,写出相关反应的化学方程式:
溶液完全吸收,写出相关反应的化学方程式:___________ 。
③工业生产中利用氨水吸收 和
和 ,原理如图所示。
,原理如图所示。

 被吸收过程的离子方程式为
被吸收过程的离子方程式为___________ 。

(1)图1中,
 的化学式为
的化学式为 具有
具有(2)回答下列关于
 的问题:
的问题:①实验室常用
 与
与 制取氨气,该反应的化学方程式为
制取氨气,该反应的化学方程式为②下列试剂不能用于干燥
 的是
的是A.浓硫酸 B.碱石灰 C.
 固体 D.
固体 D. E.
E.
(3)若要收集一瓶氨气,请将上述装置补充完整,在图2虚框内画出连接图

(4)氨气是重要的化工原料,可以合成多种物质,写出其催化氧化的化学方程式:
(5)回答下列关于
 的问题:
的问题:①汽车排气管上装有催化转化器可减少尾气对环境的污染,汽车尾气中的有害气体
 和
和 反应可转化为无害气体排放,写出相关反应的化学方程式:
反应可转化为无害气体排放,写出相关反应的化学方程式:②
 和
和 按一定比例混合可以被
按一定比例混合可以被 溶液完全吸收,写出相关反应的化学方程式:
溶液完全吸收,写出相关反应的化学方程式:③工业生产中利用氨水吸收
 和
和 ,原理如图所示。
,原理如图所示。
 被吸收过程的离子方程式为
被吸收过程的离子方程式为
您最近一年使用:0次
2023-05-27更新
|
155次组卷
|
2卷引用:河南省信阳市2022~2023学年高一下学期期中考试化学试题



