解题方法
1 . I、“侯氏制碱法”促进了我国纯碱工业的发展。该法以NaCl、 、
、 等为原料先制得
等为原料先制得 ,进而生产出纯碱,如图是模拟“侯氏制碱法”制取
,进而生产出纯碱,如图是模拟“侯氏制碱法”制取 的部分装置:
的部分装置:
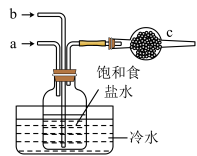
已知: 极易溶于水,溶于水时易发生溶液倒吸现象,从而导致安全隐患。
极易溶于水,溶于水时易发生溶液倒吸现象,从而导致安全隐患。
(1)下列操作说法正确的是___________。
II.某化学兴趣小组在实验室中模拟并改进侯氏制碱法制备碳酸钠的实验流程如图:
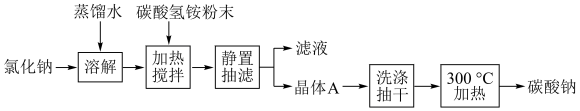
(2)“加热搅拌”中发生反应的化学方程式为___________ ,该反应属于___________ (填基本反应类型);
(3)“300℃加热”需用到的仪器除酒精灯、三角架、泥三角外,还有需要___________ (填主要仪器名称);
(4)若向 中加入过量稀NaOH溶液,所涉及的离子方程式为
中加入过量稀NaOH溶液,所涉及的离子方程式为___________ ;
(5)除去 溶液中混有的少量
溶液中混有的少量 的最佳方法是
的最佳方法是___________ 。
 、
、 等为原料先制得
等为原料先制得 ,进而生产出纯碱,如图是模拟“侯氏制碱法”制取
,进而生产出纯碱,如图是模拟“侯氏制碱法”制取 的部分装置:
的部分装置:
已知:
 极易溶于水,溶于水时易发生溶液倒吸现象,从而导致安全隐患。
极易溶于水,溶于水时易发生溶液倒吸现象,从而导致安全隐患。(1)下列操作说法正确的是___________。
A.a中先通入 ,然后b通入 ,然后b通入 ,c中放碱石灰 ,c中放碱石灰 |
B.b中先通入 ,然后a通入 ,然后a通入 ,c中放蘸有稀硫酸的脱脂棉 ,c中放蘸有稀硫酸的脱脂棉 |
C.a中先通入 ,然后b通入 ,然后b通入 ,c中放蘸有稀硫酸的脱脂棉 ,c中放蘸有稀硫酸的脱脂棉 |
D.b中先通入 ,然后a通入 ,然后a通入 ,c中放碱石灰 ,c中放碱石灰 |
II.某化学兴趣小组在实验室中模拟并改进侯氏制碱法制备碳酸钠的实验流程如图:

(2)“加热搅拌”中发生反应的化学方程式为
(3)“300℃加热”需用到的仪器除酒精灯、三角架、泥三角外,还有需要
(4)若向
 中加入过量稀NaOH溶液,所涉及的离子方程式为
中加入过量稀NaOH溶液,所涉及的离子方程式为(5)除去
 溶液中混有的少量
溶液中混有的少量 的最佳方法是
的最佳方法是
您最近一年使用:0次
名校
2 . 含氮物质是一类常见物质,在人们的生产、生活活动中有重要作用。
(1)实验室中,采用一定浓度的NaNO2溶液和NH4Cl溶液作为反应物,通过加热制备少量N2。
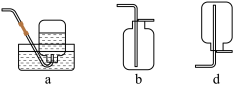
①该反应的化学方程式是_______ ,收集N2的方法是_______ (填标号)。
②实验小组同学设计以下实验探究上述反应的速率与c(NaNO2)的关系
i. V1=_______ ,V3=_______ 。
ii. 已知该反应的速率方程为 ,k为反应速率常数。根据上述实验数据,
,k为反应速率常数。根据上述实验数据,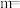
_______ (填整数)。
(2)“侯氏制碱法”是中国人的骄傲,上述实验中需用到的NH4Cl是“侯氏制碱法”的副产物。实验小组模拟“侯氏制碱法”的原理,在实验室中制备少量NaHCO3,使用的装置如下图:
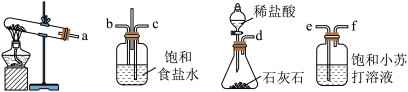
装置接口正确的连接顺序为_______ (填接口序号);由该装置可知,该实验中制备NH3需用到的试剂是_______ (填化学式)。
(3)实验小组在实验中,将1.0 mol·L-1 NaNO2溶液滴入pH=0.5的1.0 mol·L-1 FeSO4溶液中,观察到溶液为棕色,而不是预期的黄色。于是他们进行以下实验探究。
①查阅资料 常温下,[Fe(NO)]2+在溶液中能稳定存在,溶液为棕色,受热分解释放出NO。
②提出猜想 溶液的棕色来源于[Fe(NO)]2+,且[Fe(NO)]2+的颜色掩盖了Fe3+的黄色。
③设计实验、验证猜想
④实验现象及分析
i. 实验5溶液变红色,说明溶液中存在Fe3+,Fe3+的来源是_______ (写出离子方程式);
ii. 实验6观察到_______ (填实验现象),证明溶液呈棕色是因为存在[Fe(NO)]2+,且其颜色掩盖了Fe3+的黄色。
(1)实验室中,采用一定浓度的NaNO2溶液和NH4Cl溶液作为反应物,通过加热制备少量N2。

①该反应的化学方程式是
②实验小组同学设计以下实验探究上述反应的速率与c(NaNO2)的关系
| 实验编号 | 溶液体积/mL | 收集1.0mLN2所用时间/s | |||
| NaNO2溶液 | NH4Cl溶液 | 醋酸 | 水 | ||
| 1 | 4.0 | 4.0 | 4.0 | 8.0 | 334 |
| 2 | V1 | 4.0 | 4.0 | V3 | 150 |
| 3 | 8.0 | 4.0 | 4.0 | 4.0 | 83 |
| 4 | 12.0 | 4.0 | 4.0 | 0.0 | 38 |
ii. 已知该反应的速率方程为
 ,k为反应速率常数。根据上述实验数据,
,k为反应速率常数。根据上述实验数据,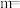
(2)“侯氏制碱法”是中国人的骄傲,上述实验中需用到的NH4Cl是“侯氏制碱法”的副产物。实验小组模拟“侯氏制碱法”的原理,在实验室中制备少量NaHCO3,使用的装置如下图:

装置接口正确的连接顺序为
(3)实验小组在实验中,将1.0 mol·L-1 NaNO2溶液滴入pH=0.5的1.0 mol·L-1 FeSO4溶液中,观察到溶液为棕色,而不是预期的黄色。于是他们进行以下实验探究。
①查阅资料 常温下,[Fe(NO)]2+在溶液中能稳定存在,溶液为棕色,受热分解释放出NO。
②提出猜想 溶液的棕色来源于[Fe(NO)]2+,且[Fe(NO)]2+的颜色掩盖了Fe3+的黄色。
③设计实验、验证猜想
| 实验编号 | 5 | 6 |
| 操作方法 | 取上述滴有NaNO2溶液的棕色混合液,向其中滴加稀KSCN溶液 | 取上述棕色混合液,按下图所示加热 |
i. 实验5溶液变红色,说明溶液中存在Fe3+,Fe3+的来源是
ii. 实验6观察到
您最近一年使用:0次
解题方法
3 . 下列实验设计能达到实验目的的是
| 选项 | 实验目的 | 实验设计 |
| A | 制备NO | 将铜丝插入浓硝酸中 |
| B | 鉴别NaBr和KI溶液 | 分别加新制氯水后再用CCl4萃取 |
| C | 证明碳的非金属性比硅的强 | 将盐酸与石灰石反应产生的气体直接通入硅酸钠溶液中 |
| D | 检验某盐中是否含 | 向盛某盐溶液的试管中滴入氢氧化钠溶液后,观察试管口处湿润的蓝色石蕊试纸是否变红 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-03-22更新
|
1040次组卷
|
2卷引用:江苏省徐州市2022-2023学年高一下学期期中考试化学试题
4 . 利用如图所示装置(夹持装置略)进行实验,b中现象不能证明a中产物生成。( )
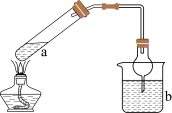

| 装置a中反应 | b中检测试剂及现象 |
| 浓NaOH与NH4Cl溶液生成NH3 | 酚酞溶液变红 |
您最近一年使用:0次
名校
5 . 用如图装置(搅拌装置略)探究溶液离子浓度变化,灯光变化不可能 出现“亮→暗(或灭)→亮”现象的是
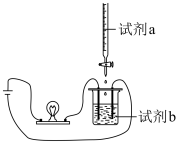

| 选项 | A | B | C | D |
| 试剂a |  |  |  |  |
| 试剂b |  | 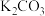 |  |  |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
6 . 过二硫酸钠( ,其中S的化合价为
,其中S的化合价为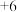 )是白色品状粉末,易溶于水,加热至较高温度时发生分解,常用作漂白剂、金属表面处理剂等。某化学小组在实验室对过二硫酸钠的制备和成品含量测定进行探究。已知:
)是白色品状粉末,易溶于水,加热至较高温度时发生分解,常用作漂白剂、金属表面处理剂等。某化学小组在实验室对过二硫酸钠的制备和成品含量测定进行探究。已知: 。
。
回答下列问题:
(1)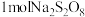 中含有的过氧键(
中含有的过氧键( 键)数目为
键)数目为_______ 。
(2)①在 下,以过二硫酸铵
下,以过二硫酸铵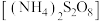 溶液和
溶液和 溶液为原料采用“复分解法”制备过二硫酸钠,装置如图所示(部分夹持仪器已略去)。
溶液为原料采用“复分解法”制备过二硫酸钠,装置如图所示(部分夹持仪器已略去)。
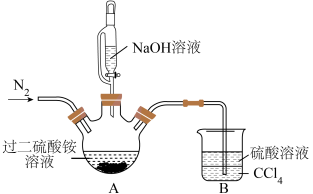
有关反应的化学方程式为_______ ,装置A的适宜加热方式为_______ 。
②装置B的作用是_______ ,反应过程中需要持续通入 的主要原因是
的主要原因是_______ 。
(3)由过二硫酸钠溶液经过减压蒸发浓缩、冷却结晶、干燥等操作即可得到过二硫酸钠晶体,采用“减压蒸发浓缩”的原因是_______ 。
(4)过二硫酸钠成品的含量可用“碘量法”测得。称取 试样,置于碘量瓶中,移取足量的
试样,置于碘量瓶中,移取足量的 溶液于其中,并加入少量乙酸溶液,密闭,在暗处放置
溶液于其中,并加入少量乙酸溶液,密闭,在暗处放置 ,生成的
,生成的 用
用 硫代硫酸钠标准溶液滴定,有关反应为
硫代硫酸钠标准溶液滴定,有关反应为 。达到滴定终点时平均消耗标准溶液的体积为
。达到滴定终点时平均消耗标准溶液的体积为 ,则滴定中选用的指示剂为
,则滴定中选用的指示剂为_______ ,成品中过二硫酸钠的含量为_______  (用含m、V的代数式表示,需化简)。
(用含m、V的代数式表示,需化简)。
 ,其中S的化合价为
,其中S的化合价为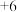 )是白色品状粉末,易溶于水,加热至较高温度时发生分解,常用作漂白剂、金属表面处理剂等。某化学小组在实验室对过二硫酸钠的制备和成品含量测定进行探究。已知:
)是白色品状粉末,易溶于水,加热至较高温度时发生分解,常用作漂白剂、金属表面处理剂等。某化学小组在实验室对过二硫酸钠的制备和成品含量测定进行探究。已知: 。
。回答下列问题:
(1)
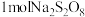 中含有的过氧键(
中含有的过氧键( 键)数目为
键)数目为(2)①在
 下,以过二硫酸铵
下,以过二硫酸铵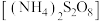 溶液和
溶液和 溶液为原料采用“复分解法”制备过二硫酸钠,装置如图所示(部分夹持仪器已略去)。
溶液为原料采用“复分解法”制备过二硫酸钠,装置如图所示(部分夹持仪器已略去)。
有关反应的化学方程式为
②装置B的作用是
 的主要原因是
的主要原因是(3)由过二硫酸钠溶液经过减压蒸发浓缩、冷却结晶、干燥等操作即可得到过二硫酸钠晶体,采用“减压蒸发浓缩”的原因是
(4)过二硫酸钠成品的含量可用“碘量法”测得。称取
 试样,置于碘量瓶中,移取足量的
试样,置于碘量瓶中,移取足量的 溶液于其中,并加入少量乙酸溶液,密闭,在暗处放置
溶液于其中,并加入少量乙酸溶液,密闭,在暗处放置 ,生成的
,生成的 用
用 硫代硫酸钠标准溶液滴定,有关反应为
硫代硫酸钠标准溶液滴定,有关反应为 。达到滴定终点时平均消耗标准溶液的体积为
。达到滴定终点时平均消耗标准溶液的体积为 ,则滴定中选用的指示剂为
,则滴定中选用的指示剂为 (用含m、V的代数式表示,需化简)。
(用含m、V的代数式表示,需化简)。
您最近一年使用:0次
2022-11-10更新
|
500次组卷
|
3卷引用:四川省内江市第二中学2023-2024学年高三上学期12月月考理综试题
四川省内江市第二中学2023-2024学年高三上学期12月月考理综试题山西省太原市2022-2023学年高三上学期期中质量监测化学试卷(已下线)化学(全国甲卷理综A卷)-学易金卷:2023年高考第一次模拟考试卷



