1 . (1)实验室中的Na2SiO3溶液长期放置,瓶底会出现白色沉淀,则形成沉淀的离子方程式是___________ 。取瓶中的上层清液加入稀盐酸,观察到既有气泡产生又有沉淀生成,其离子方程式分别为___________ , ___________ 。
(2)硫有一些特殊的化学性质,从而决定了在生活中特殊的用途。例如硫单质易与不活泼金属汞、银化合,在家庭、医务室等场所不小心有水银温度计打碎而有汞撒落的时候,可用硫粉处理。
①请写出硫粉与汞的反应方程式___________ 。
②某次实验后试管内壁上粘附有一些硫晶体,除去的方法是___________ 。
(3)将浓H2SO4表现的性质填入横线内。
A.酸性 B.强氧化性 C.脱水性 D.吸水性
①用磷矿粉[主要成分Ca3(PO4)2]和硫酸反应制磷酸_____
②热的浓硫酸与铜片反应___
③浓H2SO4不能干燥NH3、H2S、HI等气体____
④浓H2SO4能吸收H2或SO2气体中的水分____
⑤浓硫酸使湿润的蓝色石蕊试纸先变红后变黑____
(2)硫有一些特殊的化学性质,从而决定了在生活中特殊的用途。例如硫单质易与不活泼金属汞、银化合,在家庭、医务室等场所不小心有水银温度计打碎而有汞撒落的时候,可用硫粉处理。
①请写出硫粉与汞的反应方程式
②某次实验后试管内壁上粘附有一些硫晶体,除去的方法是
(3)将浓H2SO4表现的性质填入横线内。
A.酸性 B.强氧化性 C.脱水性 D.吸水性
①用磷矿粉[主要成分Ca3(PO4)2]和硫酸反应制磷酸
②热的浓硫酸与铜片反应
③浓H2SO4不能干燥NH3、H2S、HI等气体
④浓H2SO4能吸收H2或SO2气体中的水分
⑤浓硫酸使湿润的蓝色石蕊试纸先变红后变黑
您最近一年使用:0次
名校
解题方法
2 . 把硫和强碱(如NaOH)加热至沸,反应后,硫转化为S2-和SO ,则反应的S和生成的S2-、SO
,则反应的S和生成的S2-、SO 的物质的量之比为
的物质的量之比为
 ,则反应的S和生成的S2-、SO
,则反应的S和生成的S2-、SO 的物质的量之比为
的物质的量之比为| A.2:1:1 | B.3:2:1 | C.3:1:2 | D.4:1:3 |
您最近一年使用:0次
名校
解题方法
3 . 关于硫的叙述正确的是
| A.硫单质质脆,微溶于酒精和二硫化碳 |
| B.硫的非金属性较强,在自然界中只以化合态存在 |
| C.硫单质与金属单质或非金属单质反应时都作氧化剂 |
| D.从硫的化合价角度分析,单质硫既具有氧化性又具有还原性 |
您最近一年使用:0次
2021-04-08更新
|
515次组卷
|
2卷引用:重庆市巴蜀中学2020-2021学年高一3月月考化学试题
名校
4 . X、Y、Z、W是原子序数依次增大的短周期元素,且互不同族;其中只有两种为金属,X原子的最外层电子数与次外层电子数相等;X与W、Y与Z这两对原子的最外层电子数之和均为9,单质Y和W都可与浓的NaOH溶液反应。请回答下列问题:
(1)R与W同主族,且半径小于W,则R与水反应的化学方程式___________ ;
(2)X与Y化学性质相似,则单质X与浓的NaOH溶液反应的化学方程式是___________ ;
(3)Z的单质与NaOH溶液反应的离子方程式是___________ ;
(4)0.1 mol的单质W与50 mL 1.5 mol/L的FeBr2溶液反应,则被氧化的Fe2+和Br-的物质的量之比是___________ 。
(1)R与W同主族,且半径小于W,则R与水反应的化学方程式
(2)X与Y化学性质相似,则单质X与浓的NaOH溶液反应的化学方程式是
(3)Z的单质与NaOH溶液反应的离子方程式是
(4)0.1 mol的单质W与50 mL 1.5 mol/L的FeBr2溶液反应,则被氧化的Fe2+和Br-的物质的量之比是
您最近一年使用:0次
20-21高一下·全国·课时练习
名校
解题方法
5 . 下列说法中不正确的是( )
| A.在自然界中有游离态的硫存在 |
| B.试管内壁的硫粉可以用热的碱液除去 |
| C.硫与金属反应,生成低价态的金属化合物 |
| D.硫的氧化性比氯气的强 |
您最近一年使用:0次
2021-03-08更新
|
697次组卷
|
4卷引用:5.1.1 硫与二氧化硫(练好题)(基础过关)-2020-2021学年高一化学新教材新理念新设计同步课堂(人教2019必修第二册)
(已下线)5.1.1 硫与二氧化硫(练好题)(基础过关)-2020-2021学年高一化学新教材新理念新设计同步课堂(人教2019必修第二册)海南省儋州市第二中学2020-2021学年高一下学期3月月考化学试题河北省石家庄市元氏县第四中学2021-2022学年高一下学期月考化学试题天津市南开中学2022-2023学年高一下学期3月月考化学试题
名校
解题方法
6 . A是中学化学中常见的单质,B、C为化合物。它们有如图所示的转化关系(部分产物及反应条件省略)。下列判断正确的是


| A.A、B、C含有一种相同的元素 |
| B.A可能是金属,也可能是非金属 |
| C.A对应氧化物的水化物为强酸 |
| D.反应①②互为可逆反应 |
您最近一年使用:0次
2021-02-16更新
|
713次组卷
|
2卷引用:(人教版2019)必修第二册 第五章 化工生产中的重要非金属元素 第一节 硫及其化合物
真题
名校
7 . 玻璃仪器内壁残留的硫单质可用热KOH溶液洗涤除去,发生如下反应:
3S+6KOH 2K2S+K2SO3+3H2O
2K2S+K2SO3+3H2O
(x-1)S+K2S K2Sx(x=2~6)
K2Sx(x=2~6)
S+ K2SO3 K2S2O3
K2S2O3
请计算:
(1)0.480 g硫单质与V mL 1.00 mol·L-1热KOH溶液恰好完全反应,只生成K2S和K2SO3,则V=______ 。
(2)2.560 g硫单质与60.0 mL 1.00 mol·L-1热KOH溶液恰好完全反应,只生成K2Sx和K2S2O3,则x=______ 。(写出计算过程)
3S+6KOH
 2K2S+K2SO3+3H2O
2K2S+K2SO3+3H2O(x-1)S+K2S
 K2Sx(x=2~6)
K2Sx(x=2~6)S+ K2SO3
 K2S2O3
K2S2O3请计算:
(1)0.480 g硫单质与V mL 1.00 mol·L-1热KOH溶液恰好完全反应,只生成K2S和K2SO3,则V=
(2)2.560 g硫单质与60.0 mL 1.00 mol·L-1热KOH溶液恰好完全反应,只生成K2Sx和K2S2O3,则x=
您最近一年使用:0次
2021-01-09更新
|
4066次组卷
|
12卷引用:2021年1月新高考浙江化学高考真题
2021年1月新高考浙江化学高考真题(已下线)解密02 物质的量(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(已下线)解密02 物质的量(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)(已下线)考向02 物质的量浓度及其相关计算-备战2022年高考化学一轮复习考点微专题(已下线)专题18.化学计算-十年(2012-2021)高考化学真题分项汇编(浙江专用)(已下线)2021年1月浙江高考化学试题变式题26-31(已下线)解密02 物质的量(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)解密02 物质的量(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)浙江省金华市曙光学校2021-2022学年高三下学期5月模拟考试化学试题浙江省宁波市北仑中学2022-2023学年高一下学期期初返校考试化学(学考)试题(已下线)专题03 阿伏加德罗常数与化学计算 -2023年高考化学真题题源解密(新高考专用)浙江省宁波市鄞州中学(宁波鄞州蓝青高级中学)2023-2024学年高一上学期12月月考化学学科试题
名校
解题方法
8 . 实验室中下列做法错误的是
| A.粘在试管内壁的硫粉,可用热的NaOH溶液洗涤 |
| B.测定硫酸铜晶体结晶水含量时,灼烧后的坩埚置于干燥器中冷却,再称量 |
| C.稀释浓硫酸时,即便戴有防护眼罩,也不能把水倒入装有浓硫酸的烧杯中 |
| D.用镊子取绿豆粒大小的钠迅速投入盛有10mL水(含酚酞)的试管中,观察现象 |
您最近一年使用:0次
解题方法
9 . 一种由氯气与熔化的硫反应制取 的装置(夹持和加热装置已省略)如图所示:
的装置(夹持和加热装置已省略)如图所示:

已知:① 和
和 反应生成
反应生成 ,同时有少量
,同时有少量 及其他氯化物生成。
及其他氯化物生成。
②常温下, 是一种浅黄色的油状液体,极易水解。
是一种浅黄色的油状液体,极易水解。
③ 的沸点为
的沸点为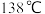 ,
, 的沸点为
的沸点为 ,硫的熔点为
,硫的熔点为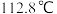 、沸点为
、沸点为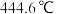 。
。
回答下列问题:
(1)实验过程中,从装置 中逸出的气体为
中逸出的气体为___________ (填化学式),装置 中盛放的试剂是
中盛放的试剂是___________ 。
(2)对装置 进行加热的合适方式是
进行加热的合适方式是___________ (填标号)。
(3)装置D中的错误之处是___________ (写一处即可)。
(4)装置F的作用是___________ (写一点即可)。
(5)纯化 :向粗产品中加入
:向粗产品中加入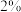 的单质硫和
的单质硫和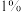 的活性炭,后续操作是
的活性炭,后续操作是________ 。
(6)取约 于试管中,滴入少量水,试管口放湿润的品红试纸,发现试管口有白雾,品红试纸褪色,试管中有淡黄色固体生成,该反应的化学方程式为
于试管中,滴入少量水,试管口放湿润的品红试纸,发现试管口有白雾,品红试纸褪色,试管中有淡黄色固体生成,该反应的化学方程式为___________ 。
(7)实验结束时,装置C中烧瓶底部有少量硫附着,可用热的NaOH浓溶液洗涤,已知产物之一为Na2S2O3,该反应的离子方程式为___________________________ 。
 的装置(夹持和加热装置已省略)如图所示:
的装置(夹持和加热装置已省略)如图所示:
已知:①
 和
和 反应生成
反应生成 ,同时有少量
,同时有少量 及其他氯化物生成。
及其他氯化物生成。②常温下,
 是一种浅黄色的油状液体,极易水解。
是一种浅黄色的油状液体,极易水解。③
 的沸点为
的沸点为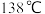 ,
, 的沸点为
的沸点为 ,硫的熔点为
,硫的熔点为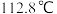 、沸点为
、沸点为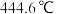 。
。回答下列问题:
(1)实验过程中,从装置
 中逸出的气体为
中逸出的气体为 中盛放的试剂是
中盛放的试剂是(2)对装置
 进行加热的合适方式是
进行加热的合适方式是| 选项 | A | B | C | D |
| 加热方式 | 水浴 | 甘油浴 | 沙浴 | 锡浴 |
极限温度/ | 98 | 220 | 400 | 600 |
(4)装置F的作用是
(5)纯化
 :向粗产品中加入
:向粗产品中加入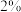 的单质硫和
的单质硫和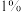 的活性炭,后续操作是
的活性炭,后续操作是(6)取约
 于试管中,滴入少量水,试管口放湿润的品红试纸,发现试管口有白雾,品红试纸褪色,试管中有淡黄色固体生成,该反应的化学方程式为
于试管中,滴入少量水,试管口放湿润的品红试纸,发现试管口有白雾,品红试纸褪色,试管中有淡黄色固体生成,该反应的化学方程式为(7)实验结束时,装置C中烧瓶底部有少量硫附着,可用热的NaOH浓溶液洗涤,已知产物之一为Na2S2O3,该反应的离子方程式为
您最近一年使用:0次
10 . 单质硫在NaOH的热溶液中发生歧化反应:3S+6NaOH=2Na2S+Na2SO3+3H2O。若硫过量,进一步生成Na2Sx(x≤5)和Na2S2O3。将2.56g硫与含0.06mol NaOH的热溶液充分反应恰好生成amol Na2Sx和bmol Na2S2O3,再加入足量NaClO-NaOH的混合溶液,硫元素全部转化为Na2SO4,转移电子nmol。则以下正确的是
| A.2a =b | B.x=2 | C.n=0.48 | D.b=0.02 |
您最近一年使用:0次
2020-11-19更新
|
1307次组卷
|
4卷引用:广东省深圳外国语学校2021届高三第二次月考化学试题



