解题方法
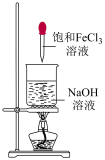
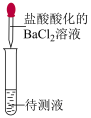
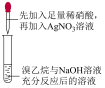
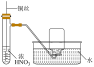
1 . 下列实验能达到对应目的的是
| 选项 | A | B | C | D |
| 实验 |
|
|
|
|
| 目的 | 制备Fe(OH)3 胶体 | 检验待测液中 是否含有  | 检验溴乙烷中的 溴元素 | 制备并收集NO2 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2 . 下列“实验结论”与“实验操作及现象”不相符 的一组是
选项 | 实验操作及现象 | 实验结论 |
A | 向某溶液中加入盐酸,产生能使澄清石灰水变浑浊的气体 | 该溶液中一定含有 |
| 向紫色石蕊溶液中加入氯水,溶液先变红,随后褪色 | 氯水中含有酸性物质和漂白性物质 |
C | 向某溶液中加入浓 溶液,加热,产生能使湿润的红色石蕊试纸变蓝的气体 溶液,加热,产生能使湿润的红色石蕊试纸变蓝的气体 | 该溶液中一定含有 |
D | 向某溶液中加入足量稀盐酸,无明显现象,再加入 溶液,有白色沉淀产生 溶液,有白色沉淀产生 | 该溶液中一定含有 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
3 . 下列物质的检验中,操作、现象与结论均正确的是
| A.向Na2SO3溶液中加入硝酸酸化的BaCl2溶液,产生白色沉淀,证明Na2SO3溶液已变质 |
B.向某溶液中加入浓NaOH溶液并加热,用湿润的蓝色石蕊试纸检验产生的气体,若试纸变红,该溶液中含有NH |
C.向某溶液中加入盐酸,产生能使澄清石灰水变浑浊的气体,该溶液中含有CO |
| D.向某溶液中加入NaOH溶液,产生白色沉淀,迅速变成灰绿色,最终变为红褐色,该溶液中含有Fe2+ |
您最近半年使用:0次
名校
解题方法
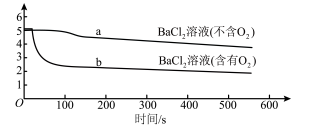
4 . 分别向等体积的不含O2、含有O2的0.1mol/L BaCl2溶液中通入SO2,探究体系中物质间的相互作用,实验记录如下。(已知:pH越小,溶液酸性越强)
下列说法不正确的是
下列说法不正确的是
pH变化 |
|
溶液中是否产生沉淀 | 不含O2的BaCl2溶液中没有白色沉淀, 含有O2的BaCl2溶液中产生白色沉淀。 |
| A.a所示溶液的pH降低的原因:SO2与H2O反应生成H2SO3,溶液的c(H+)增大 |
B.b所示溶液中发生反应: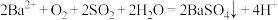 |
| C. SO2通入不含O2的BaCl2溶液后,再加入NaOH溶液,产生BaSO3沉淀 |
D.b比a所示溶液的pH小的原因: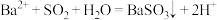 |
您最近半年使用:0次
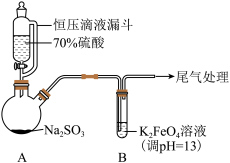
5 . 某实验小组探究SO2与K2FeO4的反应,实验如下。
资料:i.K2FeO4为紫色固体,微溶于KOH溶液;具有强氧化性,在酸性或中性溶液中快速产生O2,在碱性溶液中较稳定。
ii.Fe3+可以与C2O 形成[Fe(C2O4)3]3-;
形成[Fe(C2O4)3]3-;
(1)A中产生SO2的化学方程式为___________ 。
(2)暗红褐色沉淀X可能含Fe3+、OH-、SO 、SO
、SO ,检验如下:
,检验如下:
实验二:向X中加入足量盐酸,沉淀溶解。取少量溶液,滴加KSCN溶液后变红。证明溶液中存在___________ 。另取少量溶液滴加BaCl2溶液,产生白色沉淀,但不能确认含有SO ,原因是
,原因是___________ 。
实验三:向X中加入H2C2O4溶液,沉淀溶解。继续滴加BaCl2溶液,产生白色沉淀,过滤后,向沉淀中加入盐酸,白色沉淀溶解。确认X中不含SO 。
。
实验三中用H2C2O4溶液溶解沉淀的目的是:___________ 。
实验四:向X中加入足量盐酸,沉淀溶解。加入几滴碘水(含淀粉),蓝色立即褪去。静置,一段时间后蓝色复现,振荡,不褪色。
结合离子方程式解释沉淀溶解后的现象:___________ 。
(3)查阅资料:a.Fe3+、SO 、H2O(或OH﹣)会形成配合物HOFeOSO2。
、H2O(或OH﹣)会形成配合物HOFeOSO2。 和O2在金属离子的催化作用下产生具有强氧化性的过一硫酸(HSO
和O2在金属离子的催化作用下产生具有强氧化性的过一硫酸(HSO
①向溶液Y中滴加2滴KSCN溶液,未见红色;再加几滴6mol·L-1盐酸,溶液变红。溶液Y中存在Fe(Ⅲ),但直接滴加KSCN溶液未见红色的原因是___________ 。
②取出部分实验一中的橙色溶液,久置不褪色。结合资料a中过程ii分析实验一中溶液最终“几乎无色”的原因:___________ 。
总结:SO2与K2FeO4发生了氧化还原反应和复分解反应,并且遵循化学反应速率和限度规律。
资料:i.K2FeO4为紫色固体,微溶于KOH溶液;具有强氧化性,在酸性或中性溶液中快速产生O2,在碱性溶液中较稳定。
ii.Fe3+可以与C2O
 形成[Fe(C2O4)3]3-;
形成[Fe(C2O4)3]3-;| 装置 | 操作及现象 |
| 实验一:向B中通入SO2,产生暗红褐色沉淀X和溶液Y(略显红色);继续通入SO2一段时间后,溶液呈红色,继而变为橙色,最终沉淀消失,溶液几乎无色。 |
(1)A中产生SO2的化学方程式为
(2)暗红褐色沉淀X可能含Fe3+、OH-、SO
 、SO
、SO ,检验如下:
,检验如下:实验二:向X中加入足量盐酸,沉淀溶解。取少量溶液,滴加KSCN溶液后变红。证明溶液中存在
 ,原因是
,原因是实验三:向X中加入H2C2O4溶液,沉淀溶解。继续滴加BaCl2溶液,产生白色沉淀,过滤后,向沉淀中加入盐酸,白色沉淀溶解。确认X中不含SO
 。
。实验三中用H2C2O4溶液溶解沉淀的目的是:
实验四:向X中加入足量盐酸,沉淀溶解。加入几滴碘水(含淀粉),蓝色立即褪去。静置,一段时间后蓝色复现,振荡,不褪色。
结合离子方程式解释沉淀溶解后的现象:
(3)查阅资料:a.Fe3+、SO
 、H2O(或OH﹣)会形成配合物HOFeOSO2。
、H2O(或OH﹣)会形成配合物HOFeOSO2。
 和O2在金属离子的催化作用下产生具有强氧化性的过一硫酸(HSO
和O2在金属离子的催化作用下产生具有强氧化性的过一硫酸(HSO
①向溶液Y中滴加2滴KSCN溶液,未见红色;再加几滴6mol·L-1盐酸,溶液变红。溶液Y中存在Fe(Ⅲ),但直接滴加KSCN溶液未见红色的原因是
②取出部分实验一中的橙色溶液,久置不褪色。结合资料a中过程ii分析实验一中溶液最终“几乎无色”的原因:
总结:SO2与K2FeO4发生了氧化还原反应和复分解反应,并且遵循化学反应速率和限度规律。
您最近半年使用:0次
6 .  溶液久置变为黄色(记为溶液A)。探究溶液A中阴离子的种类。
溶液久置变为黄色(记为溶液A)。探究溶液A中阴离子的种类。
已知:
ⅰ.
ⅱ.某些盐的溶解性(注: 、
、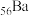 同主族)
同主族)
ⅲ. 、
、 、
、 、
、 、ZnS均可被
、ZnS均可被 氧化。
氧化。
(1)查阅资料可知,溶液变黄是因为生成了 ,
, 转化为
转化为 时,溶液的pH会
时,溶液的pH会___________ (填“升高”或“降低”)。
(2)探究溶液A中含硫粒子的种类。 和
和___________ (填离子符号)。
②向少量含淀粉的稀碘水中滴加滤液2(已调至中性),___________ (填现象),证实溶液A中有 。
。
③加入过量 溶液的目的是
溶液的目的是___________ 。
(3)利用如下实验可测定 中x的值。
中x的值。
【实验原理】 ,其中
,其中 和
和 的化学计量数之比等于
的化学计量数之比等于___________ 。通过测定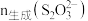 和
和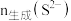 可确定x的值。
可确定x的值。
【实验过程】
实验Ⅰ 的目的是除去
的目的是除去 ,相关离子方程式是
,相关离子方程式是___________ 。
②实验Ⅱ中操作X是加入___________ (补全试剂和操作)。
③用 标准溶液滴定
标准溶液滴定___________ (填序号,下同),可确定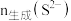 ;再用
;再用 标准溶液滴定
标准溶液滴定___________ ,可确定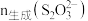 。(说明:滴定过程中需调节pH)
。(说明:滴定过程中需调节pH)
a.溶液A b.溶液 c.沉淀E d.溶液F
c.沉淀E d.溶液F
【数据处理】计算x的值。
 溶液久置变为黄色(记为溶液A)。探究溶液A中阴离子的种类。
溶液久置变为黄色(记为溶液A)。探究溶液A中阴离子的种类。已知:
ⅰ.

ⅱ.某些盐的溶解性(注:
 、
、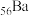 同主族)
同主族)| 盐 | ZnS(白色) | CuS(黑色) | SrS | 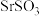 |  | 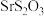 |
| 溶解性 | 难溶 | 极难溶 | 易溶 | 难溶 | 难溶 | 易溶 |
 、
、 、
、 、
、 、ZnS均可被
、ZnS均可被 氧化。
氧化。(1)查阅资料可知,溶液变黄是因为生成了
 ,
, 转化为
转化为 时,溶液的pH会
时,溶液的pH会(2)探究溶液A中含硫粒子的种类。
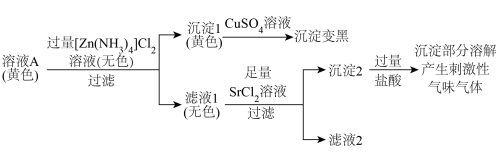
 和
和②向少量含淀粉的稀碘水中滴加滤液2(已调至中性),
 。
。③加入过量
 溶液的目的是
溶液的目的是(3)利用如下实验可测定
 中x的值。
中x的值。【实验原理】
 ,其中
,其中 和
和 的化学计量数之比等于
的化学计量数之比等于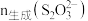 和
和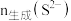 可确定x的值。
可确定x的值。【实验过程】
实验Ⅰ

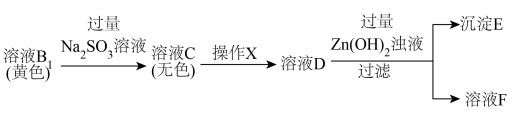
 的目的是除去
的目的是除去 ,相关离子方程式是
,相关离子方程式是②实验Ⅱ中操作X是加入
③用
 标准溶液滴定
标准溶液滴定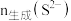 ;再用
;再用 标准溶液滴定
标准溶液滴定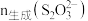 。(说明:滴定过程中需调节pH)
。(说明:滴定过程中需调节pH)a.溶液A b.溶液
 c.沉淀E d.溶液F
c.沉淀E d.溶液F【数据处理】计算x的值。
您最近半年使用:0次
名校
解题方法
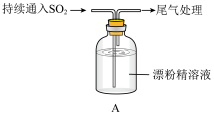
7 . 某学生对 与漂粉精的反应进行实验探究:
与漂粉精的反应进行实验探究:
(1)pH试纸颜色的变化说明漂粉精溶液具有的性质是______ 。
(2)向水中持续通入 ,未观察到白雾。推测现象ⅰ的白雾由HCl小液滴形成,进行如下实验:
,未观察到白雾。推测现象ⅰ的白雾由HCl小液滴形成,进行如下实验:
a.用湿润的碘化钾淀粉试纸检验白雾,无变化;
b.用硝酸酸化的 溶液检验白雾,产生白色沉淀。
溶液检验白雾,产生白色沉淀。
①实验a目的是______ 。
②由实验a、b不能判断白雾中含有HCl,理由是______ 。
(3)现象ⅱ中溶液变为黄绿色的可能原因:随溶液酸性的增强,漂粉精的有效成分和 发生反应。通过进一步实验确认了这种可能性,其实验方案是
发生反应。通过进一步实验确认了这种可能性,其实验方案是______ 。
(4)将A瓶中混合物过滤、洗涤,得到沉淀X。
①向沉淀X中加入稀HCl,无明显变化。取上层清液,加入 溶液,产生白色沉淀。则沉淀X中含有的物质是
溶液,产生白色沉淀。则沉淀X中含有的物质是______ 。
②用离子方程式解释现象ⅲ中黄绿色褪去的原因:______ 。
 与漂粉精的反应进行实验探究:
与漂粉精的反应进行实验探究:操作 | 现象 |
| 取4g漂粉精固体,加入100mL水 | 部分固体溶解,溶液略有颜色 |
| 过滤,测漂粉精溶液的pH | pH试纸先变蓝(约为12),后褪色 |
| ⅰ.液面上方出现白雾; ⅱ.稍后,出现浑浊,溶液变为黄绿色; ⅲ.稍后,产生大量白色沉淀,黄绿色褪去 |
(2)向水中持续通入
 ,未观察到白雾。推测现象ⅰ的白雾由HCl小液滴形成,进行如下实验:
,未观察到白雾。推测现象ⅰ的白雾由HCl小液滴形成,进行如下实验:a.用湿润的碘化钾淀粉试纸检验白雾,无变化;
b.用硝酸酸化的
 溶液检验白雾,产生白色沉淀。
溶液检验白雾,产生白色沉淀。①实验a目的是
②由实验a、b不能判断白雾中含有HCl,理由是
(3)现象ⅱ中溶液变为黄绿色的可能原因:随溶液酸性的增强,漂粉精的有效成分和
 发生反应。通过进一步实验确认了这种可能性,其实验方案是
发生反应。通过进一步实验确认了这种可能性,其实验方案是(4)将A瓶中混合物过滤、洗涤,得到沉淀X。
①向沉淀X中加入稀HCl,无明显变化。取上层清液,加入
 溶液,产生白色沉淀。则沉淀X中含有的物质是
溶液,产生白色沉淀。则沉淀X中含有的物质是②用离子方程式解释现象ⅲ中黄绿色褪去的原因:
您最近半年使用:0次
8 . 下列实验结论与实验操作及现象不相符 的一组是
| 选项 | 实验操作及现象 | 实验结论 |
| A | 向样品中加入 溶液,有白色沉淀生成 溶液,有白色沉淀生成 | 样品中一定含 |
| B | 向 -淀粉溶液中滴入氯水,溶液变成蓝色 -淀粉溶液中滴入氯水,溶液变成蓝色 |  的还原性强于 的还原性强于 |
| C | 向某溶液中加入稀盐酸,产生的气体使澄清石灰水变浑浊 | 该溶液中可能含有 |
| D | 向某盐溶液中加入 溶液,加热,用湿润的红色石蕊试纸放在试管口,试纸变蓝 溶液,加热,用湿润的红色石蕊试纸放在试管口,试纸变蓝 | 该盐溶液中含有 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
解题方法
9 . (一)某同学为研究浓硝酸与KSCN溶液的反应,进行如下实验:
资料: 能被氧化为(SCN)2,(SCN)2迅速聚合为红色的(SCN)x。
能被氧化为(SCN)2,(SCN)2迅速聚合为红色的(SCN)x。
(1)KSCN中,C、N元素的化合价分别为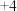 价和
价和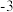 价,则S元素的化合价为
价,则S元素的化合价为_________ 。
(2)I中溶液立即变红是因为生成了__________________ (填化学式)。
(二)研究 的最终转化产物。
的最终转化产物。
(3)取少量Ⅱ中试管内的溶液,_________ (填操作和现象),证明 中S元素的转化产物是
中S元素的转化产物是 。
。
(4)经检验Ⅱ中“红棕色气体”含有 ,但不能说明
,但不能说明 一定是
一定是 中N元素的转化产物,原因是
中N元素的转化产物,原因是__________________ 。
将Ⅱ中沉淀过滤、洗涤,取少量于试管中,加入过量的稀硝酸,沉淀完全溶解,再滴加少量 溶液,不褪色。证明了红棕色气体中不含
溶液,不褪色。证明了红棕色气体中不含 。
。
(5)综合上述实验, 的最终转化产物中一定有
的最终转化产物中一定有__________________ 。
| 实验操作 | 实验现象 |
I.取1支试管,加入 浓硝酸,滴加5滴 浓硝酸,滴加5滴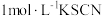 溶液 溶液 | 溶液立即变红 |
| Ⅱ.将试管静置一段时间 | 突然剧烈反应,红色迅速褪去,放出大量红棕色气体 |
Ⅲ.将Ⅱ中的气体通入 和 和 的混合溶液中 的混合溶液中 | 有白色沉淀生成 |
 能被氧化为(SCN)2,(SCN)2迅速聚合为红色的(SCN)x。
能被氧化为(SCN)2,(SCN)2迅速聚合为红色的(SCN)x。(1)KSCN中,C、N元素的化合价分别为
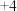 价和
价和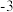 价,则S元素的化合价为
价,则S元素的化合价为(2)I中溶液立即变红是因为生成了
(二)研究
 的最终转化产物。
的最终转化产物。(3)取少量Ⅱ中试管内的溶液,
 中S元素的转化产物是
中S元素的转化产物是 。
。(4)经检验Ⅱ中“红棕色气体”含有
 ,但不能说明
,但不能说明 一定是
一定是 中N元素的转化产物,原因是
中N元素的转化产物,原因是将Ⅱ中沉淀过滤、洗涤,取少量于试管中,加入过量的稀硝酸,沉淀完全溶解,再滴加少量
 溶液,不褪色。证明了红棕色气体中不含
溶液,不褪色。证明了红棕色气体中不含 。
。(5)综合上述实验,
 的最终转化产物中一定有
的最终转化产物中一定有
您最近半年使用:0次
名校
解题方法
10 . 实验小组探究 与
与 的反应。向盛有
的反应。向盛有 的烧瓶中加入
的烧瓶中加入 固体,测得反应体系中
固体,测得反应体系中 含量的变化如图。
含量的变化如图。

下列说法不正确 的是
 与
与 的反应。向盛有
的反应。向盛有 的烧瓶中加入
的烧瓶中加入 固体,测得反应体系中
固体,测得反应体系中 含量的变化如图。
含量的变化如图。
下列说法
A.有 生成推测发生了反应: 生成推测发生了反应: |
B.bc段 含量下降与反应 含量下降与反应 有关 有关 |
C.可用 酸化的 酸化的 溶液检验b点固体中是否含有 溶液检验b点固体中是否含有 |
D.产物 也可能是 也可能是 与 与 直接化合生成的 直接化合生成的 |
您最近半年使用:0次