1 . 四氧化三铁磁流体既具有固体的磁性,又具有液体的流动性,采用共沉淀法可以制得黑色的分散质微粒直径介于5.5-36nm纳米级磁流体材料。其流程如下图所示:
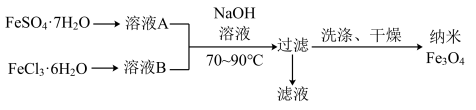
下列说法错误的是

下列说法错误的是
| A.该磁流体材料形成的分散系能产生丁达尔效应 |
| B.取溶液B加入硫氰酸钾溶液,溶液变为红色 |
| C.FeCl3·6H2O和FeSO4·7H2O的物质的量之比最好为1∶2 |
| D.取最后一次的洗涤液,加入氯化钡溶液,若无白色沉淀,证明沉淀已经洗涤干净 |
您最近一年使用:0次
2 . 下列有关实验的说法,错误的是
| A.实验剩余药品都不能放回原试剂瓶,防止污染瓶中药品 |
B.模拟“侯氏制碱法”时,应向饱和 溶液中先通入 溶液中先通入 再通入 再通入 |
C.进行粗盐提纯时,可向上层清液中滴加 滴 滴 溶液以检验 溶液以检验 是否除尽 是否除尽 |
| D.某些强氧化剂(如:氯酸钾、高锰酸钾)及其混合物不能研磨,否则可能引起爆炸 |
您最近一年使用:0次
解题方法
3 . 硫及其化合物的“价-类”二维图如下图所示,回答下列问题:
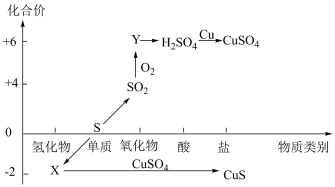
(1) 的电子式是
的电子式是______ , 的化学式是
的化学式是______ 。
(2) 与
与 反应的化学方程式是
反应的化学方程式是______ ,氧化剂是______ (填化学式)。
(3) 属于
属于______ (填“强”、“弱”或“非”)电解质,检验 时,取少量待测液于试管中,先加入
时,取少量待测液于试管中,先加入______ ,无明显现象,再加入______ 溶液,若产生白色沉淀,则溶液中含有 。
。
(4) 与足量浓硫酸反应也可制得
与足量浓硫酸反应也可制得 ,该反应的化学方程式为:
,该反应的化学方程式为: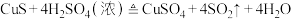 。
。
①请用“双线桥”法标明该反应电子转移的方向和数目______ 。
②当有 电子发生转移时,理论上生成
电子发生转移时,理论上生成 的体积(标准状况)为
的体积(标准状况)为______  。
。
(5)某化工厂生产硫酸,使用一种含杂质为 的黄铁矿原料。若取
的黄铁矿原料。若取 该矿石,理论上可制得
该矿石,理论上可制得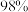 的浓硫酸
的浓硫酸______  (假设生产过程中硫的损失为零)。
(假设生产过程中硫的损失为零)。
已知黄铁矿与氧气反应的化学方程式是

(1)
 的电子式是
的电子式是 的化学式是
的化学式是(2)
 与
与 反应的化学方程式是
反应的化学方程式是(3)
 属于
属于 时,取少量待测液于试管中,先加入
时,取少量待测液于试管中,先加入 。
。(4)
 与足量浓硫酸反应也可制得
与足量浓硫酸反应也可制得 ,该反应的化学方程式为:
,该反应的化学方程式为: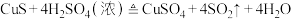 。
。①请用“双线桥”法标明该反应电子转移的方向和数目
②当有
 电子发生转移时,理论上生成
电子发生转移时,理论上生成 的体积(标准状况)为
的体积(标准状况)为 。
。(5)某化工厂生产硫酸,使用一种含杂质为
 的黄铁矿原料。若取
的黄铁矿原料。若取 该矿石,理论上可制得
该矿石,理论上可制得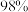 的浓硫酸
的浓硫酸 (假设生产过程中硫的损失为零)。
(假设生产过程中硫的损失为零)。已知黄铁矿与氧气反应的化学方程式是

您最近一年使用:0次
名校
4 . 粗食盐中常含有钙盐、镁盐、硫酸盐等可溶性杂质,一种制备精盐的工艺流程如下图所示(所加试剂均过量),下列说法正确的是


| A.操作Ⅰ、Ⅱ、Ⅲ都要用到玻璃棒 |
| B.若试剂1是NaOH溶液,则试剂2是Na2CO3溶液 |
| C.白色沉淀的主要成分为氢氧化镁和碳酸钙 |
D.取滤液滴加BaCl2溶液,可检验 是否除净 是否除净 |
您最近一年使用:0次
2024-02-04更新
|
106次组卷
|
3卷引用:安徽省蒙城县2023-2024学年高一上学期期末联考化学试题
解题方法
5 . 根据实验操作和现象得出的结论正确的是
| 选项 | 实验操作和现象 | 实验结论 |
| A. | 用铂丝蘸取少量某溶液进行焰色试验,火焰呈黄色,透过蓝色钴玻璃显紫色 | 该溶液中一定含有钠钾两种元素 |
| B. | 取一定量可能被氧化的还原铁粉,加稀盐酸溶解,滴入几滴KSCN溶液,溶液不显血红色 | 还原铁粉未变质 |
| C. | 测等浓度的HF溶液与HCl溶液的pH,前者大于后者 | F的非金属性强于Cl |
| D. | 向某溶液中加入盐酸酸化的 溶液,有白色沉淀生成 溶液,有白色沉淀生成 | 该溶液中一定含 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-02-03更新
|
162次组卷
|
4卷引用:湖北省武汉市部分重点中学2023-2024学年高一上学期期末联考化学试题
湖北省武汉市部分重点中学2023-2024学年高一上学期期末联考化学试题(已下线)5.1.3硫酸根离子的检验和含硫化合物的转化课后作业基础篇(已下线)5.1.3硫酸根离子的检验和含硫化合物的转化课后作业巩固篇湖北省黄冈市黄梅县晋梅高级中学2023-2024学年高一下学期3月月考化学试题
解题方法
6 . 根据下列有关化学实验操作,得出的现象、解释与结论均正确的是
| 选项 | 实验操作 | 现象 | 解释与结论 |
| A | 将点燃的氢气的导管伸入到盛满氯气的集气瓶中 | 氢气继续燃烧,火焰呈苍白色,瓶口产生大量白烟 | 反应生成HCl |
| B | 用玻璃棒蘸取NaClO溶液滴在pH试纸上,测其酸碱性及pH值 | 试纸变蓝 | NaClO溶液显碱性 |
| C | 将硫酸酸化的H2O2滴入FeSO4溶液中 | 溶液由浅绿色变为黄色 | 证明H2O2的氧化性强于Fe3+ |
| D | 某澄清溶液中加入盐酸酸化的氯化钡溶液 | 产生白色沉淀 | 原溶液中一定含有 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
7 . 有关溶液中离子检验的实验操作和结论正确的是
A.某溶液中滴加BaCl2溶液产生白色沉淀,再滴入稀盐酸沉淀不溶解,一定有 |
| B.K2SO4溶液的焰色试验现象为火焰呈紫色,这是K2SO4溶液的化学性质 |
| C.用洁净的铂丝蘸取某溶液在火焰上灼烧,火焰呈黄色,一定有Na+没有K+ |
| D.用洁净的铂丝蘸取某溶液在火焰上灼烧,火焰呈黄色,一定有Na+可能有K+ |
您最近一年使用:0次
8 . 根据下列实验操作和现象所得到的结论正确的是
| 选项 | 实验操作和现象 | 结论 |
| A | 向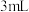 淀粉 淀粉 溶液中滴加几滴氯水,振荡,溶液变为蓝色 溶液中滴加几滴氯水,振荡,溶液变为蓝色 | 氧化性: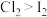 |
| B | 向溶液Y中滴加硝酸酸化的硝酸钡溶液,产生白色沉淀 | 溶液Y含 |
| C | 向表面皿中加入少量 ,再加入约 ,再加入约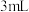 浓硫酸,搅拌,观察实验现象 浓硫酸,搅拌,观察实验现象 | 浓硫酸具有脱水性 |
| D | 向溶液X中加入稀 溶液,将湿润的红色石蕊试纸置于试管口,试纸未变蓝色 溶液,将湿润的红色石蕊试纸置于试管口,试纸未变蓝色 | 溶液X不含 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
9 . 对某透明溶液分别进行下列操作所得现象和结论均正确的是
A.加入硝酸钡溶液有白色沉淀产生,再加稀盐酸,沉淀不消失,则原溶液中一定有 |
B.加入硝酸酸化的 溶液,无明显现象,再滴加 溶液,无明显现象,再滴加 溶液,有白色沉淀生成,则溶液中一定含有 溶液,有白色沉淀生成,则溶液中一定含有 |
C.滴加 溶液后再加入KSCN溶液,溶液呈红色,则原溶液中一定含有 溶液后再加入KSCN溶液,溶液呈红色,则原溶液中一定含有 |
D.加入 溶液,有白色沉淀生成,再滴加盐酸沉淀消失,则原溶液中一定有 溶液,有白色沉淀生成,再滴加盐酸沉淀消失,则原溶液中一定有 |
您最近一年使用:0次
10 . 某种混合溶液中可能含有K+、CO 、SO
、SO 这些阴阳离子中的几种,某同学为了确定存在的阴、阳离子种类,设计了以下实验方案,请你帮该同学完成实验方案的内容:
这些阴阳离子中的几种,某同学为了确定存在的阴、阳离子种类,设计了以下实验方案,请你帮该同学完成实验方案的内容:
(1)取少量混合溶液于试管中,进行_______ ,透过_______ ,如果观察到火焰呈_______ 色,证明溶液中含有K+。
(2)另取少量混合溶液,加入_______ ,若无明显现象,则说明不含有_______ ;再加入_______ ,若有产生白色沉淀,证明含有SO 。
。
 、SO
、SO 这些阴阳离子中的几种,某同学为了确定存在的阴、阳离子种类,设计了以下实验方案,请你帮该同学完成实验方案的内容:
这些阴阳离子中的几种,某同学为了确定存在的阴、阳离子种类,设计了以下实验方案,请你帮该同学完成实验方案的内容:(1)取少量混合溶液于试管中,进行
(2)另取少量混合溶液,加入
 。
。
您最近一年使用:0次



