名校
解题方法
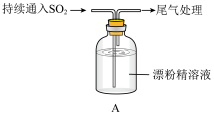
1 . 某学生对 与漂粉精的反应进行实验探究:
与漂粉精的反应进行实验探究:
(1)pH试纸颜色的变化说明漂粉精溶液具有的性质是______ 。
(2)向水中持续通入 ,未观察到白雾。推测现象ⅰ的白雾由HCl小液滴形成,进行如下实验:
,未观察到白雾。推测现象ⅰ的白雾由HCl小液滴形成,进行如下实验:
a.用湿润的碘化钾淀粉试纸检验白雾,无变化;
b.用硝酸酸化的 溶液检验白雾,产生白色沉淀。
溶液检验白雾,产生白色沉淀。
①实验a目的是______ 。
②由实验a、b不能判断白雾中含有HCl,理由是______ 。
(3)现象ⅱ中溶液变为黄绿色的可能原因:随溶液酸性的增强,漂粉精的有效成分和 发生反应。通过进一步实验确认了这种可能性,其实验方案是
发生反应。通过进一步实验确认了这种可能性,其实验方案是______ 。
(4)将A瓶中混合物过滤、洗涤,得到沉淀X。
①向沉淀X中加入稀HCl,无明显变化。取上层清液,加入 溶液,产生白色沉淀。则沉淀X中含有的物质是
溶液,产生白色沉淀。则沉淀X中含有的物质是______ 。
②用离子方程式解释现象ⅲ中黄绿色褪去的原因:______ 。
 与漂粉精的反应进行实验探究:
与漂粉精的反应进行实验探究:操作 | 现象 |
| 取4g漂粉精固体,加入100mL水 | 部分固体溶解,溶液略有颜色 |
| 过滤,测漂粉精溶液的pH | pH试纸先变蓝(约为12),后褪色 |
| ⅰ.液面上方出现白雾; ⅱ.稍后,出现浑浊,溶液变为黄绿色; ⅲ.稍后,产生大量白色沉淀,黄绿色褪去 |
(2)向水中持续通入
 ,未观察到白雾。推测现象ⅰ的白雾由HCl小液滴形成,进行如下实验:
,未观察到白雾。推测现象ⅰ的白雾由HCl小液滴形成,进行如下实验:a.用湿润的碘化钾淀粉试纸检验白雾,无变化;
b.用硝酸酸化的
 溶液检验白雾,产生白色沉淀。
溶液检验白雾,产生白色沉淀。①实验a目的是
②由实验a、b不能判断白雾中含有HCl,理由是
(3)现象ⅱ中溶液变为黄绿色的可能原因:随溶液酸性的增强,漂粉精的有效成分和
 发生反应。通过进一步实验确认了这种可能性,其实验方案是
发生反应。通过进一步实验确认了这种可能性,其实验方案是(4)将A瓶中混合物过滤、洗涤,得到沉淀X。
①向沉淀X中加入稀HCl,无明显变化。取上层清液,加入
 溶液,产生白色沉淀。则沉淀X中含有的物质是
溶液,产生白色沉淀。则沉淀X中含有的物质是②用离子方程式解释现象ⅲ中黄绿色褪去的原因:
您最近半年使用:0次
名校
解题方法
2 . 某小组同学探究SO2与新制Cu(OH)2悬浊液反应的实验装置图如下所示:
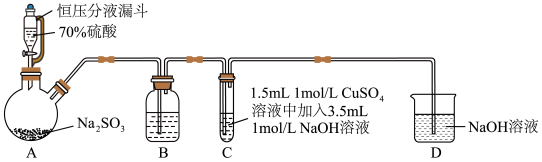
| A.配制70%的硫酸溶液需要用到的仪器有烧杯、量筒、玻璃棒、胶头滴管 |
| B.装置B的作用是监控SO2流速,其中试剂可以用饱和 NaHSO3溶液 |
| C.反应开始时C中出现砖红色沉淀(Cu2O),氧化剂和还原剂的物质的量之比为2:1 |
| D.反应后向C的溶液中加入稀盐酸酸化后,再滴加BaCl2溶液,有白色沉淀生成,证明反应中SO2作还原剂 |
您最近半年使用:0次
3 . “价—类”二维图是预测物质性质的重要思维工具。如图是硫元素的常见化合价与部分物质类别的对应关系。___________ 氧化物。
(2)A 中硫元素处于最低化合价,具有___________ 性,预测 A 溶液久置于空气会出现的现象___________ ,写出发生反应的化学方程式___________ 。
(3)气体A 和气体C混合时有黄色粉末生成,该反应的化学方程式为___________ ;试管内的单质B可用热的NaOH溶液洗涤,反应过程中仅生成G、水以及另一种钠盐,该钠盐的化学式为___________ 。
(4)工业上用___________ (填试剂名称)吸收D制E,检验某溶液中是否含有:  的方法为取适量待测液于试管中,加入足量
的方法为取适量待测液于试管中,加入足量___________ ,充分反应后,再滴加适量___________ ,若产生白色沉淀,则证明溶液中含有: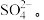
(5)E的浓溶液与碳单质在加热条件下发生反应,若要验证气体产物有(CO2和SO2可选择以下试剂进行实验:
①酸性高锰酸钾 ②品红溶液 ③澄清石灰水,合理的顺序为___________ (填序号)。
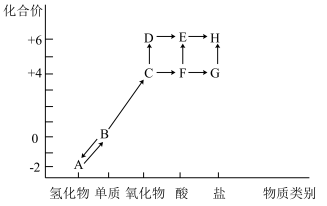
(2)A 中硫元素处于最低化合价,具有
(3)气体A 和气体C混合时有黄色粉末生成,该反应的化学方程式为
(4)工业上用
 的方法为取适量待测液于试管中,加入足量
的方法为取适量待测液于试管中,加入足量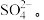
(5)E的浓溶液与碳单质在加热条件下发生反应,若要验证气体产物有(CO2和SO2可选择以下试剂进行实验:
①酸性高锰酸钾 ②品红溶液 ③澄清石灰水,合理的顺序为
您最近半年使用:0次
4 . 下列实验结论与实验操作及现象不相符 的一组是
| 选项 | 实验操作及现象 | 实验结论 |
| A | 向样品中加入 溶液,有白色沉淀生成 溶液,有白色沉淀生成 | 样品中一定含 |
| B | 向 -淀粉溶液中滴入氯水,溶液变成蓝色 -淀粉溶液中滴入氯水,溶液变成蓝色 |  的还原性强于 的还原性强于 |
| C | 向某溶液中加入稀盐酸,产生的气体使澄清石灰水变浑浊 | 该溶液中可能含有 |
| D | 向某盐溶液中加入 溶液,加热,用湿润的红色石蕊试纸放在试管口,试纸变蓝 溶液,加热,用湿润的红色石蕊试纸放在试管口,试纸变蓝 | 该盐溶液中含有 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
5 . 为了除去粗盐中的 、
、 、
、 及泥沙,可将粗盐溶于水,然后进行下列五项操作。正确的操作顺序是:
及泥沙,可将粗盐溶于水,然后进行下列五项操作。正确的操作顺序是:
①过滤,②加过量的NaOH溶液,③加适量盐酸,④加过量 溶液,⑤加过量
溶液,⑤加过量 溶液
溶液
 、
、 、
、 及泥沙,可将粗盐溶于水,然后进行下列五项操作。正确的操作顺序是:
及泥沙,可将粗盐溶于水,然后进行下列五项操作。正确的操作顺序是:①过滤,②加过量的NaOH溶液,③加适量盐酸,④加过量
 溶液,⑤加过量
溶液,⑤加过量 溶液
溶液| A.④②⑤①③ | B.④⑤②①③ | C.⑤④①②③ | D.⑤④②①③ |
您最近半年使用:0次
6 . 下列有关实验操作、现象和解释或结论都正确的是
| 选项 | 实验操作 | 现象 | 解释或结论 |
| A | 过量的Fe粉中加入稀HNO3,充分反应后,滴入KSCN溶液 | 溶液呈红色 | 稀HNO3将Fe氧化为Fe3+ |
| B | Na2SO3固体加水溶解后,滴加硝酸酸化的硝酸钡溶液 | 产生白色沉淀 | Na2SO3已变质 |
| C | 铁片插入浓HNO3中 | 无现象 | 铁片遇浓HNO3钝化,没发生化学变化 |
| D | 用玻璃棒蘸取浓HNO3点到红色石蕊试纸上 | 试纸变蓝色然后褪色 | 浓HNO3具有酸性和强氧化性 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
解题方法
7 . 下列实验能达到目的或结论正确的是
| 选项 | 实验 | 目的或结论 |
| A | 将混有 、 、 的 的 依次通过足量的氢氧化钠溶液、灼热的铜网,最后用真空气囊收集 依次通过足量的氢氧化钠溶液、灼热的铜网,最后用真空气囊收集 | 可以收集干燥纯净的 |
| B | 取少量 固体溶于水,加入足量稀硝酸酸化,再加入 固体溶于水,加入足量稀硝酸酸化,再加入 溶液 溶液 | 有沉淀生成,证明探究 已经变质 已经变质 |
| C | 浓硫酸滴入蔗糖中,产生的气体导入澄清石灰水 | 蔗糖变黑、体积膨胀,澄清石灰水变浑浊,说明浓硫酸具有脱水性和强氧化性 |
| D | 铁粉中加入少量稀硝酸,充分反应后,滴加KSCN溶液 | 有无色气泡产生,溶液呈血红色,说明稀硝酸能将 氧化成 氧化成 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
解题方法
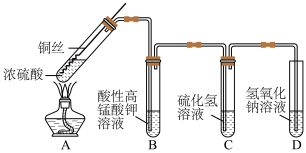
8 . 某化学实验小组的同学利用铜与浓硫酸反应制取二氧化硫并研究其性质,所用实验装置如下:
(1)将铜丝下端卷成螺旋状的理由是___________ 。
(2)装置A中反应的化学方程式是___________ ,该反应中浓硫酸体现的性质___________ 。
(3)装置B中反应的离子方程式是___________ 。
(4)氢氧化钠溶液的作用是___________ 。
(5)向外拉铜丝,终止反应,冷却后,进一步证明A装置试管中反应所得产物含有铜离子的操作是___________ 。请设计实验验证该产物中的阴离子___________
(6)化学实验小组的同学发现试管中有黑色物质产生,猜测黑色物质中可能含有 、
、 和
和 ,针对产生的黑色物质,该小组同学利用装置A用不同浓度的浓硫酸与铜反应继续实验探究,并获得数据如下表。下列说法错误的是___________(填字母)。已知:
,针对产生的黑色物质,该小组同学利用装置A用不同浓度的浓硫酸与铜反应继续实验探究,并获得数据如下表。下列说法错误的是___________(填字母)。已知: 、
、 不溶于稀硫酸。
不溶于稀硫酸。
(1)将铜丝下端卷成螺旋状的理由是
(2)装置A中反应的化学方程式是
(3)装置B中反应的离子方程式是
(4)氢氧化钠溶液的作用是
(5)向外拉铜丝,终止反应,冷却后,进一步证明A装置试管中反应所得产物含有铜离子的操作是
(6)化学实验小组的同学发现试管中有黑色物质产生,猜测黑色物质中可能含有
 、
、 和
和 ,针对产生的黑色物质,该小组同学利用装置A用不同浓度的浓硫酸与铜反应继续实验探究,并获得数据如下表。下列说法错误的是___________(填字母)。已知:
,针对产生的黑色物质,该小组同学利用装置A用不同浓度的浓硫酸与铜反应继续实验探究,并获得数据如下表。下列说法错误的是___________(填字母)。已知: 、
、 不溶于稀硫酸。
不溶于稀硫酸。硫酸浓度/( ) ) | 黑色物质出现的温度/℃ | 黑色物质消失的温度/℃ |
| 15 | 约150 | 约236 |
| 16 | 约140 | 约250 |
| 18 | 约120 | 不消失 |
A.取黑色物质洗涤、干燥后称量,加入足量稀硫酸充分混合,再取固体洗涤、干燥后称量,固体质量不变,说明黑色物质中不含 |
B.黑色物质消失过程中有 、 、 生成 生成 |
| C.相同条件下,硫酸浓度越大,反应速率越快,黑色物质越易出现、越易消失 |
D.硫酸浓度为16 时,先升温至250℃以上,再将铜与浓硫酸接触,可避免产生黑色物质 时,先升温至250℃以上,再将铜与浓硫酸接触,可避免产生黑色物质 |
您最近半年使用:0次
9 . 下列叙述正确的是
A.向某溶液中加入BaCl2,产生不溶于稀HNO3的白色沉淀,则溶液中一定含有 |
| B.将浓硫酸滴入蔗糖,固体变黑膨胀,说明浓硫酸有吸水性和强氧化性 |
| C.浓硝酸具有不稳定性,实验室保存时可使用棕色试剂瓶,放置在阴凉处 |
| D.氢氧化钠溶液保存在带玻璃塞的试剂瓶中 |
您最近半年使用:0次
名校
10 . 硫酰氯(SO2Cl2)是一种重要的有机氯化剂,可用于制造医药品、农药和染料等。某化学学习小组用干燥的SO2和Cl2在活性炭催化下制取硫酰氯,反应的化学方程式为: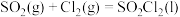 ,该反应为放热反应,装置如图所示(部分夹持装置省略)。
,该反应为放热反应,装置如图所示(部分夹持装置省略)。
(1)仪器A的名称为___________ 。
(2)C中盛放的药品是___________ ,其作用为___________ 。
(3)用浓盐酸和高锰酸钾反应可以制备氯气,写出相关离子方程式___________ 。
(4)若缺少装置乙和丁,对产品硫酰氯会有何影响,请用化学方程式表示___________ 。
(5)反应过程中,为防止SO2Cl2分解,可采取的措施有___________ 。(至少写一条)
(6)该化学小组成员经过实验测得产物量较少,猜测可能是原料中亚硫酸钠部分变质,为了验证亚硫酸钠发生了变质,可设计如下实验:取少量亚硫酸钠原料加水溶解,___________ 。
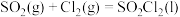 ,该反应为放热反应,装置如图所示(部分夹持装置省略)。
,该反应为放热反应,装置如图所示(部分夹持装置省略)。
(1)仪器A的名称为
(2)C中盛放的药品是
(3)用浓盐酸和高锰酸钾反应可以制备氯气,写出相关离子方程式
(4)若缺少装置乙和丁,对产品硫酰氯会有何影响,请用化学方程式表示
(5)反应过程中,为防止SO2Cl2分解,可采取的措施有
(6)该化学小组成员经过实验测得产物量较少,猜测可能是原料中亚硫酸钠部分变质,为了验证亚硫酸钠发生了变质,可设计如下实验:取少量亚硫酸钠原料加水溶解,
您最近半年使用:0次