1 . 下列实验、现象与结论不对应的一组是
| 选项 | 实验 | 现象 | 结论 |
| A | 向某溶液滴加盐酸,无明显现象,再加BaCl2溶液 | 产生白色沉淀 | 溶液中含有 |
| B | 向某盐溶液中加入浓NaOH溶液,加热 | 产生的气体能使湿润的红色石蕊试纸变蓝 | 该溶液中含有 |
| C | 向某溶液中滴加稀盐酸,将产生的气体通入澄清石灰水中 | 澄消石灰水变浑浊 | 该溶液中不一定含有 |
| D | 用洁净的铂丝蘸取某溶液在酒精灯外焰上灼烧 | 观察不到紫色 | 溶液中一定没有钾元素 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2 . 下列实验方案设计、现象和结论都正确的是
| 选项 | 目的 | 方案设计 | 现象和结论 |
| A | 探究溴乙烷消去反应的产物是乙烯 | 取溴乙烷,加入乙醇、氢氧化钠固体,加热,将产生的气体通入 溶液中 溶液中 | 若 溶液褪色,则溴乙烷消去反应的产物为乙烯 溶液褪色,则溴乙烷消去反应的产物为乙烯 |
| B | 证明酸性:碳酸>苯酚 | 将盐酸与 混合产生的气体直接通入苯酚钠溶液 混合产生的气体直接通入苯酚钠溶液 | 若溶液变浑浊,这证明碳酸酸性大于苯酚 |
| C | 探究 固体样品是否变质 固体样品是否变质 | 取少量待测样品溶于蒸馏水,加入足量稀盐酸,再加入足量 溶液 溶液 | 若有白色沉淀产生,则样品已经变质 |
| D | 验证 有还原性 有还原性 | 向HCl酸化的 溶液中滴加 溶液中滴加 溶液,溶液褪色 溶液,溶液褪色 |  具有还原性 具有还原性 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
解题方法
3 . 一种制备 的工艺路线如图所示,反应②所得溶液
的工艺路线如图所示,反应②所得溶液 在3~4之间,反应③需及时补充
在3~4之间,反应③需及时补充 以保持反应在
以保持反应在 条件下进行。
条件下进行。 的电离平衡常数
的电离平衡常数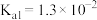 ,
,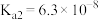 。请回答:
。请回答:
(1)溶液①中阴离子浓度大小(用“>”表示):___________ 。
(2)下列说法正确的是___________。
(3)写出反应③的化学方程式:___________ 。
(4)“低温真空蒸发”可防止 被氧化。请设计实验证明
被氧化。请设计实验证明 是否被氧化
是否被氧化___________ 。若 部分被氧化,为不降低
部分被氧化,为不降低 的产率,补充
的产率,补充 的量应适当
的量应适当___________ (填“增加”“减少”或“不变”)。
 的工艺路线如图所示,反应②所得溶液
的工艺路线如图所示,反应②所得溶液 在3~4之间,反应③需及时补充
在3~4之间,反应③需及时补充 以保持反应在
以保持反应在 条件下进行。
条件下进行。
 的电离平衡常数
的电离平衡常数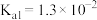 ,
,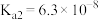 。请回答:
。请回答:(1)溶液①中阴离子浓度大小(用“>”表示):
(2)下列说法正确的是___________。
| A.反应①、②和③均为氧化还原反应 |
| B.气体①和②是造成酸雨的主要成分 |
| C.往反应①后的溶液中加水可得到硫酸铜溶液 |
| D.溶液Y可循环用于反应②进行吸收气体① |
(3)写出反应③的化学方程式:
(4)“低温真空蒸发”可防止
 被氧化。请设计实验证明
被氧化。请设计实验证明 是否被氧化
是否被氧化 部分被氧化,为不降低
部分被氧化,为不降低 的产率,补充
的产率,补充 的量应适当
的量应适当
您最近半年使用:0次
2024-04-21更新
|
187次组卷
|
2卷引用:浙江省金华市十校2023-2024学年高三下学期4月模拟考试化学试题
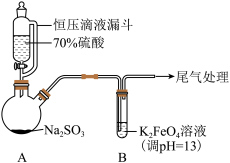
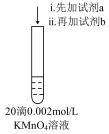
4 . 某实验小组探究SO2与K2FeO4的反应,实验如下。
资料:i.K2FeO4为紫色固体,微溶于KOH溶液;具有强氧化性,在酸性或中性溶液中快速产生O2,在碱性溶液中较稳定。
ii.Fe3+可以与C2O 形成[Fe(C2O4)3]3-;
形成[Fe(C2O4)3]3-;
(1)A中产生SO2的化学方程式为___________ 。
(2)暗红褐色沉淀X可能含Fe3+、OH-、SO 、SO
、SO ,检验如下:
,检验如下:
实验二:向X中加入足量盐酸,沉淀溶解。取少量溶液,滴加KSCN溶液后变红。证明溶液中存在___________ 。另取少量溶液滴加BaCl2溶液,产生白色沉淀,但不能确认含有SO ,原因是
,原因是___________ 。
实验三:向X中加入H2C2O4溶液,沉淀溶解。继续滴加BaCl2溶液,产生白色沉淀,过滤后,向沉淀中加入盐酸,白色沉淀溶解。确认X中不含SO 。
。
实验三中用H2C2O4溶液溶解沉淀的目的是:___________ 。
实验四:向X中加入足量盐酸,沉淀溶解。加入几滴碘水(含淀粉),蓝色立即褪去。静置,一段时间后蓝色复现,振荡,不褪色。
结合离子方程式解释沉淀溶解后的现象:___________ 。
(3)查阅资料:a.Fe3+、SO 、H2O(或OH﹣)会形成配合物HOFeOSO2。
、H2O(或OH﹣)会形成配合物HOFeOSO2。 和O2在金属离子的催化作用下产生具有强氧化性的过一硫酸(HSO
和O2在金属离子的催化作用下产生具有强氧化性的过一硫酸(HSO
①向溶液Y中滴加2滴KSCN溶液,未见红色;再加几滴6mol·L-1盐酸,溶液变红。溶液Y中存在Fe(Ⅲ),但直接滴加KSCN溶液未见红色的原因是___________ 。
②取出部分实验一中的橙色溶液,久置不褪色。结合资料a中过程ii分析实验一中溶液最终“几乎无色”的原因:___________ 。
总结:SO2与K2FeO4发生了氧化还原反应和复分解反应,并且遵循化学反应速率和限度规律。
资料:i.K2FeO4为紫色固体,微溶于KOH溶液;具有强氧化性,在酸性或中性溶液中快速产生O2,在碱性溶液中较稳定。
ii.Fe3+可以与C2O
 形成[Fe(C2O4)3]3-;
形成[Fe(C2O4)3]3-;| 装置 | 操作及现象 |
| 实验一:向B中通入SO2,产生暗红褐色沉淀X和溶液Y(略显红色);继续通入SO2一段时间后,溶液呈红色,继而变为橙色,最终沉淀消失,溶液几乎无色。 |
(1)A中产生SO2的化学方程式为
(2)暗红褐色沉淀X可能含Fe3+、OH-、SO
 、SO
、SO ,检验如下:
,检验如下:实验二:向X中加入足量盐酸,沉淀溶解。取少量溶液,滴加KSCN溶液后变红。证明溶液中存在
 ,原因是
,原因是实验三:向X中加入H2C2O4溶液,沉淀溶解。继续滴加BaCl2溶液,产生白色沉淀,过滤后,向沉淀中加入盐酸,白色沉淀溶解。确认X中不含SO
 。
。实验三中用H2C2O4溶液溶解沉淀的目的是:
实验四:向X中加入足量盐酸,沉淀溶解。加入几滴碘水(含淀粉),蓝色立即褪去。静置,一段时间后蓝色复现,振荡,不褪色。
结合离子方程式解释沉淀溶解后的现象:
(3)查阅资料:a.Fe3+、SO
 、H2O(或OH﹣)会形成配合物HOFeOSO2。
、H2O(或OH﹣)会形成配合物HOFeOSO2。
 和O2在金属离子的催化作用下产生具有强氧化性的过一硫酸(HSO
和O2在金属离子的催化作用下产生具有强氧化性的过一硫酸(HSO
①向溶液Y中滴加2滴KSCN溶液,未见红色;再加几滴6mol·L-1盐酸,溶液变红。溶液Y中存在Fe(Ⅲ),但直接滴加KSCN溶液未见红色的原因是
②取出部分实验一中的橙色溶液,久置不褪色。结合资料a中过程ii分析实验一中溶液最终“几乎无色”的原因:
总结:SO2与K2FeO4发生了氧化还原反应和复分解反应,并且遵循化学反应速率和限度规律。
您最近半年使用:0次
5 . 对下列实验操作、现象及解释或结论均正确的是
| 选项 | 操作 | 现象 | 解释(或结论) |
| A | 稀盐酸滴加到石灰石中,产生的气体通过盛有饱和 溶液的洗气瓶后再通入到 溶液的洗气瓶后再通入到 溶液中 溶液中 | 石灰石表面产生气泡, 溶液中出现白色沉淀 | 非金属性: |
| B | 将某无色晶体溶解于稀盐酸中酸化,所得澄清溶液中再滴加 溶液 溶液 | 澄清溶液中出现白色沉淀 | 原无色晶体中含有 |
| C | 某无色溶液中滴加浓NaOH溶液,加热,湿润的红色石蕊试纸靠近试管口 | 湿润的红色石蕊试纸变蓝 | 原无色溶液不一定是铵盐溶液 |
| D | 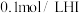 溶液中滴加几滴淀粉试剂,再滴加几滴 溶液中滴加几滴淀粉试剂,再滴加几滴  溶液 溶液 | 溶液出现蓝色 | 氧化性: |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
解题方法
6 . 某小组设计实验探究氯气的性质,装置如图所示:
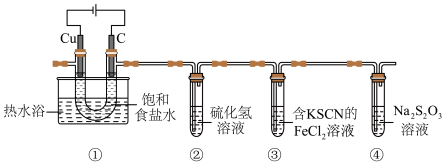
实验中观察到③中溶液先变红色,后褪色。
资料显示:④中反应为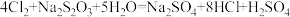
下到叙述错误的是

实验中观察到③中溶液先变红色,后褪色。
资料显示:④中反应为
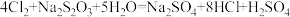
下到叙述错误的是
A.铜极附近逸出气泡,其溶液 升高 升高 |
| B.②中溶液变浑浊,可推知氯的非金属性比硫的强 |
C.取③中溶液,滴加 溶液可判断 溶液可判断 是否被氧化 是否被氧化 |
D.用硝酸酸化的 溶液可验证④中是否生成了 溶液可验证④中是否生成了 |
您最近半年使用:0次
名校
解题方法
7 . 实验小组探究溶液酸碱性对锰化合物和 ,氧化还原反应的影响。
,氧化还原反应的影响。
资料:i. 呈绿色,
呈绿色, 为棕黑色沉淀,
为棕黑色沉淀, 几乎无色。
几乎无色。
ii. 在强碱性溶液中能稳定存在,在酸性、中性或弱碱性溶液中易转化为
在强碱性溶液中能稳定存在,在酸性、中性或弱碱性溶液中易转化为 和
和 。
。
iii. 为微溶物。
为微溶物。
(1)用离子方程式解释实验I中出现乳白色浑浊的原因________________________ 。
(2)已知,实验I、II、III中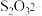 均被氧化为
均被氧化为 ,针对实验I、II、III进行分析:
,针对实验I、II、III进行分析:
①对于 氧化性的认识是
氧化性的认识是____________ 。
②实验Ⅱ所得溶液中 的检验方法为
的检验方法为________________________ 。
(3)针对实验Ⅲ、Ⅳ进行分析:
①实验Ⅲ中“溶液变为绿色”相应反应的离子方程式为____________ 。
②实验IV中“静置5min,有棕黑色沉淀生成”的可能原因:____________ (写出2点)。
(4)针对实验Ⅲ、Ⅳ继续探究:
①实验V:向实验III的试管中继续滴加足量 ,振荡,溶液立即变为紫红色,产生棕黑色沉淀。
,振荡,溶液立即变为紫红色,产生棕黑色沉淀。
②实验VI:向实验IV的试管中继续滴加足量 ,振荡,绿色溶液迅速变为无色,棕黑色沉淀逐渐减少直至消失,静置一段时间后,出现乳白色浑浊。
,振荡,绿色溶液迅速变为无色,棕黑色沉淀逐渐减少直至消失,静置一段时间后,出现乳白色浑浊。
对比实验V、VI,结合方程式分析实验VI滴加 后溶液未见紫红色的可能原因
后溶液未见紫红色的可能原因____________ 。
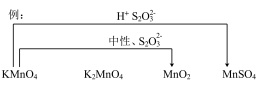
(5)综合上述实验,在下图中用连线的方式补充完善实验I~VI已证实的锰化合物转化关系_____________ 。
 ,氧化还原反应的影响。
,氧化还原反应的影响。资料:i.
 呈绿色,
呈绿色, 为棕黑色沉淀,
为棕黑色沉淀, 几乎无色。
几乎无色。ii.
 在强碱性溶液中能稳定存在,在酸性、中性或弱碱性溶液中易转化为
在强碱性溶液中能稳定存在,在酸性、中性或弱碱性溶液中易转化为 和
和 。
。iii.
 为微溶物。
为微溶物。实验 | 序号 | 试剂 | 现象 |
| I | a:10滴 溶液 溶液b:20滴 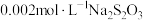 溶液 溶液 | 溶液紫色变浅至接近无色,静置一段时间后出现乳白色浑浊 |
II | a:10滴蒸馏水 b:20滴 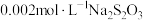 溶液 溶液 | 紫色溶液逐渐褪色,产生棕黑色沉淀 | |
III | a:10滴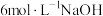 溶液 溶液b:2滴 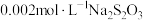 溶液和18滴蒸馏水 溶液和18滴蒸馏水 | 溶液变为绿色,无沉淀生成;静置5min,未见明显变化 | |
IV | a:10滴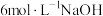 溶液 溶液b:20滴 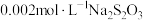 溶液 溶液 | 溶液变为绿色,无沉淀生成;静置5min,绿色变浅,有棕黑色沉淀生成 |
(1)用离子方程式解释实验I中出现乳白色浑浊的原因
(2)已知,实验I、II、III中
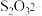 均被氧化为
均被氧化为 ,针对实验I、II、III进行分析:
,针对实验I、II、III进行分析:①对于
 氧化性的认识是
氧化性的认识是②实验Ⅱ所得溶液中
 的检验方法为
的检验方法为(3)针对实验Ⅲ、Ⅳ进行分析:
①实验Ⅲ中“溶液变为绿色”相应反应的离子方程式为
②实验IV中“静置5min,有棕黑色沉淀生成”的可能原因:
(4)针对实验Ⅲ、Ⅳ继续探究:
①实验V:向实验III的试管中继续滴加足量
 ,振荡,溶液立即变为紫红色,产生棕黑色沉淀。
,振荡,溶液立即变为紫红色,产生棕黑色沉淀。②实验VI:向实验IV的试管中继续滴加足量
 ,振荡,绿色溶液迅速变为无色,棕黑色沉淀逐渐减少直至消失,静置一段时间后,出现乳白色浑浊。
,振荡,绿色溶液迅速变为无色,棕黑色沉淀逐渐减少直至消失,静置一段时间后,出现乳白色浑浊。对比实验V、VI,结合方程式分析实验VI滴加
 后溶液未见紫红色的可能原因
后溶液未见紫红色的可能原因(5)综合上述实验,在下图中用连线的方式补充完善实验I~VI已证实的锰化合物转化关系
您最近半年使用:0次
2024-02-29更新
|
210次组卷
|
2卷引用:北京市第一七一中学2023-2024学年高三下学期开学考试化学试题
8 . 以 溶液和不同金属的盐溶液作为实验对象,探究
溶液和不同金属的盐溶液作为实验对象,探究 的性质和盐溶液间反应的多样性。
的性质和盐溶液间反应的多样性。
【查阅资料】
① 能与多种不同金属离子形成沉淀或配合物:
能与多种不同金属离子形成沉淀或配合物:
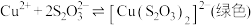 ,
,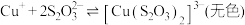
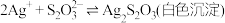 ,
,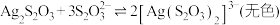
② 易被氧化为
易被氧化为 或者
或者
【进行实验】
Ⅰ.探究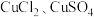 和
和 溶液之间的反应
溶液之间的反应
(1)经检验,实验a绿色变浅后的溶液中含 ,这说明
,这说明 具有
具有_______ (填“氧化”或“还原”)性。
(2)从反应速率和化学平衡两个角度解释实验a的实验现象_______ 。
II.探究 和
和 溶液之间的反应。
溶液之间的反应。
(3)实验c中产生的白色沉淀为 ,用化学用语解释“超过
,用化学用语解释“超过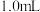 后,产生少量白色沉淀”的原因:
后,产生少量白色沉淀”的原因:_______ 。
(4)为了探究实验c中产生黑色沉淀的原因,甲同学进行了进一步的实验:
ⅰ.取少量滤液B,用广泛pH试纸测定 ;
;
ⅱ.另取少量滤液B于试管中,_______ (填操作和现象),说明滤液中有 。
。
由上述实验现象,进而推测出黑色沉淀A可能为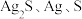 或它们的混合物。运用氧化还原反应规律,做出该推测的理由是
或它们的混合物。运用氧化还原反应规律,做出该推测的理由是_______ 。
【获得结论】
(5)根据上述实验, 和金属盐溶液之间反应的多样性与多种因素有关:①
和金属盐溶液之间反应的多样性与多种因素有关:①_______ :②金属盐中的阴离子是否能够参与反应;③反应时间的长短;④_______ 。
 溶液和不同金属的盐溶液作为实验对象,探究
溶液和不同金属的盐溶液作为实验对象,探究 的性质和盐溶液间反应的多样性。
的性质和盐溶液间反应的多样性。| 实验 试管 | 试剂滴管:逐滴滴加,总体积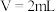 | 现象 |
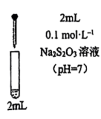 | 实验a: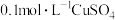 溶液 溶液实验b: 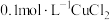 溶液 溶液 | 溶液先变为绿色,静止后缓慢变浅,最终变为浅绿色 溶液先变为绿色,缓慢产生白色浑浊,充分反应后绿色比实验a更浅 |
实验c: 溶液 溶液 | 生成白色沉淀,振荡后迅速溶解,得到无色清液;超过1.0mL后,产生少量白色沉淀,立即变为棕黄色,最终变为黑色,静置充分反应后,过滤得到黑色沉淀A和滤液B |
①
 能与多种不同金属离子形成沉淀或配合物:
能与多种不同金属离子形成沉淀或配合物: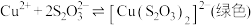 ,
,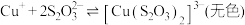
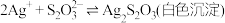 ,
,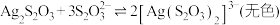
②
 易被氧化为
易被氧化为 或者
或者
【进行实验】
Ⅰ.探究
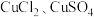 和
和 溶液之间的反应
溶液之间的反应(1)经检验,实验a绿色变浅后的溶液中含
 ,这说明
,这说明 具有
具有(2)从反应速率和化学平衡两个角度解释实验a的实验现象
II.探究
 和
和 溶液之间的反应。
溶液之间的反应。(3)实验c中产生的白色沉淀为
 ,用化学用语解释“超过
,用化学用语解释“超过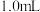 后,产生少量白色沉淀”的原因:
后,产生少量白色沉淀”的原因:(4)为了探究实验c中产生黑色沉淀的原因,甲同学进行了进一步的实验:
ⅰ.取少量滤液B,用广泛pH试纸测定
 ;
;ⅱ.另取少量滤液B于试管中,
 。
。由上述实验现象,进而推测出黑色沉淀A可能为
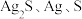 或它们的混合物。运用氧化还原反应规律,做出该推测的理由是
或它们的混合物。运用氧化还原反应规律,做出该推测的理由是【获得结论】
(5)根据上述实验,
 和金属盐溶液之间反应的多样性与多种因素有关:①
和金属盐溶液之间反应的多样性与多种因素有关:①
您最近半年使用:0次
9 . 通过化学实验现象得出相应的结论是探究物质性质的一种重要方法,下列实验操作和现象或结论不正确的是
| 选项 | 实验操作和现象 | 结论 |
| A | 向包有足量过氧化钠粉末的脱脂棉上滴加几滴水,脱脂棉燃烧 | 过氧化钠与水反应放热 |
| B | 向某未知溶液(不含 )中加入足量硝酸酸化的硝酸银溶液,无气体产生,但有白色沉淀出现 )中加入足量硝酸酸化的硝酸银溶液,无气体产生,但有白色沉淀出现 | 未知溶液中含有Cl-,一定不 或 或 |
| C | 用铂丝蘸取少量未知固体化合物做焰色试验,火焰呈黄色 | 固体中一定含Na+,可能含K+ |
| D | 向某溶液中加入盐酸酸化的BaCl2溶液,有白色沉淀 | 溶液中一定含有 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2024-02-25更新
|
370次组卷
|
2卷引用:湖南省长沙市长沙县第一中学2023-2024学年高一下学期开学化学试题
2024高二·全国·专题练习
10 . ZnO是电镀、涂料、有机合成等化学工业的重要原料。某课题组设计由含锌工业废料(含Fe、Cu、Mn等杂质)生产ZnO的工艺流程如下:
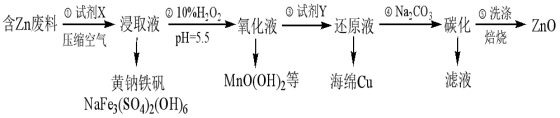
已知:黄钠铁矾在pH为1.5,温度为90℃时完全沉淀,且易于过滤。
(1)试剂X为Na2SO4和___________ 的混合液,步骤①的浸取液里除含有Cu2+、Mn2+以外,还含有的金属离子有___________ ,写出Cu溶解变为Cu2+离子方程式___________ 。
(2)步骤②可进一步氧化除铁,还氧化除去了Mn2+,试写出相应的除去Mn2+的离子方程式___________ 。
(3)步骤③加入试剂Y的目的是置换出Cu,则Y的化学式为___________ ,整个工艺流程中可以循环使用的试剂是___________ 。
(4)步骤⑤中检验沉淀是否洗涤干净的操作方法是___________ 。
(5)步骤④碳化实际得到的是一种碱式碳酸锌[ZnCO3·xZn(OH)2·yH2O],取该样品6.82g,充分灼烧后测得残留物质量为4.86g,将所得气体通入足量澄清石灰水中,得到2.00g沉淀,则此碱式碳酸锌的化学式是___________ 。

已知:黄钠铁矾在pH为1.5,温度为90℃时完全沉淀,且易于过滤。
(1)试剂X为Na2SO4和
(2)步骤②可进一步氧化除铁,还氧化除去了Mn2+,试写出相应的除去Mn2+的离子方程式
(3)步骤③加入试剂Y的目的是置换出Cu,则Y的化学式为
(4)步骤⑤中检验沉淀是否洗涤干净的操作方法是
(5)步骤④碳化实际得到的是一种碱式碳酸锌[ZnCO3·xZn(OH)2·yH2O],取该样品6.82g,充分灼烧后测得残留物质量为4.86g,将所得气体通入足量澄清石灰水中,得到2.00g沉淀,则此碱式碳酸锌的化学式是
您最近半年使用:0次