名校
解题方法
1 . 下列物质的性质与用途具有对应关系的是
| A.H2S具有还原性,可除去废水中的Hg2+ |
| B.HNO3具有强氧化性,可用于制NH4NO3 |
| C.Al(OH)3胶体具有吸附性,可用于净水 |
| D.NaClO溶液呈碱性,可用于杀菌消毒 |
您最近一年使用:0次
名校
解题方法
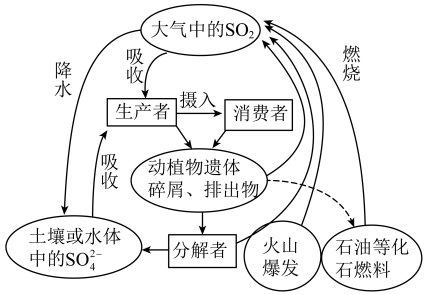
2 . 硫是生物必需的大量营养元素之一,下图是自然界中硫的循环图,在循环过程中S的价态变化在-2价至+6价之间,请分析此图并回答有关问题:______ 。
A.硫化氢分子很稳定,受热难分解
B.硫化氢分子中所有原子的最外层都达到8电子结构
C.将硫化氢通入硫酸亚铁溶液,产生沉淀
D.硫化氢中硫元素为-2价,因此只有还原性,没有氧化性
E.硫化氢可在空气中燃烧生成二氧化硫
(2)大中的SO2经过一系列转化最终生成H2SO4,导致降水具有较强酸性,称为酸雨。收集某次酸雨样品,发现8小时内,样品pH一直在减小,其原因可能是___________ (用化学方程式表示)。
(3)研究发现,空气中少量的NO2也能参与硫酸型酸雨的形成,反应过程如下:
①SO+NO2→SO3+NO ②SO3+H2O→H2SO4 ③2NO+O2→2NO2
NO2在上述过程中的作用,与H2SO4在下列变化中的作用不符的是___________。
(4)在制葡萄酒时可以人工添加SO2,有两个目的:抗氧化和抗菌,实验室模拟二氧化硫抗氧化过程,向溴水中通入SO2,请用离子方程式表示该反应原理___________ 。发酵酒卫生标准中对葡萄酒中的二氧化硫含量有要求:总SO2小于250mg/L,若在室温下。每升溶液中最多通入___________ mL SO2.(室温下Vm=24.5L/mol,结果保留3位有效数字,体积变化忽略不计)
(5)明代《徐光启手迹》记载了用硫酸盐制备硝酸的方法,其主要流程(部分产物已省略)如下:___________ 。
②关于整个制备过程,下列说法正确的是___________ 。
A.本流程涉及复分解反应
B.由H2SO4制HNO3利用了强酸制弱酸原理
C.制备使用的铁锅易损坏
(6)工业上为了防止制硫酸过程中产生污染,可以利用氧化亚铁硫杆菌(T·f)对硫铁矿进行催化脱硫,该过程如图所示:___________ 。
②脱硫过程中产生的 在酸性溶液中会形成淡黄色沉淀并产生刺激性气味的气体,写出其离子方程式
在酸性溶液中会形成淡黄色沉淀并产生刺激性气味的气体,写出其离子方程式___________ 。
③从氧化还原角度分析,若要制备Na2S2O3应选择___________ (填字母)。
A.SO2+Na2SO4 B.Na2S+S C.Na2SO3+Na2SO4 D.Na2SO3+S
A.硫化氢分子很稳定,受热难分解
B.硫化氢分子中所有原子的最外层都达到8电子结构
C.将硫化氢通入硫酸亚铁溶液,产生沉淀
D.硫化氢中硫元素为-2价,因此只有还原性,没有氧化性
E.硫化氢可在空气中燃烧生成二氧化硫
(2)大中的SO2经过一系列转化最终生成H2SO4,导致降水具有较强酸性,称为酸雨。收集某次酸雨样品,发现8小时内,样品pH一直在减小,其原因可能是
(3)研究发现,空气中少量的NO2也能参与硫酸型酸雨的形成,反应过程如下:
①SO+NO2→SO3+NO ②SO3+H2O→H2SO4 ③2NO+O2→2NO2
NO2在上述过程中的作用,与H2SO4在下列变化中的作用不符的是___________。
| A.潮湿的氯气通过盛有浓H2SO4的洗气瓶 |
| B.硫化氢通入浓H2SO4中 |
| C.浓H2SO4滴入萤石中,加热 |
| D.向盐酸中加入浓硫酸产生白雾 |
(4)在制葡萄酒时可以人工添加SO2,有两个目的:抗氧化和抗菌,实验室模拟二氧化硫抗氧化过程,向溴水中通入SO2,请用离子方程式表示该反应原理
(5)明代《徐光启手迹》记载了用硫酸盐制备硝酸的方法,其主要流程(部分产物已省略)如下:

②关于整个制备过程,下列说法正确的是
A.本流程涉及复分解反应
B.由H2SO4制HNO3利用了强酸制弱酸原理
C.制备使用的铁锅易损坏
(6)工业上为了防止制硫酸过程中产生污染,可以利用氧化亚铁硫杆菌(T·f)对硫铁矿进行催化脱硫,该过程如图所示:
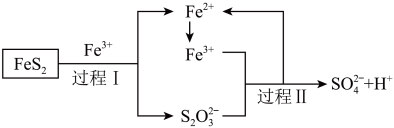
②脱硫过程中产生的
 在酸性溶液中会形成淡黄色沉淀并产生刺激性气味的气体,写出其离子方程式
在酸性溶液中会形成淡黄色沉淀并产生刺激性气味的气体,写出其离子方程式③从氧化还原角度分析,若要制备Na2S2O3应选择
A.SO2+Na2SO4 B.Na2S+S C.Na2SO3+Na2SO4 D.Na2SO3+S
您最近一年使用:0次
解题方法
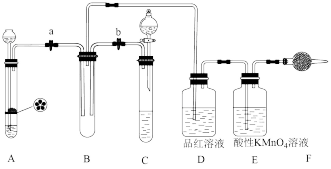
3 . 某课外学习小组的同学设计了如图所示的实验装置(夹持装置略),以验证 的氧化性、还原性和漂白性。
的氧化性、还原性和漂白性。
请回答下列问题:
(1)用Na2SO3固体和70%的浓硫酸反应制取SO2气体,应选用____________ (填“A”或“C”)装置作气体发生装置,不选用另一装置的理由是_______________________________ 。
(2)该课外学习小组的同学用FeS固体和稀硫酸反应制取H2S气体,反应的化学方程式为___________________________ 。
(3)SO2气体通过D装置时的现象是___________________________ ,通过E装置时的现象是__________________________ ;SO2与H2S在B装置中反应,现象是__________________________ 。
(4)F装置中盛有碱石灰,其作用是_______________________________ 。
 的氧化性、还原性和漂白性。
的氧化性、还原性和漂白性。请回答下列问题:
(1)用Na2SO3固体和70%的浓硫酸反应制取SO2气体,应选用
(2)该课外学习小组的同学用FeS固体和稀硫酸反应制取H2S气体,反应的化学方程式为
(3)SO2气体通过D装置时的现象是
(4)F装置中盛有碱石灰,其作用是

您最近一年使用:0次
名校
解题方法
4 . 根据下列实验操作和现象,得出的结论错误的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 向酸性高锰酸钾溶液中滴入 溶液 溶液 | 溶液褪色 | 证明 具有还原性 具有还原性 |
| B | 向氢硫酸溶液中滴入 溶液 溶液 | 产生黄色沉淀 | 证明 具有氧化性 具有氧化性 |
| C | 向 溶液中滴入酸化的 溶液中滴入酸化的 溶液 溶液 | 溶液变为黄色 | 证明氧化性: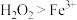 |
| D | 向NaClO溶液中滴入 溶液,并在试管口放置带火星的木条 溶液,并在试管口放置带火星的木条 | 木条复燃 | 证明还原性: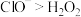 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-10-09更新
|
109次组卷
|
2卷引用:黑龙江省哈尔滨市第九中学校2022一2023学年高一上学期9月份考试化学试题
名校
解题方法
5 . 硫是生物必需的大量营养元素之一,下图是自然界中硫的循环图,请分析此图并回答有关问题。
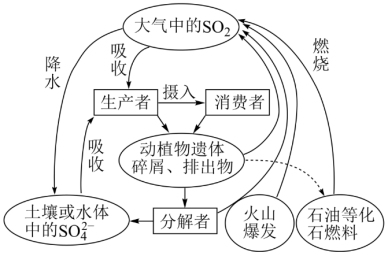
(1)氮循环和硫循环是自然界中两种重要的元素循环过程,下列关于这两种循环的说法正确的是________ 。
(2)分解者可将含硫有机物分解为H2S,硫磺细菌和硫化细菌可将H2S进一步变为硫单质或硫酸盐,下列关于硫化氢说法正确的是_______ 。
A.H2S分子很稳定,受热难分解
B. H2S分子中所有原子的最外层都达到8电子结构
C.将H2S通入FeSO4溶液,产生沉淀
D.H2S中硫元素为-2价,因此H2S只有还原性,没有氧化性
E.H2S是一种无色臭鸡蛋气味的有毒气体
(3)大气中的SO2经过一系列转化最终生成H2SO4,导致降水具有较强酸性,称为酸雨。检验某次降雨是否为酸雨的方法是_________________ ,收集某次酸雨样品,发现8小时内,样品pH一直在减小,其原因可能是________________ 。(用化学方程式表示)
(4)为了防治酸雨,工业上常采用“钙基固硫法”即将生石灰和含硫的煤混合后燃烧,燃烧时硫、氧气和生石灰共同作用,使硫元素转移到炉渣中,大部分硫元素最终转化为固体盐是_______ (填化学式)。

(1)氮循环和硫循环是自然界中两种重要的元素循环过程,下列关于这两种循环的说法正确的是
| 选项 | 比较 | 氮循环 | 硫循环 |
| A | 异 | 氮元素会进入大气 | 硫元素不会进入大气 |
| B | 氮循环过程有生物圈参与 | 硫循环过程无生物圈参与 | |
| C | 同 | 人类活动对氮循环和硫循环都造成巨大影响 | |
| D | 氮循环和硫循环对环境的影响是都能导致温室效应 | ||
A.H2S分子很稳定,受热难分解
B. H2S分子中所有原子的最外层都达到8电子结构
C.将H2S通入FeSO4溶液,产生沉淀
D.H2S中硫元素为-2价,因此H2S只有还原性,没有氧化性
E.H2S是一种无色臭鸡蛋气味的有毒气体
(3)大气中的SO2经过一系列转化最终生成H2SO4,导致降水具有较强酸性,称为酸雨。检验某次降雨是否为酸雨的方法是
(4)为了防治酸雨,工业上常采用“钙基固硫法”即将生石灰和含硫的煤混合后燃烧,燃烧时硫、氧气和生石灰共同作用,使硫元素转移到炉渣中,大部分硫元素最终转化为固体盐是
您最近一年使用:0次
6 . 关于硫化氢气体在空气中完全燃烧的产物,叙述正确的是( )
①具有臭鸡蛋气味的气体;②是淡黄色的固体;③它能使溴水褪色;④它的水溶液具有酸性;⑤它具有氧化性和还原性。
①具有臭鸡蛋气味的气体;②是淡黄色的固体;③它能使溴水褪色;④它的水溶液具有酸性;⑤它具有氧化性和还原性。
| A.只有② | B.只有③ | C.①和④ | D.③、④和⑤ |
您最近一年使用:0次
2018-12-24更新
|
143次组卷
|
2卷引用:云南省元江县一中2018-2019学年高一上学期12月考试化学试题
7 . 硫化氢能与二氧化硫反应,说明硫化氢具有
| A.还原性 | B.氧化性 | C.酸性 | D.不稳定性 |
您最近一年使用:0次
2018-04-17更新
|
286次组卷
|
3卷引用:安徽省安庆市九一六学校2020—2021学年高一4月月考化学试题
名校
8 . 用化学用语表示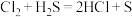 中的相关微粒,其中正确的是
中的相关微粒,其中正确的是
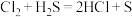 中的相关微粒,其中正确的是
中的相关微粒,其中正确的是A.中子数为1的氢原子: | B. 的结构示意图: 的结构示意图: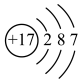 |
C. 中S元素的化合价: 中S元素的化合价: | D.单质S既有氧化性又有还原性 |
您最近一年使用:0次
名校
9 . 硒 单质及化合物与硫单质及化合物性质类似,则下列说法中错误的是
单质及化合物与硫单质及化合物性质类似,则下列说法中错误的是
 单质及化合物与硫单质及化合物性质类似,则下列说法中错误的是
单质及化合物与硫单质及化合物性质类似,则下列说法中错误的是A. 有毒,能在空气中燃烧 有毒,能在空气中燃烧 |
B. 通入 通入 溶液中,无明显现象 溶液中,无明显现象 |
C. 可被 可被 溶液吸收 溶液吸收 |
| D.SeO2既有氧化性,又有还原性 |
您最近一年使用:0次
2022-01-25更新
|
262次组卷
|
3卷引用:山东省威海市2021-2022学年高一上学期期末考试化学试题
名校
10 . 下列事实与括号中物质的性质对应关系正确的是
| A.浓硝酸敞口放置于空气中密度减小(硝酸有强氧化性) |
| B.NO暴露于空气中变红棕色(NO有氧化性) |
| C.氢硫酸久置时变浑浊(H2S有还原性) |
| D.光照甲烷与氯气混合气体时,气体颜色变浅(甲烷有可燃性) |
您最近一年使用:0次
2021-08-17更新
|
622次组卷
|
2卷引用:广东省惠州市2020-2021学年高一下学期期末考试化学试题



