名校
解题方法
1 . 阅读下列科普短文并填空:海水中含有多种盐类,如 、
、 等。目前,通过海水晒盐可制得食盐晶体和苦卤,食盐精制后可制成饱和
等。目前,通过海水晒盐可制得食盐晶体和苦卤,食盐精制后可制成饱和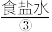 用以生产
用以生产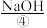 、
、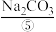 、
、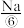 、
、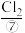 、
、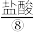 等,经过氯气氧化,热空气吹出、
等,经过氯气氧化,热空气吹出、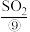 吸收等一系列操作可获得 Br2。
吸收等一系列操作可获得 Br2。
(1)上述标有序号的物质中属于电解质的是___________ (填序号, 下同);属于非电解质的是___________ ; 能导电的物质是___________ 。
(2)写出⑤溶于水的电离方程式:___________ 。 将少量的⑤溶于装有50mL蒸馏水的烧杯中后,逐滴加入⑧观察到刚开始并没有出现气泡,一段时间后出现气泡,则出现该现象的原因是___________ , 写出对应反应的离子方程式;___________ ,___________ 。
(3)海水提溴的过程中涉及的反应有2Br- +Cl2=Br2 +2Cl-, 2H2O+SO2+Br2=4H+ +2Br- +SO ,根据上述反应可判断Cl-、Br-、 SO2的还原性由强到弱的顺序为
,根据上述反应可判断Cl-、Br-、 SO2的还原性由强到弱的顺序为___________ 。
 、
、 等。目前,通过海水晒盐可制得食盐晶体和苦卤,食盐精制后可制成饱和
等。目前,通过海水晒盐可制得食盐晶体和苦卤,食盐精制后可制成饱和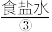 用以生产
用以生产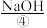 、
、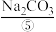 、
、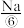 、
、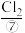 、
、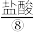 等,经过氯气氧化,热空气吹出、
等,经过氯气氧化,热空气吹出、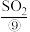 吸收等一系列操作可获得 Br2。
吸收等一系列操作可获得 Br2。(1)上述标有序号的物质中属于电解质的是
(2)写出⑤溶于水的电离方程式:
(3)海水提溴的过程中涉及的反应有2Br- +Cl2=Br2 +2Cl-, 2H2O+SO2+Br2=4H+ +2Br- +SO
 ,根据上述反应可判断Cl-、Br-、 SO2的还原性由强到弱的顺序为
,根据上述反应可判断Cl-、Br-、 SO2的还原性由强到弱的顺序为
您最近一年使用:0次
20-21高二上·江西南昌·期中
2 . 下表是25℃时某些弱酸的电离常数,其中多元弱酸分步电离。
(1)根据表中数据判断下述反应可以发生的是__ (填编号)。
①NaF+CH3COOH=CH3COONa+HF
②HF+NaHCO3=NaF+H2O+CO2↑
③CH3COOH+K2C2O4=CH3COOK+KHC2O4
(2)少量CO2通入NaClO溶液中发生反应的离子方程式为__ 。
(3)常温下在20mL0.1mol/LNa2CO3溶液中逐滴滴加40mL0.1mol/L盐酸溶液,溶液中含碳元素的三种微粒H2CO3、HCO 、CO
、CO (CO2因逸出未画出)物质的量分数(纵轴)随溶液pH变化的部分情况如图所示。
(CO2因逸出未画出)物质的量分数(纵轴)随溶液pH变化的部分情况如图所示。

问答下列问题:
①各字母代表的粒子为b__ ,c___ 。
②在同一溶液中,H2CO3、HCO 、CO
、CO (填“能“或“不能”)
(填“能“或“不能”)___ 大量共存。
| 弱酸 | K | 弱酸 | K |
| HF | 3.52×10-4 | H2CO3 | K1=4.4×10-7 |
| HClO | 2.95×10-8 | K2=4.7×10-11 | |
| HCOOH | 1.765×10-4 | H2C2O4 | K1=5.4×10-2 |
| CH3COOH | 1.753×10-5 | K2=5.4×10-5 |
①NaF+CH3COOH=CH3COONa+HF
②HF+NaHCO3=NaF+H2O+CO2↑
③CH3COOH+K2C2O4=CH3COOK+KHC2O4
(2)少量CO2通入NaClO溶液中发生反应的离子方程式为
(3)常温下在20mL0.1mol/LNa2CO3溶液中逐滴滴加40mL0.1mol/L盐酸溶液,溶液中含碳元素的三种微粒H2CO3、HCO
 、CO
、CO (CO2因逸出未画出)物质的量分数(纵轴)随溶液pH变化的部分情况如图所示。
(CO2因逸出未画出)物质的量分数(纵轴)随溶液pH变化的部分情况如图所示。
问答下列问题:
①各字母代表的粒子为b
②在同一溶液中,H2CO3、HCO
 、CO
、CO (填“能“或“不能”)
(填“能“或“不能”)
您最近一年使用:0次
名校
解题方法
3 . 按要求答题
I.NaNO2 因外观和食盐相似,又有咸味,容易使人误食中毒。已知 NaNO2能发生反应:2NaNO2+4HI=2NO↑+I2+2NaI+2H2O。
(1)上述反应中氧化剂是________ 。
(2)根据上述反应,鉴别 NaNO2 和 NaCl。可选用的物质有①水、②碘化钾淀粉试纸③淀粉、④白酒、⑤食醋,你认为必须选用的物质有________ (填序号)。
(3)请配平以下化学方程式:____Al+____NaNO3+____ NaOH= ____NaAlO2+____ N2↑+___H2O,________________ ,若反应过程中转移 5 mol 电子,则生成标准状况下 N2 的体积为_________ L。
II.向100mL1.5mol/L 的氢氧化钠溶液中缓慢通入一定量的CO2,反应后,向所得溶液中逐滴缓慢滴加一定浓度的盐酸,所得气体的体积与所加盐酸的体积(不考虑气体溶解于水)关系如图所示。

则:①氢氧化钠溶液与一定量的CO2 充分反应后的溶液中溶质为____ (写化学式)。
②盐酸的浓度为_______ 。
③B点时,产生的气体在标准状况下的体积为_______ L。
I.NaNO2 因外观和食盐相似,又有咸味,容易使人误食中毒。已知 NaNO2能发生反应:2NaNO2+4HI=2NO↑+I2+2NaI+2H2O。
(1)上述反应中氧化剂是
(2)根据上述反应,鉴别 NaNO2 和 NaCl。可选用的物质有①水、②碘化钾淀粉试纸③淀粉、④白酒、⑤食醋,你认为必须选用的物质有
(3)请配平以下化学方程式:____Al+____NaNO3+____ NaOH= ____NaAlO2+____ N2↑+___H2O,
II.向100mL1.5mol/L 的氢氧化钠溶液中缓慢通入一定量的CO2,反应后,向所得溶液中逐滴缓慢滴加一定浓度的盐酸,所得气体的体积与所加盐酸的体积(不考虑气体溶解于水)关系如图所示。

则:①氢氧化钠溶液与一定量的CO2 充分反应后的溶液中溶质为
②盐酸的浓度为
③B点时,产生的气体在标准状况下的体积为
您最近一年使用:0次
2019-02-05更新
|
502次组卷
|
3卷引用:江西省上饶市“山江湖”协作体2019-2020学年高一上学期期中联考化学(自主班)试题



