名校
解题方法
1 . 纯碱是重要的生活用碱和化工原料,用途广泛。请同学们按要求回答问题。
Ⅰ.纯碱生产:我国化学家侯德榜改革国外的纯碱生产工艺,其生产流程可简要表示如下。
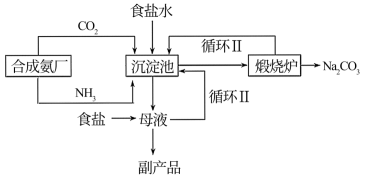
(1)请写出煅烧炉中发生反应的化学方程式:___________ 。
(2)侯氏制碱的创新之处:根据NH4Cl在常温时的溶解度比NaCl大,而在低温下却比NaCl溶解度小的原理,在5℃~10℃时,向母液中加入食盐细粉,而使NH4Cl单独结晶析出供做氮肥,大大提高了原料利用率、降低了生产成本,为世界制碱业做出了巨大贡献。依据上述信息可知,副产品的成分为___________ ,循环Ⅰ中物质的主要成分是___________ 。(本小题涉及到的物质均写化学式)
Ⅱ.产品纯度的测定:上述生产中获得的纯碱产品中含有少量NaCl杂质,为测定该样品中纯碱的质量分数,可用如图所示的装置进行实验。
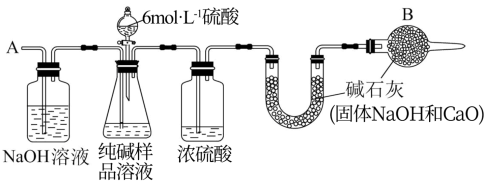
主要实验步骤如下:
①按如图所示装置来组装仪器,并检查装置的气密性;
②将a g纯碱样品放入锥形瓶中,加入适量蒸馏水溶解,得到纯碱样品溶液;
③称量盛有碱石灰的U形管的质量为b g;
④通过分液漏斗滴入6 mol·L-1的硫酸,直到不再产生气体为止;
⑤从导管A处缓缓鼓入一定量的空气;
⑥再次称量盛有碱石灰的U形管的质量为c g;
⑦重复步骤⑤和⑥的操作,直到U形管的质量基本不变,为d g.
请回答下列问题:
(3)装置中干燥管B的作用是___________ 。
(4)从A处通入的空气如果不经过NaOH溶液,测量结果将___________ (填“偏高”、“偏低”或“不变”)。
(5)步骤⑤的目的是___________ 。
(6)步骤⑦的目的是___________ 。
(7)该样品中纯碱的质量分数的计算式为___________ 。
(8)如果所得产品中除含有少量NaCl杂质外还含有少量NaHCO3杂质,下列实验方案中能测定出产品中纯碱的质量分数的是___________ 。
A.取a g产品充分加热,质量减少b g。
B.取a g产品与足量Ba(OH)2溶液反应,过滤、洗涤、干燥,得到b g固体。
C.取a g产品与足量BaCl2溶液反应,过滤、洗涤、干燥,得到b g固体。
Ⅰ.纯碱生产:我国化学家侯德榜改革国外的纯碱生产工艺,其生产流程可简要表示如下。

(1)请写出煅烧炉中发生反应的化学方程式:
(2)侯氏制碱的创新之处:根据NH4Cl在常温时的溶解度比NaCl大,而在低温下却比NaCl溶解度小的原理,在5℃~10℃时,向母液中加入食盐细粉,而使NH4Cl单独结晶析出供做氮肥,大大提高了原料利用率、降低了生产成本,为世界制碱业做出了巨大贡献。依据上述信息可知,副产品的成分为
Ⅱ.产品纯度的测定:上述生产中获得的纯碱产品中含有少量NaCl杂质,为测定该样品中纯碱的质量分数,可用如图所示的装置进行实验。

主要实验步骤如下:
①按如图所示装置来组装仪器,并检查装置的气密性;
②将a g纯碱样品放入锥形瓶中,加入适量蒸馏水溶解,得到纯碱样品溶液;
③称量盛有碱石灰的U形管的质量为b g;
④通过分液漏斗滴入6 mol·L-1的硫酸,直到不再产生气体为止;
⑤从导管A处缓缓鼓入一定量的空气;
⑥再次称量盛有碱石灰的U形管的质量为c g;
⑦重复步骤⑤和⑥的操作,直到U形管的质量基本不变,为d g.
请回答下列问题:
(3)装置中干燥管B的作用是
(4)从A处通入的空气如果不经过NaOH溶液,测量结果将
(5)步骤⑤的目的是
(6)步骤⑦的目的是
(7)该样品中纯碱的质量分数的计算式为
(8)如果所得产品中除含有少量NaCl杂质外还含有少量NaHCO3杂质,下列实验方案中能测定出产品中纯碱的质量分数的是
A.取a g产品充分加热,质量减少b g。
B.取a g产品与足量Ba(OH)2溶液反应,过滤、洗涤、干燥,得到b g固体。
C.取a g产品与足量BaCl2溶液反应,过滤、洗涤、干燥,得到b g固体。
您最近一年使用:0次
名校
2 . 侯氏制碱法是在索尔维制碱法的基础上创造出的一种新的制造纯碱的方法。具体工艺流程图如下:
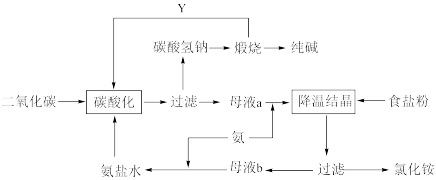
Ⅰ.根据以上流程回答下列问题:
(1)与索尔维制碱法相比,侯氏制碱法最突出的优点是___________
A.原料利用率高 B.设备少 C.生产方便
(2)碳酸化这一步的原理是(用化学方程式表示)___________
(3)侯氏制碱法副产品的一种用途为___________ 。
(4)Y物质是___________ 。
Ⅱ.工业上碳酸钠大多采用侯氏制碱法制取,所得碳酸钠样品中往往含有少的NaCl,现欲测定某碳酸钠样品中 的质量分数,某探究性学习小组取样品b g设计了如下实验方案。
的质量分数,某探究性学习小组取样品b g设计了如下实验方案。
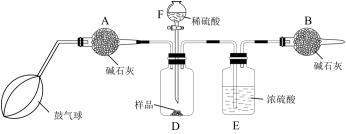
该实验的操作步骤如下:
①如图连接装置(除B外)并加入所需药品。
②称量并记录B的质量( )。
)。
③按动鼓气球,持续约1分钟。
④连接上B。
⑤打开分液漏斗F的活塞,将稀硫酸快速加入D中后,关闭活塞。
⑥按动鼓气球,持续约1分钟。
⑦称量并记录B的质( )。
)。
⑧计算
(5)操作⑥中,鼓入空气的作用是___________ ;
(6)根据题干所给的数据列出样品中 的质量分数表达式
的质量分数表达式___________ 。
(7)经实验发现最终所得的 的质量分数超过100%,其可能的原因是
的质量分数超过100%,其可能的原因是___________ 。

Ⅰ.根据以上流程回答下列问题:
(1)与索尔维制碱法相比,侯氏制碱法最突出的优点是
A.原料利用率高 B.设备少 C.生产方便
(2)碳酸化这一步的原理是(用化学方程式表示)
(3)侯氏制碱法副产品的一种用途为
(4)Y物质是
Ⅱ.工业上碳酸钠大多采用侯氏制碱法制取,所得碳酸钠样品中往往含有少的NaCl,现欲测定某碳酸钠样品中
 的质量分数,某探究性学习小组取样品b g设计了如下实验方案。
的质量分数,某探究性学习小组取样品b g设计了如下实验方案。
该实验的操作步骤如下:
①如图连接装置(除B外)并加入所需药品。
②称量并记录B的质量(
 )。
)。③按动鼓气球,持续约1分钟。
④连接上B。
⑤打开分液漏斗F的活塞,将稀硫酸快速加入D中后,关闭活塞。
⑥按动鼓气球,持续约1分钟。
⑦称量并记录B的质(
 )。
)。⑧计算
(5)操作⑥中,鼓入空气的作用是
(6)根据题干所给的数据列出样品中
 的质量分数表达式
的质量分数表达式(7)经实验发现最终所得的
 的质量分数超过100%,其可能的原因是
的质量分数超过100%,其可能的原因是
您最近一年使用:0次
解题方法
3 . A、B、C、D是钠的重要化合物,有着非常广泛的用途,已知B是常见的供氧剂。其相互转化关系如图所示,回答下列问题:
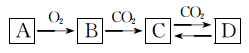
(1)灼烧A、B、C、D四种物质,其焰色为______ 色。
(2)写出 的化学方程式:
的化学方程式:______ 。
(3)等物质的量的A、B分别加入等质量的水中,所得溶液中溶质的质量分数:A______ (填“>”“<”或“=”)B。
(4)不能把等物质的量浓度的C、D鉴别开的是______ (填“澄清石灰水”或“稀盐酸”)。
(5)充分加热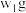 含有D杂质的C样品,若其质量变为
含有D杂质的C样品,若其质量变为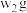 ,则该样品的纯度(质量分数)为
,则该样品的纯度(质量分数)为______ 。

(1)灼烧A、B、C、D四种物质,其焰色为
(2)写出
 的化学方程式:
的化学方程式:(3)等物质的量的A、B分别加入等质量的水中,所得溶液中溶质的质量分数:A
(4)不能把等物质的量浓度的C、D鉴别开的是
(5)充分加热
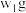 含有D杂质的C样品,若其质量变为
含有D杂质的C样品,若其质量变为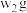 ,则该样品的纯度(质量分数)为
,则该样品的纯度(质量分数)为
您最近一年使用:0次
解题方法
4 . (1)春秋末期工艺官书《考工记》中记载有“涑帛”的方法,即利用含有碳酸钠的水溶液来洗涤丝帛。请写出碳酸钠水溶液中通入CO2气体的化学方程式___________ 。将54.8g Na2CO3和NaHCO3 的混合物分成等量的两份,一份溶于水后加入足量盐酸,收集到气体V L.另一份直接加热至恒重,生成气体2.24L(所有气体体积均在标准状况下测定),则原固体混合物中Na2CO3的物质的量:n(Na2CO3)=____________ ,气体V=___________ 。
(2)现代社会钠及其化合物用途广泛,回答下列问题:
①过氧化钠是重要的供氧剂,与水反应的离子方程式为_____________ ;
②硫代硫酸钠(Na2S2O3)可用做纸浆漂白时的脱氯剂。Na2S2O3中S的化合价是__________ ,该反应利用了硫代硫酸钠的_________ (填“氧化性”或“还原性“)。
(2)现代社会钠及其化合物用途广泛,回答下列问题:
①过氧化钠是重要的供氧剂,与水反应的离子方程式为
②硫代硫酸钠(Na2S2O3)可用做纸浆漂白时的脱氯剂。Na2S2O3中S的化合价是
您最近一年使用:0次



