名校
解题方法
1 . 下列关于Na2CO3与NaHCO3性质的叙述中正确的是
| A.相同条件下,热稳定性:Na2CO3>NaHCO3 |
| B.向Na2CO3与NaHCO3固体加入少量水,均放热 |
| C.用澄清石灰水可以鉴别Na2CO3与NaHCO3溶液 |
| D.与同浓度稀盐酸反应生成气体的速率:Na2CO3>NaHCO3 |
您最近一年使用:0次
2023-01-10更新
|
150次组卷
|
4卷引用:河南省开封五县联考2022-2023学年高一上学期期中考试化学试题
2 . 下列关于Na2CO3和NaHCO3的性质判断错误的是
| A.均溶于水 | B.均为白色固体 | C.受热时均易分解 | D.焰色反应均为黄色 |
您最近一年使用:0次
2023-01-07更新
|
234次组卷
|
2卷引用:2021年河南省普通高中学生学业水平考试化学试题
3 . 某化学兴趣小组为研究用不同膨松剂蒸馒头的效果,在相同条件下依次进行以下四组实验。实验结束后,比较不同实验中所蒸馒头的蓬松度、颜色和口味(碱性增强会使馒头颜色变黄)。下列说法错误的是
| 实验编号 | 1 | 2 | 3 | 4 |
| 所加物质 | 酵头、 | 酵头、 | 酵头、 、适量柠檬酸 、适量柠檬酸 | 1.5g某种酵母 |
| 实验结果 | 硬实、黄色、带碱味 | 较松软、黄色、略带碱味 | 松软、黄色较浅、无碱味 | 松软、颜色正常、无碱味 |
| A.该兴趣小组用到的研究方法有观察法、实验法等 |
| B.实验4中所用酵母为生物膨松剂,使用过程中发生了化学反应 |
C.对比实验1和实验2,可知 和 和 均能单独作为蒸馒头的膨松剂 均能单独作为蒸馒头的膨松剂 |
| D.对比实验2和实验3,可知柠檬酸作用主要是降低馒头的碱性并使馒头更为松软 |
您最近一年使用:0次
名校
解题方法
4 . 某小组通过实验探究 和
和 的性质。
的性质。
实验一:探究 和
和 的溶解性和水溶液的酸碱性。
的溶解性和水溶液的酸碱性。
根据上述实验现象,回答下列问题:
(1)常温下, 的溶解度
的溶解度_______ (填“大于”“小于”或“等于”) 的溶解度。
的溶解度。
(2)下列推断正确的是_______(填字母)。
(3) 溶液和少量盐酸反应生成
溶液和少量盐酸反应生成 ,离子方程式为
,离子方程式为_______ 。
实验二:探究 和
和 的热稳定性。
的热稳定性。

观察到的实验现象如下表所示:
根据上述实验现象,回答下列问题:
(4)加热 时,装置C中产生气泡的原因是
时,装置C中产生气泡的原因是_______ 。
(5)实验结论是_______ 。
(6)加热 发生反应的化学方程式为
发生反应的化学方程式为_______ 。
 和
和 的性质。
的性质。实验一:探究
 和
和 的溶解性和水溶液的酸碱性。
的溶解性和水溶液的酸碱性。| 步骤 | 实验操作 | 观察到的实验现象 | |
 |  | ||
| ① | 在2支试管里分别加入1g 和1g 和1g ,各加入10mL水,振荡 ,各加入10mL水,振荡 | 全部溶解,得到透明溶液 | 部分溶解,试管底部有少许固体 |
| ② | 将步骤①的试管中溶液分别分成两份,其中1份溶液中各滴加2滴酚酞溶液 | 溶液变红色 | 溶液变浅红色 |
| ③ | 在步骤②的另两份溶液中各滴加2滴10%盐酸,振荡 | 没有气泡产生 | 产生少量气泡 |
(1)常温下,
 的溶解度
的溶解度 的溶解度。
的溶解度。(2)下列推断正确的是_______(填字母)。
| A.碳酸钠溶液呈碱性,碳酸氢钠溶液呈酸性 |
| B.碳酸钠溶液、碳酸氢钠溶液都呈碱性 |
| C.碳酸钠溶液、碳酸氢钠溶液都呈酸性 |
| D.碳酸钠溶液呈碱性,碳酸氢钠溶液呈中性 |
 溶液和少量盐酸反应生成
溶液和少量盐酸反应生成 ,离子方程式为
,离子方程式为实验二:探究
 和
和 的热稳定性。
的热稳定性。
观察到的实验现象如下表所示:
| 物质 | 装置B中现象 | 装置C中现象 |
 | 无明显变化 | 开始断断续续产生气泡,一会儿后,没有气泡,溶液保持澄清 |
 | 白色粉末变蓝色 | 开始断断续续产生气泡,一会儿后,产生连续气泡,溶液变浑浊 |
(4)加热
 时,装置C中产生气泡的原因是
时,装置C中产生气泡的原因是(5)实验结论是
(6)加热
 发生反应的化学方程式为
发生反应的化学方程式为
您最近一年使用:0次
2023-01-04更新
|
81次组卷
|
2卷引用:河南省洛阳市栾川县第一高级中学2022-2023学年高一上学期期末考试化学试题
名校
5 . 下列装置或试剂合理且能达到实验目的的是
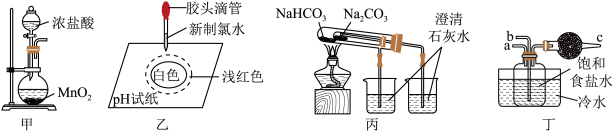

| A.用装置甲可以制取氯气 |
B.装置乙实验可以说明溶液中 和HClO分子能共存 和HClO分子能共存 |
C.装置丙可以用于比较 和 和 的热稳定性 的热稳定性 |
D.装置丁可用于模拟“侯氏制碱法”制取 ,a先通入 ,a先通入 ,然后b通入 ,然后b通入 ,c中放碱石灰,目的是防止 ,c中放碱石灰,目的是防止 污染环境 污染环境 |
您最近一年使用:0次
2023-01-03更新
|
202次组卷
|
6卷引用:河南省漯河市高级中学2023-2024学年高一上学期模拟预测化学试题
解题方法
6 . 下列实验操作和现象与所得出的结论均正确的是
| 选项 | 实验操作和现象 | 结论 |
| A | 向两支装有 沉淀的试管中分别滴加 沉淀的试管中分别滴加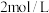 盐酸和 盐酸和 溶液,边加边振荡,沉淀均逐渐溶解 溶液,边加边振荡,沉淀均逐渐溶解 |  为两性氢氧化物 为两性氢氧化物 |
| B | 鉴别 和 和 固体时,将两份固体配制成等物质的量浓度的溶液,再滴入几滴酚酞溶液,其中一溶液变红且颜色较深 固体时,将两份固体配制成等物质的量浓度的溶液,再滴入几滴酚酞溶液,其中一溶液变红且颜色较深 | 该溶液的溶质是 |
| C | 向某溶液中滴加 溶液,溶液颜色无变化;再滴入氯水,溶液颜色仍无明显变化 溶液,溶液颜色无变化;再滴入氯水,溶液颜色仍无明显变化 | 该溶液中没有 |
| D | 向某溶液中滴加 溶液,生成白色沉淀,再加入盐酸,沉淀不溶解 溶液,生成白色沉淀,再加入盐酸,沉淀不溶解 | 该溶液中一定含有 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-01-01更新
|
460次组卷
|
2卷引用:河南省信阳市华中师大息县附中2022-2023学年高一下学期开学考试化学试题
7 . 下列叙述正确的是
A.向饱和 溶液中通入 溶液中通入 ,溶液中有沉淀生成 ,溶液中有沉淀生成 |
B.向某溶液中滴加少量盐酸后没有明显现象,则该溶液中一定不含 |
C.向 溶液中通入 溶液中通入 气体,溶液变混浊 气体,溶液变混浊 |
D.用澄清石灰水可以鉴别 溶液和 溶液和 溶液 溶液 |
您最近一年使用:0次
解题方法
8 . 某化学兴趣小组同学探究Na2CO3和NaHCO3与澄清石灰水的反应,常温下向两等份澄清石灰水中分别滴加0.05mol•L-1Na2CO3溶液和0.05mol•L-1NaHCO3溶液,测得实验过程中溶液的pH变化如图所示。下列说法错误的是
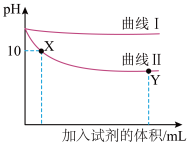

| A.曲线I表示的是滴加Na2CO3溶液的pH变化 |
| B.曲线Ⅱ反应至Ca2+恰好完全沉淀时,对应溶液的pH>7 |
| C.Y点时,溶液中的溶质只有NaHCO3 |
D.X点时,发生反应的离子方程式为2HCO +2OH-+Ca2+=CaCO3↓+CO +2OH-+Ca2+=CaCO3↓+CO +2H2O +2H2O |
您最近一年使用:0次
解题方法
9 . 如图所示实验装置正确,且能达到相应实验目的的是
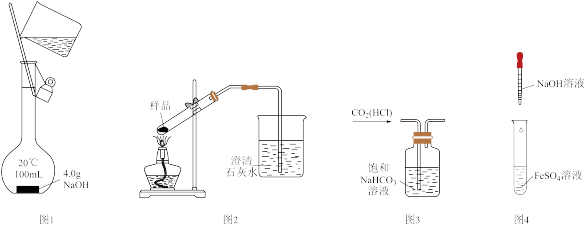

| A.图1:配制100mL1mol•L-1NaOH溶液 |
| B.图2:鉴别Na2CO3与NaHCO3固体 |
| C.图3:除去CO2中的HCl气体 |
| D.图4:制备Fe(OH)2固体 |
您最近一年使用:0次
10 . 我国化学家侯德榜发明的“联合制碱法”为世界制碱工业做出了巨大贡献。联合制碱法的工艺流程简化如下:

I.资料1:反应I中的化学方程式为:NaCl+NH3+CO2+H2O=NH4Cl+NaHCO3↓
资料2:20℃时,溶解度小于0.0lg的物质属于难溶物;20℃时BaSO4溶解度为 g。
g。
资料3:表1有关物质的溶解度(20℃)
(1)操作I的名称为_______ ,反应II的化学方程式为_______ 。
(2)相同温度下,用pH试纸测量同等浓度的Na2CO3与NaHCO3溶液pH,_______ 溶液碱性强。
(3)离子反应: ,BaSO4难溶生成沉淀,符合复分解反应发生的条件;反应I中NaHCO3不是难溶物,也生成了沉淀,理由是
,BaSO4难溶生成沉淀,符合复分解反应发生的条件;反应I中NaHCO3不是难溶物,也生成了沉淀,理由是_______ 。
II.泡腾片是一种医药片剂,适用于儿童、老年人以及吞服药丸困难的患者。泡腾片放入水中,在崩解剂的作用下,即刻产生大量气泡(二氧化碳),使片剂迅速崩解形成水溶液,崩解剂主要由NaHCO3固体与柠檬酸固体组成。
(4)下列说法正确的是_______ (填字母)。
A.NaHCO3固体与柠檬酸固体不反应
B.柠檬酸在水中电离产生H+与NaHCO3反应
C.Na2CO3比NaHCO3稳定,受热不易分解
(5)某NaHCO3样品中含NaCl杂质,取质量为a g的样品,加入足量的稀盐酸,充分反应后,加热、蒸干、灼烧,得到b g固体物质,则此样品中NaHCO3的质量分数是_______ 。

I.资料1:反应I中的化学方程式为:NaCl+NH3+CO2+H2O=NH4Cl+NaHCO3↓
资料2:20℃时,溶解度小于0.0lg的物质属于难溶物;20℃时BaSO4溶解度为
 g。
g。资料3:表1有关物质的溶解度(20℃)
| 物质 | NaCl | NH4HCO3 | NaHCO3 | NH4Cl |
| 溶解度/g | 36.0 | 21.7 | 9.6 | 37.2 |
(1)操作I的名称为
(2)相同温度下,用pH试纸测量同等浓度的Na2CO3与NaHCO3溶液pH,
(3)离子反应:
 ,BaSO4难溶生成沉淀,符合复分解反应发生的条件;反应I中NaHCO3不是难溶物,也生成了沉淀,理由是
,BaSO4难溶生成沉淀,符合复分解反应发生的条件;反应I中NaHCO3不是难溶物,也生成了沉淀,理由是II.泡腾片是一种医药片剂,适用于儿童、老年人以及吞服药丸困难的患者。泡腾片放入水中,在崩解剂的作用下,即刻产生大量气泡(二氧化碳),使片剂迅速崩解形成水溶液,崩解剂主要由NaHCO3固体与柠檬酸固体组成。
(4)下列说法正确的是
A.NaHCO3固体与柠檬酸固体不反应
B.柠檬酸在水中电离产生H+与NaHCO3反应
C.Na2CO3比NaHCO3稳定,受热不易分解
(5)某NaHCO3样品中含NaCl杂质,取质量为a g的样品,加入足量的稀盐酸,充分反应后,加热、蒸干、灼烧,得到b g固体物质,则此样品中NaHCO3的质量分数是
您最近一年使用:0次



