解题方法
1 . 化学与生活息息相关。请根据题意填空:
(1)___________ (填“ ”或“
”或“ ”)可以与水反应生成氧气用于解决鱼塘缺氧问题。
”)可以与水反应生成氧气用于解决鱼塘缺氧问题。
(2)用于做面食的苏打 与小苏打
与小苏打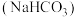 外观相似。某同学取少量两种物质分别置于干燥的坩埚中,盖上盖子加热,盖子内壁有大量水珠附着的是
外观相似。某同学取少量两种物质分别置于干燥的坩埚中,盖上盖子加热,盖子内壁有大量水珠附着的是___________ (填“苏打”或“小苏打”)。
(3)向盛有 溶液中加适量铁粉,溶液颜色
溶液中加适量铁粉,溶液颜色___________ (填“由黄色变为绿色”或“由绿色变为黄色”)。
(1)
 ”或“
”或“ ”)可以与水反应生成氧气用于解决鱼塘缺氧问题。
”)可以与水反应生成氧气用于解决鱼塘缺氧问题。(2)用于做面食的苏打
 与小苏打
与小苏打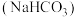 外观相似。某同学取少量两种物质分别置于干燥的坩埚中,盖上盖子加热,盖子内壁有大量水珠附着的是
外观相似。某同学取少量两种物质分别置于干燥的坩埚中,盖上盖子加热,盖子内壁有大量水珠附着的是(3)向盛有
 溶液中加适量铁粉,溶液颜色
溶液中加适量铁粉,溶液颜色
您最近一年使用:0次
解题方法
2 . 物质类别和核心元素的价态是学习元素及其化合物性质的两个重要认识视角。图为钠及其化合物的“价-类”二维图,请回答下列问题:
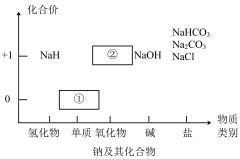
(1)物质①与水反应的离子方程式为_______ ,通常把物质①保存在_______ 中。
(2)写出淡黄色固体②与二氧化碳反应的化学方程式,并用双线桥法标识电子转移的方向和数目:_______ 。
(3)向50 mL沸水中加入5~6滴 饱和溶液,加热至产生红褐色液体,停止加热,该反应的化学方程式是:
饱和溶液,加热至产生红褐色液体,停止加热,该反应的化学方程式是:_______ 。利用_______ 来证明得到的分散系是氢氧化铁胶体。
(4)纯碱和小苏打都是重要的化工原料,在生产和生活中有若广泛的应用。
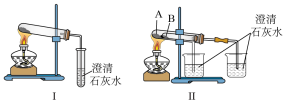
图Ⅱ中受热处发生反应的化学方程式为_______ 。
(5)下列关于 和
和 的说法不正确的是
的说法不正确的是_______ 。
A.相同条件下的溶解度;
B.可以用澄清石灰水区别 溶液和
溶液和 溶液
溶液
C.可以用加热的方法除去 固体中的
固体中的 杂质
杂质
D. 溶液和
溶液和 溶液均显碱性
溶液均显碱性
E.等质量的碳酸钠和碳酸氢钠与足量盐酸反应, 放出的气体多
放出的气体多

(1)物质①与水反应的离子方程式为
(2)写出淡黄色固体②与二氧化碳反应的化学方程式,并用双线桥法标识电子转移的方向和数目:
(3)向50 mL沸水中加入5~6滴
 饱和溶液,加热至产生红褐色液体,停止加热,该反应的化学方程式是:
饱和溶液,加热至产生红褐色液体,停止加热,该反应的化学方程式是:(4)纯碱和小苏打都是重要的化工原料,在生产和生活中有若广泛的应用。

图Ⅱ中受热处发生反应的化学方程式为
(5)下列关于
 和
和 的说法不正确的是
的说法不正确的是A.相同条件下的溶解度;

B.可以用澄清石灰水区别
 溶液和
溶液和 溶液
溶液C.可以用加热的方法除去
 固体中的
固体中的 杂质
杂质D.
 溶液和
溶液和 溶液均显碱性
溶液均显碱性E.等质量的碳酸钠和碳酸氢钠与足量盐酸反应,
 放出的气体多
放出的气体多
您最近一年使用:0次
解题方法
3 . 钠及其化合物在认识物质转化规律以及生产生活中均有重要应用。
(1)写出钠与水反应的化学方程式________ 。
(2)过氧化钠是否属于碱性氧化物________ (填“是”或“否”);列举过氧化钠的一种用途________ ;
(3)下列关于 的认识正确的是________。(填字母)
的认识正确的是________。(填字母)
(4)传统蒸馒头常采用酵头发面,酵头可使面团在微生物作用下产生 气体,从而使面团疏松,但同时也会产生乳酸、醋酸等有机酸,需要额外添加“碱面”将酸去除。等质量的
气体,从而使面团疏松,但同时也会产生乳酸、醋酸等有机酸,需要额外添加“碱面”将酸去除。等质量的 和
和 ,因
,因________ (填“ ”或“
”或“ ”)消耗酸更多,更适合作为中和发酵带来的酸味的“碱面”。
”)消耗酸更多,更适合作为中和发酵带来的酸味的“碱面”。
(5)若面团发得不好,面团内的气孔少,不够膨松,需添加________ (填“ ”或“
”或“ ”),继续揉面,上锅蒸后也能蒸出松软的馒头。用化学方程式表示其原理
”),继续揉面,上锅蒸后也能蒸出松软的馒头。用化学方程式表示其原理________ 。
(1)写出钠与水反应的化学方程式
(2)过氧化钠是否属于碱性氧化物
(3)下列关于
 的认识正确的是________。(填字母)
的认识正确的是________。(填字母)| A.受热易分解 | B.俗称纯碱、苏打 | C.属于碱 | D.可与酸反应 |
 气体,从而使面团疏松,但同时也会产生乳酸、醋酸等有机酸,需要额外添加“碱面”将酸去除。等质量的
气体,从而使面团疏松,但同时也会产生乳酸、醋酸等有机酸,需要额外添加“碱面”将酸去除。等质量的 和
和 ,因
,因 ”或“
”或“ ”)消耗酸更多,更适合作为中和发酵带来的酸味的“碱面”。
”)消耗酸更多,更适合作为中和发酵带来的酸味的“碱面”。(5)若面团发得不好,面团内的气孔少,不够膨松,需添加
 ”或“
”或“ ”),继续揉面,上锅蒸后也能蒸出松软的馒头。用化学方程式表示其原理
”),继续揉面,上锅蒸后也能蒸出松软的馒头。用化学方程式表示其原理
您最近一年使用:0次
解题方法
4 . 金属单质钠可经下图所示的过程进行转化。
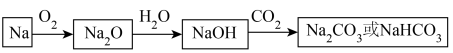
请回答下列问题:
(1)钠燃烧时,火焰呈___________ (选填“黄色”或“紫红色”)。
(2)根据物质的性质进行分类时, 可被称为
可被称为___________ (选填“酸性氧化物”或“碱性氧化物”)。
(3)在反应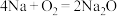 中,
中, 作
作___________ (选填“氧化剂”或“还原剂”)。
(4)钠元素的金属性较强,因此 与
与 反应生成的
反应生成的 是
是___________ (选填“强碱”或“弱碱”)。
(5)下图为 受热分解的实验装置图,图中应改正之处是
受热分解的实验装置图,图中应改正之处是___________ (填写字母)。
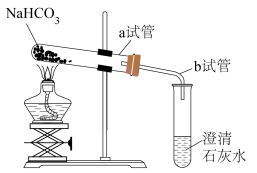
A.a试管口应略向上倾斜 B.b导管应插入液面下
(6)碳酸氢钠不稳定,受热易分解,产生的气体可以使澄清石灰水变浑浊。碳酸氢钠受热分解的化学方程式为:___________ 。
(7)可以利用___________ (选填“加热”或“过滤”)的方法来鉴别 和
和 。
。

请回答下列问题:
(1)钠燃烧时,火焰呈
(2)根据物质的性质进行分类时,
 可被称为
可被称为(3)在反应
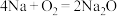 中,
中, 作
作(4)钠元素的金属性较强,因此
 与
与 反应生成的
反应生成的 是
是(5)下图为
 受热分解的实验装置图,图中应改正之处是
受热分解的实验装置图,图中应改正之处是
A.a试管口应略向上倾斜 B.b导管应插入液面下
(6)碳酸氢钠不稳定,受热易分解,产生的气体可以使澄清石灰水变浑浊。碳酸氢钠受热分解的化学方程式为:
(7)可以利用
 和
和 。
。
您最近一年使用:0次
名校
5 . 碳酸钠和碳酸氢钠是生活中常见的物质。请回答下列问题:
(1)碳酸氢钠俗称___________ ,其水溶液显___________ 性(填“酸”、“碱”或“中”)。
(2)碳酸氢钠可治疗胃酸(0.2%~0.4%的盐酸)过多,反应的离子方程式为___________ 。等质量的碳酸钠和碳酸氢钠与足量盐酸反应时生成CO2的量:前者___________ (填“>”“<”或“=”)后者。
(3)用加热的方法除去碳酸钠固体中碳酸氢钠的反应的化学方程式为___________ 。
(1)碳酸氢钠俗称
(2)碳酸氢钠可治疗胃酸(0.2%~0.4%的盐酸)过多,反应的离子方程式为
(3)用加热的方法除去碳酸钠固体中碳酸氢钠的反应的化学方程式为
您最近一年使用:0次
名校
6 . 回答下列问题。
I.纯碱 和小苏打
和小苏打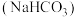 都是白色晶体,在日常生活中都可以找到。
都是白色晶体,在日常生活中都可以找到。
(1)若要在家中将它们区分开来,下列方法中可行的是___________。
(2) 溶液和
溶液和 溶液中都含有
溶液中都含有 、
、 、
、 、
、 、
、 、
、 、
、 写出一个用浓度表示这些微粒之间的电荷守恒的关系式
写出一个用浓度表示这些微粒之间的电荷守恒的关系式___________ 。
II.在两个相同的特制容器中分别加入 和
和 溶液,再分别用
溶液,再分别用 盐酸滴定,利用
盐酸滴定,利用 计和压力传感器检测,得到如下曲线:
计和压力传感器检测,得到如下曲线:
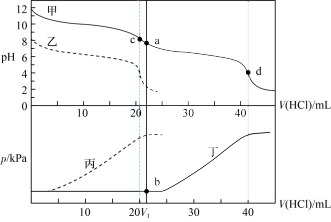
(3)甲、乙两条线中表示向 溶液中滴加盐酸的是
溶液中滴加盐酸的是___________ ,理由是___________ 。丙、丁两条线中表示向 溶液中滴加盐酸的是
溶液中滴加盐酸的是___________ ,理由是___________ 。
(4)当滴加盐酸的体积为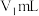 时(a点、b点),所发生的反应用化学方程式表示为
时(a点、b点),所发生的反应用化学方程式表示为___________ 。
(5)根据 图分析:
图分析:
①滴定时c点可用___________ 作指示剂指示滴定终点。
A.甲基橙 B.石蕊 C.酚酞
②滴定时d点可用___________ 作指示剂指示滴定终点。
A.甲基橙 B.石蕊 C.酚酞
I.纯碱
 和小苏打
和小苏打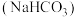 都是白色晶体,在日常生活中都可以找到。
都是白色晶体,在日常生活中都可以找到。(1)若要在家中将它们区分开来,下列方法中可行的是___________。
| A.在水杯中各盛相同质量的样品,分别加入等体积的白醋,观察反应的剧烈程度 |
| B.分别用干净铁丝蘸取样品在煤气灶的火焰上灼烧,观察火焰颜色 |
| C.将样品溶解,分别加入澄清石灰水,观察是否有白色沉淀 |
| D.分别放在炒锅中加热,观察是否有残留物 |
(2)
 溶液和
溶液和 溶液中都含有
溶液中都含有 、
、 、
、 、
、 、
、 、
、 、
、 写出一个用浓度表示这些微粒之间的电荷守恒的关系式
写出一个用浓度表示这些微粒之间的电荷守恒的关系式II.在两个相同的特制容器中分别加入
 和
和 溶液,再分别用
溶液,再分别用 盐酸滴定,利用
盐酸滴定,利用 计和压力传感器检测,得到如下曲线:
计和压力传感器检测,得到如下曲线:
(3)甲、乙两条线中表示向
 溶液中滴加盐酸的是
溶液中滴加盐酸的是 溶液中滴加盐酸的是
溶液中滴加盐酸的是(4)当滴加盐酸的体积为
 时(a点、b点),所发生的反应用化学方程式表示为
时(a点、b点),所发生的反应用化学方程式表示为(5)根据
 图分析:
图分析:①滴定时c点可用
A.甲基橙 B.石蕊 C.酚酞
②滴定时d点可用
A.甲基橙 B.石蕊 C.酚酞
您最近一年使用:0次
名校
解题方法
7 . 某小组同学进行Na2CO3和NaHCO3性质的探究,实验如图(夹持装置已略去,气密性已检验)。
(1)实验I,能够证明Na2CO3的热稳定性强于NaHCO3的证据是_______ ,NaHCO3加热分解的化学方程式为_______ 。
(2)实验II,方框内装置中饱和NaHCO3的作用是_______ 。
(3)实验II圆底烧瓶中发生反应的离子方程式为:_______ ,持续一段时间后,观察到饱和Na2CO3溶液中有细小晶体析出,用化学方程式表示产生细小晶体的原因:_______ 。
| 实验I | 实验II |
 | 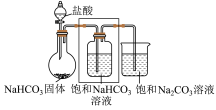 |
(1)实验I,能够证明Na2CO3的热稳定性强于NaHCO3的证据是
(2)实验II,方框内装置中饱和NaHCO3的作用是
(3)实验II圆底烧瓶中发生反应的离子方程式为:
您最近一年使用:0次
名校
8 . 完成下列填空。
(1)新制氯水呈浅黄绿色,起作用的微粒是______ 。
(2)检验某溶液中是否存在 的试剂是
的试剂是______ 和______ 。
(3)下列试剂可鉴别 溶液和
溶液和 溶液的是
溶液的是______ (填编号)。
① 溶液 ②
溶液 ② 溶液 ③盐酸 ④
溶液 ③盐酸 ④ 溶液
溶液
(4)漂白液在空气中的漂白原理用化学方程表示为______ 。
(1)新制氯水呈浅黄绿色,起作用的微粒是
(2)检验某溶液中是否存在
 的试剂是
的试剂是(3)下列试剂可鉴别
 溶液和
溶液和 溶液的是
溶液的是①
 溶液 ②
溶液 ② 溶液 ③盐酸 ④
溶液 ③盐酸 ④ 溶液
溶液(4)漂白液在空气中的漂白原理用化学方程表示为
您最近一年使用:0次
名校
解题方法
9 . 碳酸钠和碳酸氢钠是生活中常见的物质。请回答下列问题。
(1)碳酸氢钠的化学式_______ ,俗称_______ ,其水溶液显_______ (填“酸”、“碱”或“中”)性。
(2)碳酸氢钠与盐酸反应的离子方程式为_______ 。等质量的碳酸钠和碳酸氢钠与足量盐酸反应时剧烈程度,前者_______ 后者(填“>”、“<”或“=”)。
(1)碳酸氢钠的化学式
(2)碳酸氢钠与盐酸反应的离子方程式为
您最近一年使用:0次
名校
解题方法
10 . 对于数以千万计的化学物质,人们常根据物质的组成、结构、性质或用途进行分类,分类法的作用几乎是无可替代的。回答下列问题:
Ⅰ.现有以下物质:①CaO;②液态HCl;③ 固体;④熔融KCl;⑤
固体;④熔融KCl;⑤ ;⑥
;⑥ ;⑦KOH固体
;⑦KOH固体
(1)以上物质中属于碱性氧化物的是___________ (填序号,下同)。
(2)以上物质中能导电且属于电解质的是___________ 。
Ⅱ.下列三组物质中,均有一种物质的类别与其他三种不同。
①MgO、 、
、 、CuO
、CuO
②HCl、 、
、 、
、
③NaOH、 、KOH、
、KOH、
(3)三种物质依次是(填化学式):
①___________ ;②___________ ;③___________ 。
(4)上述三种物质相互作用可生成一种新物质 ,该反应
,该反应___________ (填“是”或“不是”)氧化还原反应。
(5)写出 与足量稀硫酸反应的离子方程式:
与足量稀硫酸反应的离子方程式:___________ 。
(6) 与
与 在溶液中都不能大量共存,试用离子方程式说明:
在溶液中都不能大量共存,试用离子方程式说明:___________ 。
Ⅰ.现有以下物质:①CaO;②液态HCl;③
 固体;④熔融KCl;⑤
固体;④熔融KCl;⑤ ;⑥
;⑥ ;⑦KOH固体
;⑦KOH固体(1)以上物质中属于碱性氧化物的是
(2)以上物质中能导电且属于电解质的是
Ⅱ.下列三组物质中,均有一种物质的类别与其他三种不同。
①MgO、
 、
、 、CuO
、CuO②HCl、
 、
、 、
、
③NaOH、
 、KOH、
、KOH、
(3)三种物质依次是(填化学式):
①
(4)上述三种物质相互作用可生成一种新物质
 ,该反应
,该反应(5)写出
 与足量稀硫酸反应的离子方程式:
与足量稀硫酸反应的离子方程式:(6)
 与
与 在溶液中都不能大量共存,试用离子方程式说明:
在溶液中都不能大量共存,试用离子方程式说明:
您最近一年使用:0次



