解题方法
1 . 锂在新能源等领域应用广泛。从粉煤灰(含Al2O3、Fe2O3、Li2O、SiO2等)中回收提取铝、锂元素的化合物的流程如图所示:

已知:碳酸锂的溶解度(g·L-1)见表。
回答下列问题
(1)“粉碎”的目的是___________ ,滤渣1的成分主要是___________ 。(填化学式)
(2)“调pH”的目的是沉淀Fe3+、Al3+。当离子浓度≤1.0×10-5mol·L-1时表示该离子沉淀完全。常温下,如果溶液pH=4,Fe3+、Al3+___________ (填“能”或“否”)均沉淀完全,此时溶液中c(Fe3+)、c(Al3+)之比为___________ 。(已知:Ksp[Fe(OH)3]=8.0×10-38,Ksp[Al(OH)3]=2.0×10-33)
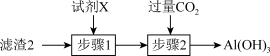
(3)从滤渣2中分离出Al(OH)3,可用如图所示方法,试剂X是___________ ,“步骤2”中主要发生的离子反应方程式有OH-+CO2=HCO 、
、___________ 。
(4)“沉锂”中的“一系列操作”依次为蒸发浓缩、___________ 、洗涤、干燥。检验母液主要溶质的阴离子所用的试剂为___________ 。母液的用途___________ (任写一种)。
(5)太阳能路灯蓄电池是磷酸铁锂电池,其工作原理如图所示。电池总反应式为LixC6 + Li1−xFePO4 LiFePO4 + 6C。试写出充电时,该电池正极材料上的反应式:
LiFePO4 + 6C。试写出充电时,该电池正极材料上的反应式:___________ 。


已知:碳酸锂的溶解度(g·L-1)见表。
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 80 | 100 |
| Li2CO3 | 1.54 | 1.43 | 1.33 | 1.25 | 1.17 | 1.08 | 1.01 | 0.85 | 0.72 |
(1)“粉碎”的目的是
(2)“调pH”的目的是沉淀Fe3+、Al3+。当离子浓度≤1.0×10-5mol·L-1时表示该离子沉淀完全。常温下,如果溶液pH=4,Fe3+、Al3+
(3)从滤渣2中分离出Al(OH)3,可用如图所示方法,试剂X是
 、
、
(4)“沉锂”中的“一系列操作”依次为蒸发浓缩、
(5)太阳能路灯蓄电池是磷酸铁锂电池,其工作原理如图所示。电池总反应式为LixC6 + Li1−xFePO4
 LiFePO4 + 6C。试写出充电时,该电池正极材料上的反应式:
LiFePO4 + 6C。试写出充电时,该电池正极材料上的反应式:
您最近一年使用:0次
名校
2 . 下列物质中属于两性氧化物的是( )
| A.CO2 | B.Na2O2 | C.Na2O | D.Al2O3 |
您最近一年使用:0次
2020-04-27更新
|
619次组卷
|
6卷引用:广东省惠州市2021-2022学年高一上学期期末质量检测化学试题



