1 . 下列各组物质中,满足图示关系并在一定条件下能一步转化的组合是
| 序号 | X | Y | Z | W |
|
| ① |  |  |  | Na | |
| ② |  |  |  |  | |
| ③ |  |  |  |  | |
| ④ |  |  | 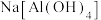 | Al |
| A.①② | B.①③ | C.②③ | D.③④ |
您最近一年使用:0次
2 . 分类是学习和研究化学的一种重要方法,下列物质的分类正确的是
| A.氧气和氯气都属于非金属单质 | B.烧碱和纯碱都属于碱 |
C. 和 和 都属于两性氧化物 都属于两性氧化物 | D. 和 和 都属于酸 都属于酸 |
您最近一年使用:0次
解题方法
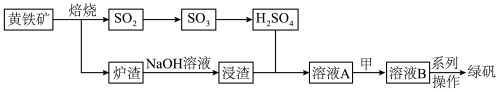
3 . 硫酸工业在生活生产中占有极其重要的地位,硫酸也是许多物质的制备原料,工业上以黄铁矿为原料制备绿矾 的工艺流程如下图所示:(已知炉渣中主要含有
的工艺流程如下图所示:(已知炉渣中主要含有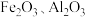 和极少量:
和极少量: )
)______ (填化学式),在焙烧之前将黄铁矿粉碎的目的是___________ 。
(2)写出由炉渣得到浸渣时发生的主要离子反应方程式__________ 。
(3)写出由 得到
得到 的化学方程式
的化学方程式__________ ,工业制硫酸时,为提高吸收效率,通常用下列哪种物质______ 吸收 。
。
A.蒸馏水 B.98.3%的浓硫酸 C.70%的浓硫酸 D.稀硫酸
(4)流程中的物质甲可以是______ 。
①铁粉 ②铜粉 ③硫化钠 ④氨水 ⑤氯气
(5)由溶液B得到绿矾的系列操作为_________ ,_________ ,过滤,洗涤,干燥。
 的工艺流程如下图所示:(已知炉渣中主要含有
的工艺流程如下图所示:(已知炉渣中主要含有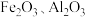 和极少量:
和极少量: )
)
(2)写出由炉渣得到浸渣时发生的主要离子反应方程式
(3)写出由
 得到
得到 的化学方程式
的化学方程式 。
。A.蒸馏水 B.98.3%的浓硫酸 C.70%的浓硫酸 D.稀硫酸
(4)流程中的物质甲可以是
①铁粉 ②铜粉 ③硫化钠 ④氨水 ⑤氯气
(5)由溶液B得到绿矾的系列操作为
您最近一年使用:0次
解题方法
4 . 七铝十二钙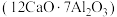 是新型的超导材料和发光材料。
是新型的超导材料和发光材料。
I.工业中 的制备研究Deacon法制备
的制备研究Deacon法制备 原理为:
原理为: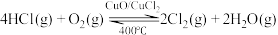
(1)热化学机理研究
已知:反应中,每 被氧化,放出
被氧化,放出 的热量。
的热量。
①Deacon法制备 的热化学方程式是
的热化学方程式是__ 。___ kJ。
(2)催化氧化机理研究
Deacon法制备 反应,
反应,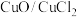 催化历程如下:
催化历程如下:
反应①:______ (写出反应①的化学方程式)
反应②:
II.用白云石(主要含 和
和 )和废
)和废 片(主要含
片(主要含 和
和 )制备七铝十二钙的工艺如下图:
)制备七铝十二钙的工艺如下图:____ 。
(4)滤液1中通入CO2时,需同时通入NH3,理由是____ 。
(5)用NaOH溶液处理废Al片的目的是_____ 。
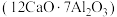 是新型的超导材料和发光材料。
是新型的超导材料和发光材料。I.工业中
 的制备研究Deacon法制备
的制备研究Deacon法制备 原理为:
原理为: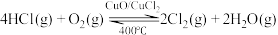
(1)热化学机理研究
已知:反应中,每
 被氧化,放出
被氧化,放出 的热量。
的热量。①Deacon法制备
 的热化学方程式是
的热化学方程式是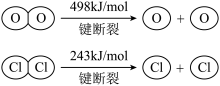
(2)催化氧化机理研究
Deacon法制备
 反应,
反应,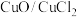 催化历程如下:
催化历程如下:反应①:
反应②:

II.用白云石(主要含
 和
和 )和废
)和废 片(主要含
片(主要含 和
和 )制备七铝十二钙的工艺如下图:
)制备七铝十二钙的工艺如下图:
(4)滤液1中通入CO2时,需同时通入NH3,理由是
(5)用NaOH溶液处理废Al片的目的是
您最近一年使用:0次
名校
解题方法
5 . GaN是一种重要的半导体材料,利用铝土矿(成分为 、
、 、
、 )制备GaN的工艺流程如图所示。已知Ga与Al的化学性质相似,Ga的熔点为29.8℃,沸点为:2403℃。下列说法错误的是
)制备GaN的工艺流程如图所示。已知Ga与Al的化学性质相似,Ga的熔点为29.8℃,沸点为:2403℃。下列说法错误的是
 、
、 、
、 )制备GaN的工艺流程如图所示。已知Ga与Al的化学性质相似,Ga的熔点为29.8℃,沸点为:2403℃。下列说法错误的是
)制备GaN的工艺流程如图所示。已知Ga与Al的化学性质相似,Ga的熔点为29.8℃,沸点为:2403℃。下列说法错误的是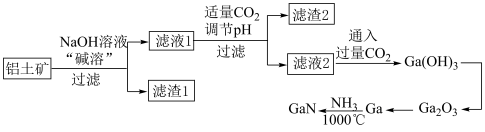
| A.过滤时需用到的硅酸盐材质仪器为烧杯、漏斗、玻璃棒 |
B.滤液1中主要含有的阴离子为 、 、 、 、 |
C.滤液2中得到 时发生反应的离子方程式为 时发生反应的离子方程式为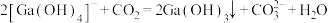 |
D.Ga与 反应生成GaN时,参与反应的氧化剂与还原剂的物质的量之比为1∶1 反应生成GaN时,参与反应的氧化剂与还原剂的物质的量之比为1∶1 |
您最近一年使用:0次
2024-06-29更新
|
454次组卷
|
5卷引用:四川省遂宁市射洪中学校2023-2024学年高一(强基班)下学期期末模拟考试化学试题
名校
6 . 为除去括号内的杂质,所选用的除杂试剂不正确的是
| A.Fe2O3固体(Al2O3):氢氧化钠溶液 | B.CH4气体(C2H4):酸性高锰酸钾溶液 |
| C.CO2气体(HCl):饱和碳酸氢钠溶液 | D.NO气体(NO2):水 |
您最近一年使用:0次
名校
解题方法
7 . 四氢铝钠( )是强还原剂,高铁酸钠(
)是强还原剂,高铁酸钠( )是一种绿色净水剂。以工业制备硫酸的烧渣(主要成分为
)是一种绿色净水剂。以工业制备硫酸的烧渣(主要成分为 、
、 和
和 ,含少量
,含少量 ,其他杂质不反应)为原料制备四氢铝钠和高铁酸钠的流程如下,回答下列问题:
,其他杂质不反应)为原料制备四氢铝钠和高铁酸钠的流程如下,回答下列问题:_____________ (任写一个)。
(2)“转化”中 的具体作用是
的具体作用是_______________ ;检验溶液中含有 的试剂和实验现象为
的试剂和实验现象为_______________ 。
(3)“分离”的操作是指____________ 。
(4)“沉铝”时通入过量 发生反应的离子方程式为
发生反应的离子方程式为___________ ;所得滤液中的溶质有__________ (写化学式)。
(5)“合成”中,发生反应的化学方程式为(乙醚作溶剂,不参与反应)____________ 。
(6) 中氢的化合价为
中氢的化合价为____________ ;“有效氢”指单位质量(1g)含氢还原剂的还原能力相当于多少克氢气的还原能力。则 的“有效氢”为
的“有效氢”为____________ (保留三位有效数字)。
 )是强还原剂,高铁酸钠(
)是强还原剂,高铁酸钠( )是一种绿色净水剂。以工业制备硫酸的烧渣(主要成分为
)是一种绿色净水剂。以工业制备硫酸的烧渣(主要成分为 、
、 和
和 ,含少量
,含少量 ,其他杂质不反应)为原料制备四氢铝钠和高铁酸钠的流程如下,回答下列问题:
,其他杂质不反应)为原料制备四氢铝钠和高铁酸钠的流程如下,回答下列问题: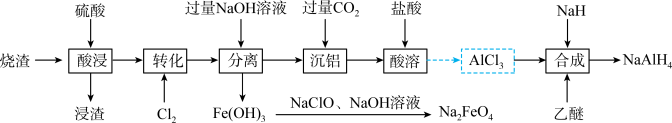
(2)“转化”中
 的具体作用是
的具体作用是 的试剂和实验现象为
的试剂和实验现象为(3)“分离”的操作是指
(4)“沉铝”时通入过量
 发生反应的离子方程式为
发生反应的离子方程式为(5)“合成”中,发生反应的化学方程式为(乙醚作溶剂,不参与反应)
(6)
 中氢的化合价为
中氢的化合价为 的“有效氢”为
的“有效氢”为
您最近一年使用:0次
名校
解题方法
8 . Ⅰ.某废旧金属材料中主要含Fe、Cu、Al、Fe2O3、FeO、Al2O3、CuO(其余成分与酸碱都不反应)和可燃性有机物,为节约和充分利用资源,通过如下工艺流程回收Al、Cu,绿矾等。回答下列问题:___________ 。
(2)操作Ⅰ和Ⅱ均会用到的仪器为___________ 。
(3)将得到的Cu加入到硫酸和稀硝酸的混合溶液中得到CuSO4溶液(过程中硝酸变成NO气体),为了得到纯净的CuSO4溶液,H2SO4和HNO3的物质的量之比为___________ ;
(4)滤渣Ⅱ的化学成分为___________ 。
(5)滤液Ⅱ制取绿矾晶体需先加入少量稀硫酸再经过___________ 、___________ 、过滤、洗涤,干燥得到绿矾晶体。
Ⅱ.海水的综合利用是当今的热点话题之一。
(6)从海水中提取粗盐后的母液中含有K+、Na+和Mg2+等阳离子。对母液进行一系列的加工可制得金属镁。
①从离子反应的角度思考,在母液中加入石灰乳所起的作用是___________ 。
②电解熔融的无水氯化镁所得的镁蒸气在特定的环境中冷却后即为固体镁。O2___________ (填“能”或“不能”)用作镁蒸气的冷却剂。
(7)海带中含有碘元素。从海带中提取碘的实验过程如图:___________ 中灼烧(填仪器名称);
②海带灰悬浊液含有I-,步骤④的试剂选用H2O2、稀硫酸,发生反应的离子方程式为___________ 。
③步骤⑤“提取”包含以下四个过程:___________ (填“CCl4”或“H2O”)中的溶解度更小。
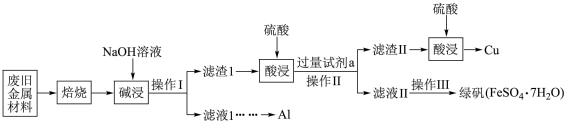
(2)操作Ⅰ和Ⅱ均会用到的仪器为
(3)将得到的Cu加入到硫酸和稀硝酸的混合溶液中得到CuSO4溶液(过程中硝酸变成NO气体),为了得到纯净的CuSO4溶液,H2SO4和HNO3的物质的量之比为
(4)滤渣Ⅱ的化学成分为
(5)滤液Ⅱ制取绿矾晶体需先加入少量稀硫酸再经过
Ⅱ.海水的综合利用是当今的热点话题之一。
(6)从海水中提取粗盐后的母液中含有K+、Na+和Mg2+等阳离子。对母液进行一系列的加工可制得金属镁。
①从离子反应的角度思考,在母液中加入石灰乳所起的作用是
②电解熔融的无水氯化镁所得的镁蒸气在特定的环境中冷却后即为固体镁。O2
(7)海带中含有碘元素。从海带中提取碘的实验过程如图:

②海带灰悬浊液含有I-,步骤④的试剂选用H2O2、稀硫酸,发生反应的离子方程式为
③步骤⑤“提取”包含以下四个过程:
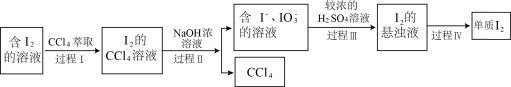
您最近一年使用:0次
23-24高一下·全国·课后作业
9 . 下列除杂试剂或方法(括号内为杂质)错误的是
A.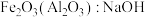 溶液 溶液 | B. :酸性 :酸性 溶液 溶液 |
C.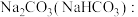 加热 加热 | D. 溶液 溶液 |
您最近一年使用:0次
2024-03-31更新
|
300次组卷
|
3卷引用:四川省眉山市仁寿第一中学校(北校区)2023-2024学年高一下学期3月月考化学试题
解题方法
10 . 下列物质中,既能与盐酸反应,又能与氢氧化钠溶液反应的有
①Na ②Na2CO3 ③Al2O3 ④NaHSO4 ⑤NaHCO3 ⑥(NH4)2CO3
①Na ②Na2CO3 ③Al2O3 ④NaHSO4 ⑤NaHCO3 ⑥(NH4)2CO3
| A.①③④⑤⑥ | B.①③⑤⑥ | C.②③⑤⑥ | D.①②③⑤ |
您最近一年使用:0次
2024-03-20更新
|
92次组卷
|
2卷引用:四川省雅安市名山区第三中学2023-2024学年高一12月月考化学试题




