11-12高三上·浙江宁波·阶段练习
名校
解题方法
1 . 将一定质量的镁和铝混合物投入200 mL硫酸中,固体全部溶解后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量n与加入NaOH溶液的体积V的变化如下图所示。则下列说法不正确的是:
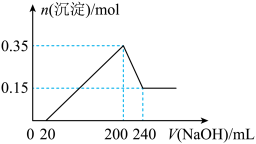
| A.镁和铝的总质量为9 g |
| B.最初20 mLNaOH溶液用于中和过量的硫酸 |
| C.硫酸的物质的量浓度为2.5 mol·L-1 |
| D.生成的氢气在标准状况下的体积为11.2 L |
您最近一年使用:0次
2021-02-05更新
|
1827次组卷
|
34卷引用:3.1.3 铝与氢氧化钠溶液的反应(重点练)-2020-2021学年高一化学上学期十分钟同步课堂专练(人教版)
(已下线)3.1.3 铝与氢氧化钠溶液的反应(重点练)-2020-2021学年高一化学上学期十分钟同步课堂专练(人教版)(已下线)3.2.2 物质的量在化学方程式计算中的应用(基础练)-2020-2021学年高一化学上学期十分钟同步课堂专练(人教版2019必修第一册)(已下线)2010-2011学年浙江宁海县正学中学高三上学期第一次阶段性测试化学试卷(已下线)2011-2012学年江西省赣州市(十一县市)高三第一学期期中联考化学试卷(已下线)2013-2014云南省玉溪一中高三5月校统测理科综合化学试卷(已下线)2014陕西西安市长安一中高一上学期期末化学(实验班)试卷(已下线)2015届江西省南昌市三校高三10月联考化学试卷2015-2016学年辽宁葫芦岛一中高二上期初考试化学试卷 2016届江西省余江县第一中学高三上学期二次模拟化学试卷2015-2016学年黑龙江省哈尔滨三中高一上期末化学试卷2015-2016学年山西省太原五中高一上学期期末化学试卷2015-2016学年河南省南阳市宛东五校高一下第一次联考化学试卷2015-2016学年黑龙江哈尔滨三中高二下期末化学试卷山东省寿光现代中学2016-2017学年高一下学期第三学段质量监测(期中)化学试题河北省大名县第一中学2018届高三(实验班)上学期第一次月考化学试题安徽省六安市第一中学2017-2018学年高一下学期开学考试化学试题新疆维吾尔自治区阿克苏市高级中学2019届高三上学期第二次月考化学试题黑龙江省双鸭山市第一中学2018-2019学年高二下学期期末考试化学试题黑龙江省双鸭山市第一中学2019-2020学年高一上学期期末考试化学试题安徽省滁州市定远县重点中学2019-2020学年高二下学期期中考试化学试题(已下线)第三章 铁 金属材料(基础过关)-2020-2021学年高一化学单元测试定心卷(人教版2019必修第一册)河南省周口市中英文学校2021届高三上学期期中考试化学试题黑龙江嫩江市高级中学2021届高三上学期第二次月考化学试题江西省南昌市第二中学2020-2021学年高一上学期第三次月考化学试题甘肃省张掖市2020-2021学年高一上学期期末学业水平质量检测化学试题(已下线)专题05 金属及其重要化合物-备战2021届高考化学二轮复习题型专练安徽省郎溪中学、泾县中学2020-2021学年高一下学期3月联考化学试题四川省眉山市彭山区第一中学2020-2021学年高一4月月考化学试题(已下线)微专题02 以物质的量为中心的计算-备战2022年高考化学考点微专题(已下线)周末培优5 物质的量应用于化学方程式的计算专练-2021-2022学年高一化学课后培优练(人教版2019必修第一册)山东省新泰市新泰中学2022届高三第一次阶段性考试化学试题(已下线)易错专题25 物质的量在化学方程式计算中的应用-【突破易错·冲刺满分】2021-2022学年高一上学期化学期中期末易错专题(人教版2019)江西省丰城市第九中学2021-2022学年高三上学期第二次月考(日新班)化学试题黑龙江省七台河市勃利县高级中学2022-2023学年高三上学期11月期中考试化学试题
2 . 只用一种试剂即可鉴别 、
、 、
、 、
、 、
、 五种溶液,这种试剂是( )
五种溶液,这种试剂是( )
 、
、 、
、 、
、 、
、 五种溶液,这种试剂是( )
五种溶液,这种试剂是( )A. 溶液 溶液 | B. 溶液 溶液 |
C. 溶液 溶液 | D. 溶液 溶液 |
您最近一年使用:0次
2020-10-02更新
|
1247次组卷
|
2卷引用:人教版(2019)高一必修第一册 第三章 铁 金属材料 章末综合检测卷
3 . 抗酸药物的种类很多,其有效成分一般都是碳酸氢钠、碳酸钙、碳酸镁、氢氧化铝和氢氧化镁等化学物质。
(1)抗酸药物具有抗酸作用的原因是:______ 。
(2)某品牌抗酸药的主要成分有糖衣、碳酸镁、氢氧化铝、淀粉。
①写出该抗酸药发挥功效时的离子方程式:______ ,_______ 。
②淀粉在抗酸药中作填充剂、粘合剂,淀粉在人体内酶的催化作用下发生水解反应,最终转化为(写分子式)______ 。
(1)抗酸药物具有抗酸作用的原因是:
(2)某品牌抗酸药的主要成分有糖衣、碳酸镁、氢氧化铝、淀粉。
①写出该抗酸药发挥功效时的离子方程式:
②淀粉在抗酸药中作填充剂、粘合剂,淀粉在人体内酶的催化作用下发生水解反应,最终转化为(写分子式)
您最近一年使用:0次
名校
4 . 铝、铁是生产、生活中常见的金属,其合金与盐在各领域都有着广泛的应用。
(1)铝合金是一种建筑装潢材料,它具有坚硬、轻巧、耐用的特性。铝合金的下列性质与这些特性无关的是
(2)铝元素在周期表中的位置是_______ 。写出 与稀硫酸反应的离子方程式
与稀硫酸反应的离子方程式_______ 。铁粉与水蒸气在高温条件下反应,生成的固态产物是_______ 。
(3)焊接金属时常用的焊接液为氯化铵,其作用是消除焊接金属表面的铁锈。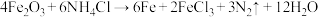 ;上述反应中当生成3.36L氮气(标准状况)时,转移的电子数为
;上述反应中当生成3.36L氮气(标准状况)时,转移的电子数为_______ 个,有同学认为,该反应产物中不应该有Fe生成,他的理由是(用化学方程式表示原因)_______ 。
(4)现有仪器和药品:试管和胶头滴管,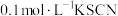 溶液、
溶液、 酸性
酸性 溶液、
溶液、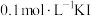 溶液、氯水等。请你设计一个简单实验,探究铁与稀硝酸完全反应后铁可能的价态,填写下列实验报告:
溶液、氯水等。请你设计一个简单实验,探究铁与稀硝酸完全反应后铁可能的价态,填写下列实验报告:
(1)铝合金是一种建筑装潢材料,它具有坚硬、轻巧、耐用的特性。铝合金的下列性质与这些特性无关的是
| A.不易生锈 | B.导电性好 | C.密度小 | D.硬度大 |
 与稀硫酸反应的离子方程式
与稀硫酸反应的离子方程式(3)焊接金属时常用的焊接液为氯化铵,其作用是消除焊接金属表面的铁锈。
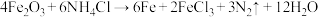 ;上述反应中当生成3.36L氮气(标准状况)时,转移的电子数为
;上述反应中当生成3.36L氮气(标准状况)时,转移的电子数为(4)现有仪器和药品:试管和胶头滴管,
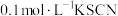 溶液、
溶液、 酸性
酸性 溶液、
溶液、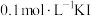 溶液、氯水等。请你设计一个简单实验,探究铁与稀硝酸完全反应后铁可能的价态,填写下列实验报告:
溶液、氯水等。请你设计一个简单实验,探究铁与稀硝酸完全反应后铁可能的价态,填写下列实验报告:| 实验步骤 | 操作 | 现象与结论 |
| 第一步 | 取少量液体装于试管,向试管中滴入几滴 溶液。 溶液。 | |
| 第二步 |  。 。 |
您最近一年使用:0次
2022-06-28更新
|
230次组卷
|
2卷引用:9.3.2合金及其应用(课后)-2019苏教版必修2课前课中课后
名校
解题方法
5 . 铝是地壳中含量最多的金属元素,铝及其化合物在生产和生活中有广泛的用途,请回答下列问题:
(1)我们知道,铝是一种活泼的金属,在常温下就能与空气中的氧气反应,但在日常生活中铝制品却司空见惯,原因是_______ ,铝制器皿无论盛放酸性或碱性溶液,均会被腐蚀,请写出铝与烧碱溶液发生反应的离子方程式:_______ 。
(2)高纯氧化铝常被用作荧光粉基体材料,制备高纯氧化铝要用化学方法,其中一种方法是将 溶液中的铝沉淀出来,再将生成的沉淀经脱水制得氧化铝。为完全沉淀
溶液中的铝沉淀出来,再将生成的沉淀经脱水制得氧化铝。为完全沉淀 溶液中的铝元素,可采用的方法是
溶液中的铝元素,可采用的方法是_______ 。
(3)胃舒平的有效成分是氢氧化铝,是治疗胃酸(盐酸)过多的常用药物,胃舒平治疗胃酸过多的原理是_______ (用离子方程式表示),小苏打片也可以治疗胃酸过多,小苏打片发挥功效的离子方程式为_______ 。

(1)我们知道,铝是一种活泼的金属,在常温下就能与空气中的氧气反应,但在日常生活中铝制品却司空见惯,原因是
(2)高纯氧化铝常被用作荧光粉基体材料,制备高纯氧化铝要用化学方法,其中一种方法是将
 溶液中的铝沉淀出来,再将生成的沉淀经脱水制得氧化铝。为完全沉淀
溶液中的铝沉淀出来,再将生成的沉淀经脱水制得氧化铝。为完全沉淀 溶液中的铝元素,可采用的方法是
溶液中的铝元素,可采用的方法是(3)胃舒平的有效成分是氢氧化铝,是治疗胃酸(盐酸)过多的常用药物,胃舒平治疗胃酸过多的原理是

您最近一年使用:0次
2021-01-28更新
|
235次组卷
|
3卷引用:3.2.1 铁合金 铝和铝合金 新型合金-2022-2023学年高一化学上学期课后培优分级练(人教版2019必修第一册)
(已下线)3.2.1 铁合金 铝和铝合金 新型合金-2022-2023学年高一化学上学期课后培优分级练(人教版2019必修第一册)山西省2020-2021学年高一上学期期末考试化学试题山西省长治市第一中学2020-2021学年高一上学期期末测试试题
6 . 下列实验操作、现象和结论均正确的是
| 实验操作 | 现象 | 结论 | |
| A | 将气体通入灼热的CuO固体 | 固体由黑色变为红色 | 该气体一定为CO |
| B | 向某溶液中加入1~2滴KSCN溶液 | 生成血红色沉淀 | 该溶液中含Fe3+ |
| C | 向Al(OH)3中加入HCl或NaOH溶液 | 固体均溶解 | Al(OH)3是两性氢氧化物 |
| D | 将氯气通入装有潮湿的有色布条的试剂瓶中 | 有色布条颜色褪去 | Cl2具有漂白性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2019-01-25更新
|
534次组卷
|
3卷引用:3.2.1 铁合金 铝和铝合金练习(2)——《高中新教材同步备课》(人教版 必修第一册)
(已下线)3.2.1 铁合金 铝和铝合金练习(2)——《高中新教材同步备课》(人教版 必修第一册)江苏省溧水高级中学2018-2019学年高一上学期期末考试化学试题河北省衡水市武强中学2021-2022学年高一上学期第三次月考化学试题
7 . 金属铝在生产生活中有着广泛的用途。回答下列问题:
(1)铝元素在周期表中的位置是_______________ 。
(2)比较原子结构示意图:它们的共同之处是___________  选填编号,下同
选填编号,下同 ;不同之处是
;不同之处是___________ 。
a.电子层数 b.次外层电子数 c.最外层电子数 d.质子数
(3)常温下铝制容器可以用来盛放浓硫酸而不被溶解,这种现象称为___________ 。
氢氧化铝和盐酸反应的化学方程式为_________________________________ 。
能把溶液中的铁离子和铝离子分离开的试剂是___________ 。 选填编号
选填编号
a.盐酸 b.硫酸铜溶液 c.氨水 d.氢氧化钠溶液
(1)铝元素在周期表中的位置是
(2)比较原子结构示意图:它们的共同之处是
 选填编号,下同
选填编号,下同 ;不同之处是
;不同之处是
a.电子层数 b.次外层电子数 c.最外层电子数 d.质子数
(3)常温下铝制容器可以用来盛放浓硫酸而不被溶解,这种现象称为
氢氧化铝和盐酸反应的化学方程式为
能把溶液中的铁离子和铝离子分离开的试剂是
 选填编号
选填编号
a.盐酸 b.硫酸铜溶液 c.氨水 d.氢氧化钠溶液
您最近一年使用:0次
8 . (1)某品牌抗酸药的主要成分有糖衣、氢氧化铝、淀粉、蛋白质。写出该抗酸药发挥功效时的离子方程式:_________________________________ ;淀粉、蛋白质在抗酸药中作填充剂、黏合剂,蛋白质在人体内酶的催化作用下发生水解反应,最终转化为_________________ 。
(2)阿司匹林是人们熟知的治感冒药,具有________ 作用,其化学名称是________ ,是一种重要的合成药物。
(2)阿司匹林是人们熟知的治感冒药,具有
您最近一年使用:0次
20-21高二上·全国·课时练习
解题方法
9 . 下列离子方程式书写正确的是
| A.硫酸铝中加入过量氨水:Al3++3OH-= Al(OH)3↓ |
| B.氢氧化铝跟盐酸反应:2Al(OH)3+6H+=2Al3++6H2O |
C.硫酸铜与氢氧化钡溶液反应:Ba2++SO =BaSO4↓ =BaSO4↓ |
D.偏铝酸钠溶液与过量稀硝酸反应:AlO +H++H2O=Al(OH)3↓ +H++H2O=Al(OH)3↓ |
您最近一年使用:0次
名校
10 . 下列有关物质的性质与用途具有对应关系的是
| A.明矾易溶于水,可用作净水剂 |
| B.石英的熔点高,可用于制作光导纤维 |
| C.NH4HCO3受热易分解,可用作食品膨化剂 |
| D.氢氧化铝具有弱酸性,可用于治疗胃酸过多 |
您最近一年使用:0次
2020-03-06更新
|
277次组卷
|
2卷引用:【百强校】江苏省启东中学2020年人教版高中化学必修一期末复习卷(三)



