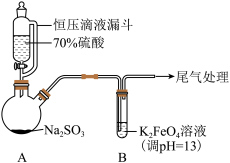
1 . 某实验小组探究SO2与K2FeO4的反应,实验如下。
资料:i.K2FeO4为紫色固体,微溶于KOH溶液;具有强氧化性,在酸性或中性溶液中快速产生O2,在碱性溶液中较稳定。
ii.Fe3+可以与C2O 形成[Fe(C2O4)3]3-;
形成[Fe(C2O4)3]3-;
(1)A中产生SO2的化学方程式为___________ 。
(2)暗红褐色沉淀X可能含Fe3+、OH-、SO 、SO
、SO ,检验如下:
,检验如下:
实验二:向X中加入足量盐酸,沉淀溶解。取少量溶液,滴加KSCN溶液后变红。证明溶液中存在___________ 。另取少量溶液滴加BaCl2溶液,产生白色沉淀,但不能确认含有SO ,原因是
,原因是___________ 。
实验三:向X中加入H2C2O4溶液,沉淀溶解。继续滴加BaCl2溶液,产生白色沉淀,过滤后,向沉淀中加入盐酸,白色沉淀溶解。确认X中不含SO 。
。
实验三中用H2C2O4溶液溶解沉淀的目的是:___________ 。
实验四:向X中加入足量盐酸,沉淀溶解。加入几滴碘水(含淀粉),蓝色立即褪去。静置,一段时间后蓝色复现,振荡,不褪色。
结合离子方程式解释沉淀溶解后的现象:___________ 。
(3)查阅资料:a.Fe3+、SO 、H2O(或OH﹣)会形成配合物HOFeOSO2。
、H2O(或OH﹣)会形成配合物HOFeOSO2。 和O2在金属离子的催化作用下产生具有强氧化性的过一硫酸(HSO
和O2在金属离子的催化作用下产生具有强氧化性的过一硫酸(HSO
①向溶液Y中滴加2滴KSCN溶液,未见红色;再加几滴6mol·L-1盐酸,溶液变红。溶液Y中存在Fe(Ⅲ),但直接滴加KSCN溶液未见红色的原因是___________ 。
②取出部分实验一中的橙色溶液,久置不褪色。结合资料a中过程ii分析实验一中溶液最终“几乎无色”的原因:___________ 。
总结:SO2与K2FeO4发生了氧化还原反应和复分解反应,并且遵循化学反应速率和限度规律。
资料:i.K2FeO4为紫色固体,微溶于KOH溶液;具有强氧化性,在酸性或中性溶液中快速产生O2,在碱性溶液中较稳定。
ii.Fe3+可以与C2O
 形成[Fe(C2O4)3]3-;
形成[Fe(C2O4)3]3-;| 装置 | 操作及现象 |
| 实验一:向B中通入SO2,产生暗红褐色沉淀X和溶液Y(略显红色);继续通入SO2一段时间后,溶液呈红色,继而变为橙色,最终沉淀消失,溶液几乎无色。 |
(1)A中产生SO2的化学方程式为
(2)暗红褐色沉淀X可能含Fe3+、OH-、SO
 、SO
、SO ,检验如下:
,检验如下:实验二:向X中加入足量盐酸,沉淀溶解。取少量溶液,滴加KSCN溶液后变红。证明溶液中存在
 ,原因是
,原因是实验三:向X中加入H2C2O4溶液,沉淀溶解。继续滴加BaCl2溶液,产生白色沉淀,过滤后,向沉淀中加入盐酸,白色沉淀溶解。确认X中不含SO
 。
。实验三中用H2C2O4溶液溶解沉淀的目的是:
实验四:向X中加入足量盐酸,沉淀溶解。加入几滴碘水(含淀粉),蓝色立即褪去。静置,一段时间后蓝色复现,振荡,不褪色。
结合离子方程式解释沉淀溶解后的现象:
(3)查阅资料:a.Fe3+、SO
 、H2O(或OH﹣)会形成配合物HOFeOSO2。
、H2O(或OH﹣)会形成配合物HOFeOSO2。
 和O2在金属离子的催化作用下产生具有强氧化性的过一硫酸(HSO
和O2在金属离子的催化作用下产生具有强氧化性的过一硫酸(HSO
①向溶液Y中滴加2滴KSCN溶液,未见红色;再加几滴6mol·L-1盐酸,溶液变红。溶液Y中存在Fe(Ⅲ),但直接滴加KSCN溶液未见红色的原因是
②取出部分实验一中的橙色溶液,久置不褪色。结合资料a中过程ii分析实验一中溶液最终“几乎无色”的原因:
总结:SO2与K2FeO4发生了氧化还原反应和复分解反应,并且遵循化学反应速率和限度规律。
您最近一年使用:0次
2024-04-15更新
|
617次组卷
|
3卷引用:辽宁省大连市大连第二十四中学2023-2024学年高一下学期期中考试化学试卷
辽宁省大连市大连第二十四中学2023-2024学年高一下学期期中考试化学试卷北京市朝阳区2023-2024学年高三下学期一模化学试题(已下线)压轴题12?化学实验综合题(5大题型+方法总结+压轴题速练)-2024年高考化学压轴题专项训练(新高考通用)
解题方法
2 . 高铁酸盐 是优良的多功能水处理剂。
是优良的多功能水处理剂。 为紫色固体,可溶于水,微溶于浓
为紫色固体,可溶于水,微溶于浓 溶液,难溶于有机物;在
溶液,难溶于有机物;在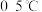 、强碱性溶液中比较稳定,在酸性、中性溶液中易分解放出
、强碱性溶液中比较稳定,在酸性、中性溶液中易分解放出 某实验小组制备高铁酸钾并测定产品纯度。回答下列问题:
某实验小组制备高铁酸钾并测定产品纯度。回答下列问题:
制备 (装置如图所示,夹持、加热等装置略)
(装置如图所示,夹持、加热等装置略)
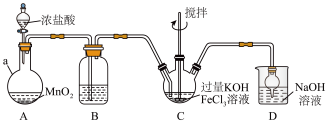
(1)仪器 的名称是
的名称是______ ,装置B中除杂质所用试剂是______ 。
(2)C中发生反应的离子方程式为______ 。
(3) 中反应为放热反应,而反应温度须控制在0∼5℃,采用的控温方法为,
中反应为放热反应,而反应温度须控制在0∼5℃,采用的控温方法为,______ ,反应中 必须过量的原因是
必须过量的原因是______ 。
(4)D中反应可制备漂白液,反应的离子方程式为______ 。
(5) 中由
中由 制备
制备 ,若生成
,若生成 ,则该反应过程中转移的电子数目
,则该反应过程中转移的电子数目______ 。
 是优良的多功能水处理剂。
是优良的多功能水处理剂。 为紫色固体,可溶于水,微溶于浓
为紫色固体,可溶于水,微溶于浓 溶液,难溶于有机物;在
溶液,难溶于有机物;在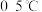 、强碱性溶液中比较稳定,在酸性、中性溶液中易分解放出
、强碱性溶液中比较稳定,在酸性、中性溶液中易分解放出 某实验小组制备高铁酸钾并测定产品纯度。回答下列问题:
某实验小组制备高铁酸钾并测定产品纯度。回答下列问题:制备
 (装置如图所示,夹持、加热等装置略)
(装置如图所示,夹持、加热等装置略)
(1)仪器
 的名称是
的名称是(2)C中发生反应的离子方程式为
(3)
 中反应为放热反应,而反应温度须控制在0∼5℃,采用的控温方法为,
中反应为放热反应,而反应温度须控制在0∼5℃,采用的控温方法为, 必须过量的原因是
必须过量的原因是(4)D中反应可制备漂白液,反应的离子方程式为
(5)
 中由
中由 制备
制备 ,若生成
,若生成 ,则该反应过程中转移的电子数目
,则该反应过程中转移的电子数目
您最近一年使用:0次
3 .  化学性质活泼,能与许多物质反应。某实验小组利用下列装置(夹持装置已省略)探究
化学性质活泼,能与许多物质反应。某实验小组利用下列装置(夹持装置已省略)探究 与
与 的反应机理,实验步骤如下:
的反应机理,实验步骤如下:
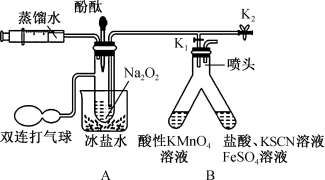
Ⅰ.打开 、
、 ,通过注射器注入适量蒸馏水,使固体全部溶解(未见气泡产生);
,通过注射器注入适量蒸馏水,使固体全部溶解(未见气泡产生);
Ⅱ.将部分液体转移至B中;
Ⅲ.向A剩余的溶液中滴加几滴酚酞试液。
请回答下列问题:
(1)“步骤Ⅱ”B中左侧溶液褪色且有气泡产生,右侧溶液变为红色。
①将部分液体转移至B中的具体操作为_______ 。
②右侧溶液变红色的原因是_______ (用离子方程式解释)。
③左侧 参与反应的离子方程式为
参与反应的离子方程式为_______ 。
(2)若向“步骤Ⅱ”A的剩余溶液中加入 时,有大量气泡产生。
时,有大量气泡产生。
① 在该反应中的作用为
在该反应中的作用为_______ 。
②“步骤Ⅲ”的现象为_______ ;由此推测 与
与 反应的第一步为
反应的第一步为_______ (写出化学方程式)。
(3)过氧化钠可与铝粉发生反应: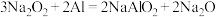 ,该反应可以体现
,该反应可以体现 具有
具有_______ (填“氧化性”、“还原性”或“既有氧化性,也有还原性”)。
 化学性质活泼,能与许多物质反应。某实验小组利用下列装置(夹持装置已省略)探究
化学性质活泼,能与许多物质反应。某实验小组利用下列装置(夹持装置已省略)探究 与
与 的反应机理,实验步骤如下:
的反应机理,实验步骤如下:
Ⅰ.打开
 、
、 ,通过注射器注入适量蒸馏水,使固体全部溶解(未见气泡产生);
,通过注射器注入适量蒸馏水,使固体全部溶解(未见气泡产生);Ⅱ.将部分液体转移至B中;
Ⅲ.向A剩余的溶液中滴加几滴酚酞试液。
请回答下列问题:
(1)“步骤Ⅱ”B中左侧溶液褪色且有气泡产生,右侧溶液变为红色。
①将部分液体转移至B中的具体操作为
②右侧溶液变红色的原因是
③左侧
 参与反应的离子方程式为
参与反应的离子方程式为(2)若向“步骤Ⅱ”A的剩余溶液中加入
 时,有大量气泡产生。
时,有大量气泡产生。①
 在该反应中的作用为
在该反应中的作用为②“步骤Ⅲ”的现象为
 与
与 反应的第一步为
反应的第一步为(3)过氧化钠可与铝粉发生反应:
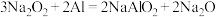 ,该反应可以体现
,该反应可以体现 具有
具有
您最近一年使用:0次
2023-01-04更新
|
772次组卷
|
3卷引用:辽宁省重点高中2022-2023学年高一上学期期末联考化学试题
4 . 某新型纳米材料氧缺位铁酸盐ZnFe2Ox(3<x<4),能在常温下将工业废气中的SO2、NO2等转化为单质而除去,由锌灰(含ZnO和少量PbO、CuO、Fe2O3等)为主要原料制备氧缺位铁酸盐及其转化废气的流程如图所示,下列说法不正确 的是
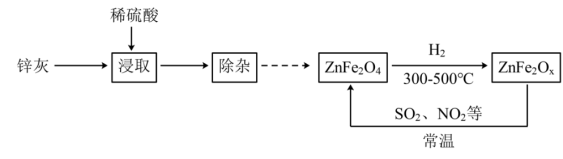

| A.浸取时为了提高酸浸效率,可以搅拌或延长浸取时间 |
| B.“除杂”过程中需要加入足量锌粉等操作,与锌粉反应的金属离子有Fe3+、Cu2+ |
| C.除去SO2时,ZnFe2Ox在反应中表现出氧化性 |
| D.ZnFe2O4与H2反应制得1molZnFe2Ox时,转移的电子物质的量为(8-2x)mol |
您最近一年使用:0次
2022-05-14更新
|
1326次组卷
|
6卷引用:选择题6-10
(已下线)选择题6-10江苏省连云港市2021-2022学年高三高考考前模拟考试(一)化学试题江苏省徐州市2021-2022学年高一下学期期末抽测化学试题(已下线)考点14 铁及其化合物-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)考点14 铁及其化合物(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)江苏省扬州市宝应县2023-2024学年高三上学期期末模拟化学试卷
5 . 化合物X在一定条件下可发生如图转化,有关叙述错误的是


A.溶液C到溶液D中发生的离子方程式为:Fe3++3SCN— Fe(SCN)3 Fe(SCN)3 |
| B.E为CO,物质的量为0.05mol |
| C.X为Fe(CO)4 |
| D.过量的稀硫酸若换成盐酸,会造成环境污染 |
您最近一年使用:0次
2021-06-30更新
|
2098次组卷
|
7卷引用:辽宁省实验中学2022届高三第一次阶段性考试化学试题
辽宁省实验中学2022届高三第一次阶段性考试化学试题安徽省淮北市2021届高三第一次模拟考试化学试题(已下线)专题三 能力提升检测卷 (测) — 2022年高考化学一轮复习讲练测(新教材新高考)(已下线)专题06 常见金属及其化合物-备战2022年高考化学学霸纠错(全国通用)(已下线)专题14物质的反应和转化-三年(2020~2022)高考真题汇编(全国卷)(已下线)专题13物质的反应和转化-2022年高考真题+模拟题汇编(全国卷)(已下线)专题14物质的反应和转化-五年(2018~2022)高考真题汇编(全国卷)
名校
解题方法
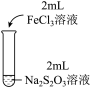
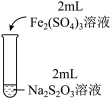
6 . 某实验小组对Na2S2O3分别与FeCl3、Fe2(SO4)3的反应进行实验探究。
实验药品:0.1mol/LNa2S2O3溶液(pH=7);0.1mol/LFeCl3溶液(pH=1);0.05mol/LFe2(SO4)3溶液(pH=1)。
实验过程
资料:ⅰ.Na2S2O3在酸性条件下不稳定,发生自身氧化还原反应;
ⅱ.Fe3++ ⇌Fe(S2O3)+(暗紫色),Fe2+遇
⇌Fe(S2O3)+(暗紫色),Fe2+遇 无明显现象
无明显现象
(1)配制FeCl3溶液时,需要用盐酸酸化,结合离子方程式解释原因:_______ 。
(2)对实验Ⅰ中现象产生的原因探究如下:
①证明有Fe2+生成:取实验Ⅰ中褪色后溶液,加入1~2滴K3[Fe(CN)6]溶液,观察到_______ 。
②实验I中紫色褪去时 被氧化成
被氧化成 ,相关反应的离子方程式是
,相关反应的离子方程式是_______ 。
③实验I和Ⅱ对比,Ⅰ中出现淡黄色浑浊,而Ⅱ中不出现淡黄色浑浊的原因是_______ 。
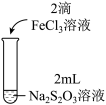
(3)为探究实验Ⅱ和Ⅲ中紫色褪去快慢不同的原因,设计实验如下:
①试剂X是_______ 。
②由实验Ⅳ和实验Ⅴ得出的结论是_______ 。
实验药品:0.1mol/LNa2S2O3溶液(pH=7);0.1mol/LFeCl3溶液(pH=1);0.05mol/LFe2(SO4)3溶液(pH=1)。
实验过程
| 实验编号 | Ⅰ | Ⅱ | Ⅲ |
| 实验操作 |
|
|
|
| 实验现象 | 溶液呈紫色, 静置后紫色迅速褪去, 久置后出现淡黄色浑浊 | 溶液呈紫色, 静置后紫色褪去, 久置后不出现淡黄色浑浊 | 溶液呈紫色, 静置后紫色缓慢褪去, 久置后不出现淡黄色浑浊 |
ⅱ.Fe3++
 ⇌Fe(S2O3)+(暗紫色),Fe2+遇
⇌Fe(S2O3)+(暗紫色),Fe2+遇 无明显现象
无明显现象(1)配制FeCl3溶液时,需要用盐酸酸化,结合离子方程式解释原因:
(2)对实验Ⅰ中现象产生的原因探究如下:
①证明有Fe2+生成:取实验Ⅰ中褪色后溶液,加入1~2滴K3[Fe(CN)6]溶液,观察到
②实验I中紫色褪去时
 被氧化成
被氧化成 ,相关反应的离子方程式是
,相关反应的离子方程式是③实验I和Ⅱ对比,Ⅰ中出现淡黄色浑浊,而Ⅱ中不出现淡黄色浑浊的原因是
(3)为探究实验Ⅱ和Ⅲ中紫色褪去快慢不同的原因,设计实验如下:
| 实验编号 | Ⅳ | Ⅴ |
| 实验操作 | 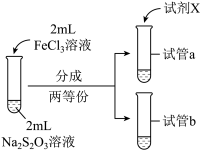 |  |
| 实验现象 | 紫色褪去时间a>b | 紫色褪去时间c<d |
②由实验Ⅳ和实验Ⅴ得出的结论是
您最近一年使用:0次
2021-01-20更新
|
1043次组卷
|
7卷引用:辽宁省葫芦岛市2021届高考第一次模拟考试化学试题
辽宁省葫芦岛市2021届高考第一次模拟考试化学试题北京市东城区2021届高三上学期期末教学统一检测化学试题(已下线)大题04 无机定量与探究实验-【考前抓大题】备战2021年高考化学(全国通用)(已下线)解密07 非金属及其化合物(分层训练)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)(已下线)解密07 非金属及其化合物(分层训练)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练北京市清华大学附属中学2022-2023学年高二上学期期末化学试题北京理工大学附属中学2023-2024学年高三上学期10月月考化学试题