解题方法
1 . 废旧计算机的某些部件含有Zn、Fe、Cu、Ag、Pt(铂)、Au(金)等金属,经物理方法初步处理后,与足量稀盐酸充分反应,然后过滤。则剩余的固体中不含有的金属是( )
| A.Cu、Ag |
| B.Fe、Zn |
| C.Pt、Cu |
| D.Ag、Au |
您最近一年使用:0次
解题方法
2 . 将Na2O2投入FeCl3溶液中,对观察到的现象描述准确的是 ( )
| A.生成白色沉淀 |
| B.既有气泡产生,又生成红褐色沉淀 |
| C.既有气泡产生,又生成白色沉淀 |
| D.有气泡产生,无沉淀生成 |
您最近一年使用:0次
解题方法
3 . 下列叙述不正确的是( )
| 选项 | 被提纯物质 | 杂质 | 除杂试剂或方法 |
| A | FeCl3溶液 | FeCl2 | 通入适量Cl2 |
| B | FeCl2溶液 | FeCl3 | 加入过量铁粉并过滤 |
| C | 铁粉 | 铝粉 | 加入过量NaOH溶液并过滤 |
| D | Fe(OH)3溶液 | Fe(OH)2 | 在空气中灼烧 |
| A.A |
| B.B |
| C.C |
| D.D |
您最近一年使用:0次
4 . 某同学对未知物A盐的水溶液进行了鉴定,实验过程及现象如图所示:
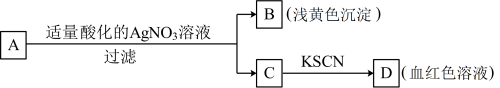
已知硝酸能将Fe2+氧化为Fe3+。回答下列问题:
(1) A可能是________________ ;
(2) B的化学式是______________ ,D的化学式是____________ ;
(3)滤液C中一定含有的阳离子Fe3+是____________ 。

已知硝酸能将Fe2+氧化为Fe3+。回答下列问题:
(1) A可能是
(2) B的化学式是
(3)滤液C中一定含有的阳离子Fe3+是
您最近一年使用:0次
解题方法
5 . 检验用硫酸亚铁制得的硫酸铁中是否含有硫酸亚铁,可选用的试剂是( )
| A.NaOH |
| B.KMnO4 |
| C.KSCN |
| D.铁 |
您最近一年使用:0次
2020-01-28更新
|
139次组卷
|
3卷引用:鲁教版高中化学必修1第二章《元素与物质世界》测试卷1
解题方法
6 . 下列物质与铁反应后的生成物,能使硫氰化钾溶液变为红色的是( )
| A.盐酸 | B.氯气 | C.硫酸铜溶液 | D.稀硫酸 |
您最近一年使用:0次
2020-01-10更新
|
69次组卷
|
2卷引用:人教版高中化学必修1第三章《金属及其化合物》测试卷5
名校
解题方法
7 . 在探究下列物质性质或组成的实验中,结论不正确 的是
| A.将二氧化硫通入酸性KMnO4溶液中,紫色褪去,证明二氧化硫有还原性 |
| B.向某溶液中加入KSCN溶液,溶液变成红色,证明原溶液中含有Fe3+ |
| C.将铝片放入冷浓硝酸中,无明显现象,证明浓硝酸与铝片不反应 |
| D.向某无色溶液中加入氢氧化钠溶液并加热,产生能使湿润红色石蕊试纸变蓝的气体,证明原溶液中一定有NH4+ |
您最近一年使用:0次
2019-12-20更新
|
732次组卷
|
6卷引用:人教版(2019)高中化学必修第二册第五章《化学生产中的重要非金属元素》检测题
名校
解题方法
8 . 已知:某些强酸盐的水溶液呈中性,如NaCl溶液,某些弱酸盐的水溶液呈碱性,如Na2CO3溶液。请根据如下图所示转化关系回答有关问题。A和B均为焰色反应呈黄色的水溶液,A呈中性,B呈碱性并具有强氧化性。

(1)写出C的化学式:________ 。
(2)依次写出A→D和D→E(E中含有某+5价元素的含氧酸根离子)的离子方程式:___________________ ,_____________________ 。
(3)写出将SO2气体通入K溶液中发生反应的离子方程式:____________ 。
(4)检验K溶液中阳离子的简易方法是__________ 。

(1)写出C的化学式:
(2)依次写出A→D和D→E(E中含有某+5价元素的含氧酸根离子)的离子方程式:
(3)写出将SO2气体通入K溶液中发生反应的离子方程式:
(4)检验K溶液中阳离子的简易方法是
您最近一年使用:0次
2019-12-18更新
|
194次组卷
|
2卷引用:人教版(2019)高中化学必修第二册第五章《化学生产中的重要非金属元素》检测题
解题方法
9 . 填空题
(1)“金属钙线”是炼制优质钢材的脱氧脱磷剂,某“金属钙线”的主要成分为金属M和金属钙Ca,并含有3.5%(质量分数)CaO.
①Ca元素原子结构示意图________ ,Ca(OH)2碱性比Mg(OH)2______ (填“强”或“弱”).
②配平用“金属钙线”脱氧脱磷的方程式:___ P +____ FeO +____ CaO
____ Ca3(PO4)2 +____ Fe
③将“金属钙线”试样溶于稀盐酸后,加入过量NaOH溶液,生成白色絮状沉淀并迅速变成灰绿色,最后变成红褐色的M(OH)n,该颜色变化过程的化学方程式为:_____________________ ,实验室检测Mn+最常用的试剂是___________ (填化学式)
④取3.2 g“金属钙线”试样,与水充分反应,生成448 mL H2(标准状况),在所得溶液中通入适量的CO2,最多能得到CaCO3________ g,“金属钙线”试样中金属M的质量分数为______ .
(2)氢化钙(CaH2)固体登山运动员常用的能源提供剂
①写出CaH2与水反应的化学方程式__________________ ,该反应的氧化产物是___ .
②请你设计一个实验,用化学方法区分钙与氢化钙,写出实验简要步骤及观察到的现象_____ .
③登山运动员常用氢化钙作为能源提供剂,与氢气相比,其优点是_______________________ .
(1)“金属钙线”是炼制优质钢材的脱氧脱磷剂,某“金属钙线”的主要成分为金属M和金属钙Ca,并含有3.5%(质量分数)CaO.
①Ca元素原子结构示意图
②配平用“金属钙线”脱氧脱磷的方程式:

③将“金属钙线”试样溶于稀盐酸后,加入过量NaOH溶液,生成白色絮状沉淀并迅速变成灰绿色,最后变成红褐色的M(OH)n,该颜色变化过程的化学方程式为:
④取3.2 g“金属钙线”试样,与水充分反应,生成448 mL H2(标准状况),在所得溶液中通入适量的CO2,最多能得到CaCO3
(2)氢化钙(CaH2)固体登山运动员常用的能源提供剂
①写出CaH2与水反应的化学方程式
②请你设计一个实验,用化学方法区分钙与氢化钙,写出实验简要步骤及观察到的现象
③登山运动员常用氢化钙作为能源提供剂,与氢气相比,其优点是
您最近一年使用:0次
解题方法
10 . 向一定量的FeO,Fe,Fe3O4的混合物中加入100mL 1mol/L的盐酸,恰好使混合物完全溶解,放出224mL(标准状况)的气体,在所得溶液中加入KSCN溶液无血红色出现. 若用足量的CO在高温下还原相同质量的此混合物,能得到铁的质量是
| A.11.2 g | B.5.6 g | C.2.8 g | D.1.4g |
您最近一年使用:0次
2019-12-08更新
|
828次组卷
|
8卷引用:人教版高一化学必修1第一章—第三章综合测试题
人教版高一化学必修1第一章—第三章综合测试题人教版2017-2018学年高一化学必修1:3.2 几种重要的金属化合物 同步测试22020届高三化学无机化学二轮专题复习——铁及其化合物的相关计算【精编20题】人教版(2019)高一必修第一册第三章 铁 金属材料 第一节 铁及其化合物 课时2 铁盐、亚铁盐鲁科版(2019)高一必修第一册第三章第1节 铁的多样性 课时2 铁及其化合物之间的转化关系(已下线)专题05 金属及其重要化合物-备战2021届高考化学二轮复习题型专练云南省华宁二中2019-2020学年高一上学期期末考试化学试题云南省勐腊县第二中学2019-2020学年高一上学期期末考试化学试题



