1 . 下列操作中,溶液的颜色不发生变化的是
| A.氯化铁溶液中加入足量铜粉,充分振荡 |
| B.氧化铜加入到稀硫酸中 |
| C.氧化镁固体加入稀盐酸中,完全溶解 |
| D.氯化铁溶液中滴加硫氰化钾(KSCN)溶液 |
您最近一年使用:0次
名校
解题方法
2 . 实验室有一瓶失去标签的溶液,以下方法能证明溶液中含有Fe3+的是
| A.品尝味道 |
| B.能与KSCN溶液显红色 |
| C.与NaOH溶液生成白色沉淀 |
| D.观察溶液的颜色为浅绿色 |
您最近一年使用:0次
2021-06-15更新
|
593次组卷
|
5卷引用:第三章 铁 金属材料(A卷·知识通关练)-【单元测试】2022-2023学年高一化学分层训练AB卷(人教版2019必修第一册)
(已下线)第三章 铁 金属材料(A卷·知识通关练)-【单元测试】2022-2023学年高一化学分层训练AB卷(人教版2019必修第一册)宁夏青铜峡市高级中学2020-2021学年高一下学期学考模拟化学试题(已下线)微专题13 亚铁离子、三价铁离子的性质及检验-备战2022年高考化学考点微专题广东省湛江市第二十一中学2022-2023学年高一下学期期中考试(学考)化学试题(已下线)专题九 铁及其化合物
3 . 为了探究铁及其化合物的氧化性或还原性,某同学设计如下实验操作,对应的实验现象、实验结论及离子方程式均正确的是
| 选项 | 实验操作 | 实验现象 | 实验结论 | 离子方程式 |
| A | 向 溶液中加入 溶液中加入 片 片 | 浅绿色溶液变为无色,溶液中有黑色固体生成 |  具有还原性 具有还原性 |  |
| B | 向 溶液中滴加新制氯水 溶液中滴加新制氯水 | 浅绿色溶液变为棕黄色 |  具有还原性 具有还原性 | 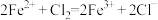 |
| C | 向 溶液中加入铁粉 溶液中加入铁粉 | 棕黄色溶液变为浅绿色 |  具有还原性 具有还原性 | 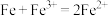 |
| D | 向 溶液中加入铜粉 溶液中加入铜粉 | 蓝色溶液变为棕黄色 |  具有氧化性 具有氧化性 | 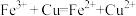 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2021-06-05更新
|
1081次组卷
|
8卷引用:第三章 铁 金属材料(B卷·能力提升练)-【单元测试】2022-2023学年高一化学分层训练AB卷(人教版2019必修第一册)
(已下线)第三章 铁 金属材料(B卷·能力提升练)-【单元测试】2022-2023学年高一化学分层训练AB卷(人教版2019必修第一册)(苏教版2019)必修第二册专题9 金属与人类文明 第二单元 探究铁及其化合物的转化(已下线)微专题13 亚铁离子、三价铁离子的性质及检验-备战2022年高考化学考点微专题(已下线)3.1.2 铁盐和亚铁盐-2021-2022学年高一化学课后培优练(人教版2019必修第一册)重庆市万州第二高级中学2022-2023学年高一上学期12月线上考试化学试题内蒙古巴彦淖尔市第一中学2022-2023学年高一上学期1月期末考试化学试题湖南省泸溪县第一中学等多校联考2023-2024学年高二上学期8月月考化学试题云南省保山市腾冲市第八中学2023--2024学年高一上学期期末化学强化训练
4 . 从古至今,铁及其化合物在人类的生产生活中都起到了巨大的作用。
(1)①古代中国四大发明之一指南针由天然磁石制成的, 其主要成分:___________ (填化学式)
②所含铁元素既有氧化性又有还原性的物质是___________ 。
A.Fe B. FeCl3 C.FeO D.FeSO4 E.Fe (OH)3
(2)①在现代半导体工业生产中,常利FeCl3腐蚀铜的原理制作印刷线路板,该原理的化学方程式为:___________ 。
②氯化铁溶液中同时加入铁粉和铜粉,反应结束后烧杯底部不可能出现的是___________
A.有铁无铜 B. 有铜无铁 C.有铁有铜 D.无铁无铜
(3)实验室在配制FeSO4溶液时,为了防止FeSO4溶液变质,经常会向其中加入一些铁粉,其原因是___________ (用离子方程式表示)。
(4)为证明某溶液中不含Fe3+而可能含有Fe2+,进行如下实验操作时最佳顺序:___________ 。
①加入适量的氯水 ②加入足量酸性KMnO4溶液 ③加入KSCN溶液
A.①③ B.③② C.③① D.①②③
(1)①古代中国四大发明之一指南针由天然磁石制成的, 其主要成分:
②所含铁元素既有氧化性又有还原性的物质是
A.Fe B. FeCl3 C.FeO D.FeSO4 E.Fe (OH)3
(2)①在现代半导体工业生产中,常利FeCl3腐蚀铜的原理制作印刷线路板,该原理的化学方程式为:
②氯化铁溶液中同时加入铁粉和铜粉,反应结束后烧杯底部不可能出现的是
A.有铁无铜 B. 有铜无铁 C.有铁有铜 D.无铁无铜
(3)实验室在配制FeSO4溶液时,为了防止FeSO4溶液变质,经常会向其中加入一些铁粉,其原因是
(4)为证明某溶液中不含Fe3+而可能含有Fe2+,进行如下实验操作时最佳顺序:
①加入适量的氯水 ②加入足量酸性KMnO4溶液 ③加入KSCN溶液
A.①③ B.③② C.③① D.①②③
您最近一年使用:0次
2021-04-29更新
|
1020次组卷
|
6卷引用:第三章 铁 金属材料(A卷·知识通关练)-【单元测试】2022-2023学年高一化学分层训练AB卷(人教版2019必修第一册)
(已下线)第三章 铁 金属材料(A卷·知识通关练)-【单元测试】2022-2023学年高一化学分层训练AB卷(人教版2019必修第一册)(已下线)【浙江新东方】【2021.4.27】【宁波】【高一上】【高中化学】【00147】河北省邯郸市大名县第一中学2020-2021学年高一下学期5月月考化学试题(已下线)3.1.2 铁盐和亚铁盐-2021-2022学年高一化学课后培优练(人教版2019必修第一册)(已下线)易错专题23 Fe2+和Fe3+的检验与转化-【突破易错·冲刺满分】2021-2022学年高一上学期化学期中期末易错专题(人教版2019)广东省深圳市观澜中学2021-2022学年高一上学期12月月考质量检测化学试题
21-22高一上·浙江·阶段练习
解题方法
5 . 某班同学用如下实验探究Fe2+、Fe3+的性质。回答下列问题:
(1)分别取一定量氯化铁、氯化亚铁固体,均配制成0.1 mol/L的溶液。为防止Fe2+被氧化,FeCl2溶液中需加入___________ 反应的化学方程式为___________ 。
(2)甲组同学取2 mL FeCl2溶液,加入1滴KSCN溶液,再加入几滴氯水,溶液变红,说明___________ 。
(3)乙组同学认为甲组的实验不够严谨,该组同学在2 mLFeCl2溶液中先加入0.5 mL煤油,再于液面下依次加入1滴KSCN溶液和几滴氯水,溶液变红,煤油的作用是___________ 。
(4)丙组同学取5 mL 0.1 mol/LKI溶液,加入6 mL 0.1 mol/LFeCl3溶液混合。分别取2 mL此溶液于3支试管中进行如下实验:
①第一支试管中加入1滴淀粉溶液,溶液显___________ 色;
②第二支试管中加入1滴K3[Fe(CN)6]溶液,生成蓝色沉淀;
③第三支试管中加入1滴KSCN溶液,溶液变红。
实验②检验的离子可能是___________ (填离子符号);写出KI与FeCl3反应的离子方程式___________ 。
(1)分别取一定量氯化铁、氯化亚铁固体,均配制成0.1 mol/L的溶液。为防止Fe2+被氧化,FeCl2溶液中需加入
(2)甲组同学取2 mL FeCl2溶液,加入1滴KSCN溶液,再加入几滴氯水,溶液变红,说明
(3)乙组同学认为甲组的实验不够严谨,该组同学在2 mLFeCl2溶液中先加入0.5 mL煤油,再于液面下依次加入1滴KSCN溶液和几滴氯水,溶液变红,煤油的作用是
(4)丙组同学取5 mL 0.1 mol/LKI溶液,加入6 mL 0.1 mol/LFeCl3溶液混合。分别取2 mL此溶液于3支试管中进行如下实验:
①第一支试管中加入1滴淀粉溶液,溶液显
②第二支试管中加入1滴K3[Fe(CN)6]溶液,生成蓝色沉淀;
③第三支试管中加入1滴KSCN溶液,溶液变红。
实验②检验的离子可能是
您最近一年使用:0次
10-11高三上·吉林长春·期中
名校
解题方法
6 . 把一定量铁粉放入氯化铁溶液中,完全反应后,所得溶液中Fe2+和Fe3+的溶度恰好相等,则未反应的Fe3+和已反应的Fe3+的物质的量的比为
| A.1∶1 | B.1∶2 | C.3∶2 | D.2∶3 |
您最近一年使用:0次
2021-04-15更新
|
1217次组卷
|
85卷引用:2018-2019学年苏教版高中化学必修一 专题综合测评3
2018-2019学年苏教版高中化学必修一 专题综合测评3鲁科版高中化学必修1第二章《元素与物质世界》测试卷(已下线)第03章 铁 金属材料(A卷基础强化篇)——2020-2021学年高一化学必修第一册同步单元AB卷(新教材人教版)(已下线)吉林省长春市十一高中2010-2011学年度高三上学期期中考(已下线)2011届陕西省西安交大阳光中学高三上学期期中考试化学卷(已下线)2010年福建省三明一中高一上学期期中考试化学卷(已下线)2010年上海市吴淞中学高二上学期期中考试化学试卷(已下线)2010—2011学年海南省洋浦中学高一上学期期末考试化学试卷(已下线)2011-2012学年甘肃省武威第五中学高一期末考试化学试卷(已下线)2011-2012学年江西省赣州市信丰县信丰中学高一第二次月考化学试卷(已下线)2011-2012学年甘肃省白银市平川中恒学校高一上学期期末考试化学试卷(已下线)2011-2012学年吉林省长春外国语学校高一上学期期末考试文科化学试卷(已下线)2011-2012学年吉林省长春市十一高中高一上学期期末考试化学试卷(已下线)2011—2012学年海南省洋浦中学高一第一学期期末考试化学试卷(已下线)2011-2012学年云南省玉溪一中高一下学期期中考试化学试卷(已下线)2012-2013学年福建省福清东张中学高一上学期期末考试化学试卷(已下线)2012-2013学年陕西省宝鸡中学高一上学期期末考试化学试卷(已下线)2013-2014学年福建省厦门市高一上学期期末质量检测模拟化学试卷(已下线)2013-2014学年北京市西城区高一上学期期末考试化学试卷(已下线)2012-2013湖北省孝感高中高一上学期期末考试化学试卷(已下线)2014-2015江苏省宿迁市五校高一上学期期中联考化学试卷2014-2015辽宁省大连市第二十高中高一上学期期末化学试卷2014-2015江苏省涟水中学高一12月月考化学试卷2014-2015陕西省西安市一中高一上学期期末化学试卷2014-2015四川省乐山市高一年级上学期期末考试化学试卷2015-2016学年北大附中河南分校高一上9月考化学试卷2015-2016学年河北省永年二中高一上学期12月月考化学试卷2015-2016学年四川阆中中学校高一上第二次段考化学试卷2015-2016学年陕西省西安一中高一上12月月考化学试卷2015-2016学年湖北省宜昌市部分示范高中高一上期末联考化学试卷2016-2017学年浙江省余姚中学高一上期中化学试卷2016-2017学年山东省枣庄八中高一12月月考化学卷重庆市第一中学2016-2017学年高一上学期期末考试化学试题2016-2017学年江西省南昌市第十中学高一上学期期末考试化学试卷云南省峨山彝族自治县第一中学2016-2017学年高二下学期期末考试化学试题山西省忻州市第一中学2016-2017学年高一必修一:3.2.3几种重要的金属化合物同步练习化学试题黑龙江省牡丹江市第一高级中学2017-2018学年高二10月月考(文)化学试题江苏省东台市创新学校2018届高三10月月考化学试题甘肃省甘谷县第一中学2017-2018学年高一上学期第二次月考化学试题上海杨浦高级中学2017-2018学年高二上学期12月月考化学试题湖北省宜昌市长阳县第一高级中学2017-2018学年高一12月月考化学试题山西省太原市成成中学校2017-2018学年高一12月月考化学试题宁夏育才中学2017-2018学年高一上学期期末考试化学试题新疆昌吉市2017-2018学年高一上学期期末考试化学试题天津市和平区2017-2018学年高一上学期期末考试化学试题江西省临川实验学校2017-2018学年高一上学期期末质量检测化学试题云南省玉溪第一中学2017-2018学年高一上学期期末考试化学试题河南省开封市兰考县第三高级中学2017-2018学年高一上学期期末考试化学试卷陕西省黄陵中学2017-2018学年高一(普通班)下学期开学考试化学试题【全国百强校】山东省泰安市第一中学2018-2019学年高一上学期期中考试化学试题【全国百强校】甘肃省兰州市第一中学2018-2019学年高一上学期12月月考化学试题山西省忻州市实验中学2018-2019学年高一上学期第三次教学质量检测化学试题河南省封丘县一中2018-2019学年高一上学期12月月考化学试题山东省泰安市宁阳一中2018-2019学年高一上学期阶段性考试二(12月)化学试题山西省晋中市平遥县第二中学2018-2019学年高一上学期12月月考化学试题河南省永城市实验高级中学2019届高三上学期期中考试化学试题甘肃省白银市会宁县第一中学2018届高三上学期期中考试化学试题吉林省白城市通榆县第一中学2020届高三上学期第二次月考化学试题山西省晋中市平遥县第二中学2019-2020学年高一12月月考化学试题四川省三台中学2019-2020学年高一上学期第三次月考化学试题云南省兰坪县第一中学2019-2020学年高一上学期期末考试化学试题陕西省西安中学2019-2020学年高一上学期期末考试化学试题广东省梅州市蕉岭县蕉岭中学2019—2020学年高一上学期期末考试化学试题四川省眉山市2019-2020学年高一上学期期末教学质量检测化学试题湖北省荆州市2019-2020学年高一上学期期末考试化学试题上海市闵行区向明世博中学2018-2019学年高二上学期期中考试化学试题河南省焦作市沁阳市第一中学2019-2020学年高一上学期12月月考化学试题陕西省咸阳市实验中学2019-2020学年高一上学期第三次月考化学试题山东省枣庄市2019-2020学年高一下学期期末考试化学试题(已下线)3.1.1 铁及其化合物练习(1)——《高中新教材同步备课》(鲁科版 必修第一册)人教版(2019)高一必修第一册 第三章 第一节 铁及其化合物鲁科版(2019)高一必修第一册第3章 物质的性质与转化 第1节 铁的多样性重庆市铜梁中学校等七校2019-2020学年高一上学期期末联考化学试题高一必修第一册(鲁科2019)第3章 第1节 铁的多样性 教材帮(已下线)3.1.1 铁的单质-2020-2021学年高一化学同步课堂帮帮帮(人教版2019必修第一册)宁夏石嘴山市平罗中学2020-2021学年高一上学期第三次月考化学试题甘肃省兰州市第一中学2020-2021学年高一上学期期末考试化学(文)试题湖南省常德市石门县第六中学2019-2020学年高一下学期第三次月考化学试题云南省梁河县第一中学2020-2021学年高一上学期第二次月考化学试题宁夏固原市隆德县2020-2021学年高一上学期期末考试化学试题广西南宁市邕宁高中2020-2021学年高一上学期期末考试化学试题江西省抚州市金溪县第一中学2020-2021学年高一上学期第二次月考化学试题云南省楚雄中学2020-2021学年高一下学期4月月考化学试题甘肃省武威市民勤县第四中学2020-2021学年高一下学期第一次月考化学(实验班)试题(已下线)专题08 铁及其化合物 (热点讲义)-2022年高三毕业班化学常考点归纳与变式演练
2021高三·浙江·专题练习
名校
7 . 为确定Fe2O3和Cu混合物的组成(假设混合均匀),某兴趣小组称取五份不同质量的样品,分别投入30.0 mL某浓度的稀硫酸中。充分反应后,每组样品剩余固体的质量与原样品质量的关系如图所示。下列说法不正确 的是
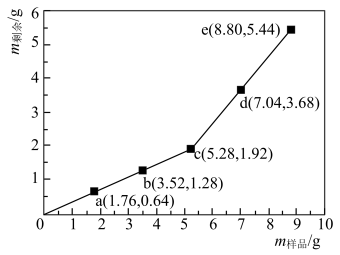

| A.各组样品均发生反应:Fe2O3+6H+=2Fe3++3H2O、2Fe3++Cu=2Fe2++Cu2+ |
| B.1.76 g样品充分反应后,溶液中一定存在Fe2+和Cu2+,一定不存在Fe3+ |
| C.该混合物中n(Fe2O3)︰n(Cu)=1︰3 |
| D.稀硫酸的浓度为3.00 mol·L-1 |
您最近一年使用:0次
2021-03-13更新
|
778次组卷
|
5卷引用:第三章 铁 金属材料
第三章 铁 金属材料(已下线)解密06 金属及其化合物(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)(已下线)解密06 金属及其化合物(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练陕西省咸阳市实验中学2021-2022学年高一上学期第三次月考化学试题(已下线)第3讲 铁盐及其亚铁盐
8 . 配合物在许多方面有着广泛的用途,目前我国科学家利用配合物在能源转化与储存方面有着杰出的贡献,请根据题意回答下列问题:
I.向黄色的FeCl3溶液中加入无色的KSCN溶液,溶液变成血红色。该反应在有的教材中用方程式FeCl3+3KSCN=Fe(SCN)3+3KCl表示。
(1)经研究表明,Fe(SCN)3是配合物,Fe3+与SCN-不仅能以1:3的个数比配合,还可以其他个数比配合。请按要求填空:
①若所得Fe3+和SCN-的配合物中,主要是Fe3+与SCN-以个数比1:1配合所得离子显血红色。该离子的离子符号是______ 。
②若Fe3+与SCN-以个数比1:5配合,则FeCl3与KSCN在水溶液中发生反应的化学方程式可以表示为______ 。
(2)向上述血红色溶液中继续加入浓KSCN溶液,溶液血红色加深,这是由于______ (填字母代号)。
A.与Fe3+配合的SCN-数目增多 B.血红色离子的数目增多 C.血红色离子的浓度增加
(3)向上述血红色溶液中加入NaF溶液振荡,只观察到血红色溶液迅速褪成无色,表示该反应的离子方程式为:______ ;能使该反应发生的可能原因是______ 。
II.已知: 在溶液中为橙色,
在溶液中为橙色, 在溶液中为黄色
在溶液中为黄色
(1)下列反应曾用于检测司机是否酒后驾驶:2 +3CH3CH2OH+16H++13H2O→4[Cr(H2O)6]3++3CH3COOH
+3CH3CH2OH+16H++13H2O→4[Cr(H2O)6]3++3CH3COOH
①基态Cr原子外围电子排布图为______ ;配合物[Cr(H2O)6]3+中与Cr3+形成配位键的原子是______ (填元素符号)。
②CH3CH2OH与H2O可以任意比例互溶,除因为它们都是极性分子外,还因为______ 。
(2)有下列实验:
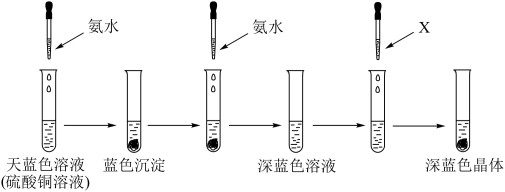
①呈天蓝色的离子的化学式为______ ,溶剂X可以是______ (填名称),继续添加氨水,沉淀溶解的离子方程式为______ 。
②该实验能说明NH3、H2O与Cu2+结合的能力由强到弱的顺序是______ 。
③下列有关化学实验的“操作→现象→解释”均正确的是______ 。
I.向黄色的FeCl3溶液中加入无色的KSCN溶液,溶液变成血红色。该反应在有的教材中用方程式FeCl3+3KSCN=Fe(SCN)3+3KCl表示。
(1)经研究表明,Fe(SCN)3是配合物,Fe3+与SCN-不仅能以1:3的个数比配合,还可以其他个数比配合。请按要求填空:
①若所得Fe3+和SCN-的配合物中,主要是Fe3+与SCN-以个数比1:1配合所得离子显血红色。该离子的离子符号是
②若Fe3+与SCN-以个数比1:5配合,则FeCl3与KSCN在水溶液中发生反应的化学方程式可以表示为
(2)向上述血红色溶液中继续加入浓KSCN溶液,溶液血红色加深,这是由于
A.与Fe3+配合的SCN-数目增多 B.血红色离子的数目增多 C.血红色离子的浓度增加
(3)向上述血红色溶液中加入NaF溶液振荡,只观察到血红色溶液迅速褪成无色,表示该反应的离子方程式为:
II.已知:
 在溶液中为橙色,
在溶液中为橙色, 在溶液中为黄色
在溶液中为黄色(1)下列反应曾用于检测司机是否酒后驾驶:2
 +3CH3CH2OH+16H++13H2O→4[Cr(H2O)6]3++3CH3COOH
+3CH3CH2OH+16H++13H2O→4[Cr(H2O)6]3++3CH3COOH①基态Cr原子外围电子排布图为
②CH3CH2OH与H2O可以任意比例互溶,除因为它们都是极性分子外,还因为
(2)有下列实验:

①呈天蓝色的离子的化学式为
②该实验能说明NH3、H2O与Cu2+结合的能力由强到弱的顺序是
③下列有关化学实验的“操作→现象→解释”均正确的是
| 选项 | 操作 | 现象 | 解释 |
| A | 向某溶液中滴加KSCN溶液 | 产生红色沉淀 | Fe3++3SCN-=Fe(SCN)3↓ |
| B | 向由0.1molCrCl3·6H2O配成的溶液加入足量AgNO3溶液 | 产生0.2mol沉淀 | 已知Cr3+的配位数为6,则 CrCl3·6H2O的化学式可表示为[Cr(H2O)5Cl]Cl2·H2O |
| C | 向溶液K2Cr2O7溶液中先滴加3滴浓硫酸,再改加10滴浓NaOH | 溶液先橙色加深,后变为黄 色 | 溶液中存在 +H2O⇌2 +H2O⇌2 +2H+ +2H+ |
| D | 向AgCl悬浊液中滴加氨水 | 沉淀溶解 | AgCl不溶于水,但溶于氨水,重新电离成Ag+和Cl- |
您最近一年使用:0次
解题方法
9 . 取少量红棕色的氧化铁粉末溶于适量盐酸中,得到棕黄色的氯化铁溶液。用此溶液进行以下实验:
(1)取少量溶液置于试管中,滴入氢氧化钠溶液,可观察到有红褐色沉淀生成,反应的化学方程式为_______ ,此反应属于_______ 反应。
(2)在小烧杯中加入20 mL蒸馏水,加热至沸腾后,向沸水中滴入几滴氯化铁溶液,继续煮沸至溶液呈______ 色,停止加热,制得的分散系为______ ,区分此分散系和其它溶液的方法为_______ (填操作名称)
(3)向第(2)题烧杯中的分散系逐滴滴入过量盐酸,出现一系列变化:
①先出现红褐色沉淀,原因是______________ 。
②随后沉淀逐渐溶解,溶液呈棕黄色,反应的化学方程式为_______ 。
(1)取少量溶液置于试管中,滴入氢氧化钠溶液,可观察到有红褐色沉淀生成,反应的化学方程式为
(2)在小烧杯中加入20 mL蒸馏水,加热至沸腾后,向沸水中滴入几滴氯化铁溶液,继续煮沸至溶液呈
(3)向第(2)题烧杯中的分散系逐滴滴入过量盐酸,出现一系列变化:
①先出现红褐色沉淀,原因是
②随后沉淀逐渐溶解,溶液呈棕黄色,反应的化学方程式为
您最近一年使用:0次
解题方法
10 . 某实验小组进行Cu和 溶液的实验。实验探究过程如图:
溶液的实验。实验探究过程如图:
实验装置

实验操作与现象:ⅰ.加入Cu粉后充分振荡,静置,溶液变成浅蓝绿色;
ⅱ.取少量ⅰ中清液于试管中,滴加3滴0.1mol/L KSCN溶液,立即出现白色沉淀,溶液局部变为红色,振荡后红色迅速褪去。
查阅资料:
Ⅰ. 可与
可与 反应生成CuSCN(白色沉淀)和
反应生成CuSCN(白色沉淀)和 ,
, 的性质与
的性质与 相似。
相似。
Ⅱ.CuSCN能与稀硝酸反应: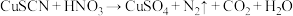 (未配平)。
(未配平)。
回答下列问题:
(1)Cu和 溶液反应的离子方程式为
溶液反应的离子方程式为___________ 。
(2)根据以上给出的实验现象推断白色沉淀为___________ 。为验证该白色沉淀,取少量白色沉淀于试管中,加入___________ ,若___________ 即可证明(补充所加试剂及实验现象)。
(3)用离子方程式解释ⅱ中溶液局部变为红色的原因是___________ 。
(4)根据ⅱ中实验现象可推知 更易与
更易与___________ 结合(填“ ”或“
”或“ ”)
”)
 溶液的实验。实验探究过程如图:
溶液的实验。实验探究过程如图:实验装置

实验操作与现象:ⅰ.加入Cu粉后充分振荡,静置,溶液变成浅蓝绿色;
ⅱ.取少量ⅰ中清液于试管中,滴加3滴0.1mol/L KSCN溶液,立即出现白色沉淀,溶液局部变为红色,振荡后红色迅速褪去。
查阅资料:
Ⅰ.
 可与
可与 反应生成CuSCN(白色沉淀)和
反应生成CuSCN(白色沉淀)和 ,
, 的性质与
的性质与 相似。
相似。Ⅱ.CuSCN能与稀硝酸反应:
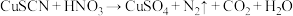 (未配平)。
(未配平)。回答下列问题:
(1)Cu和
 溶液反应的离子方程式为
溶液反应的离子方程式为(2)根据以上给出的实验现象推断白色沉淀为
(3)用离子方程式解释ⅱ中溶液局部变为红色的原因是
(4)根据ⅱ中实验现象可推知
 更易与
更易与 ”或“
”或“ ”)
”)
您最近一年使用:0次



