1 . 健康人体内含铁元素大约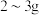 ,人体内铁元素以亚铁离子和三价铁离子的形式存在,
,人体内铁元素以亚铁离子和三价铁离子的形式存在, 易被吸收,所以给贫血者补充铁元素时,应补充含
易被吸收,所以给贫血者补充铁元素时,应补充含 的亚铁盐。“速力菲”(主要成分:琥珀酸亚铁,呈暗黄色)是市场上一种常见的补铁药物。该药品不溶于水但能溶于人体中的胃酸。某同学为了检测“速力菲”药片中
的亚铁盐。“速力菲”(主要成分:琥珀酸亚铁,呈暗黄色)是市场上一种常见的补铁药物。该药品不溶于水但能溶于人体中的胃酸。某同学为了检测“速力菲”药片中 的存在,设计并进行了如图实验:
的存在,设计并进行了如图实验:_____ ;试剂2的化学式为_____ 。
(2)加入新制氯水,溶液中发生反应的离子方程式是_____ 。
(3)加入试剂2时溶液为淡红色说明“速力非”中的 已被部分氧化,一般在服用“速力菲”时,同时服用维生素C,说明维生素C具有
已被部分氧化,一般在服用“速力菲”时,同时服用维生素C,说明维生素C具有_____ 性。
(4)不仅溶液中 易被氧化成
易被氧化成 ,溶液中白色沉淀
,溶液中白色沉淀 更易被
更易被 氧化,请写出反应的化学方程式:
氧化,请写出反应的化学方程式:______ 。
(5) 溶液存放时应在试剂瓶中加入
溶液存放时应在试剂瓶中加入______ ,防止 被氧化。
被氧化。
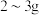 ,人体内铁元素以亚铁离子和三价铁离子的形式存在,
,人体内铁元素以亚铁离子和三价铁离子的形式存在, 易被吸收,所以给贫血者补充铁元素时,应补充含
易被吸收,所以给贫血者补充铁元素时,应补充含 的亚铁盐。“速力菲”(主要成分:琥珀酸亚铁,呈暗黄色)是市场上一种常见的补铁药物。该药品不溶于水但能溶于人体中的胃酸。某同学为了检测“速力菲”药片中
的亚铁盐。“速力菲”(主要成分:琥珀酸亚铁,呈暗黄色)是市场上一种常见的补铁药物。该药品不溶于水但能溶于人体中的胃酸。某同学为了检测“速力菲”药片中 的存在,设计并进行了如图实验:
的存在,设计并进行了如图实验:
(2)加入新制氯水,溶液中发生反应的离子方程式是
(3)加入试剂2时溶液为淡红色说明“速力非”中的
 已被部分氧化,一般在服用“速力菲”时,同时服用维生素C,说明维生素C具有
已被部分氧化,一般在服用“速力菲”时,同时服用维生素C,说明维生素C具有(4)不仅溶液中
 易被氧化成
易被氧化成 ,溶液中白色沉淀
,溶液中白色沉淀 更易被
更易被 氧化,请写出反应的化学方程式:
氧化,请写出反应的化学方程式:(5)
 溶液存放时应在试剂瓶中加入
溶液存放时应在试剂瓶中加入 被氧化。
被氧化。
您最近半年使用:0次
2 . 除去下列物质中所含的少量杂质(括号内为杂质),所选除杂试剂正确的是
A. :饱和碳酸氢钠溶液洗气 :饱和碳酸氢钠溶液洗气 | B. 溶液( 溶液( ):加入过量盐酸 ):加入过量盐酸 |
C.CO2(HCl): 溶液 溶液 | D. 溶液( 溶液( ):加入足量铁粉,过滤 ):加入足量铁粉,过滤 |
您最近半年使用:0次
解题方法
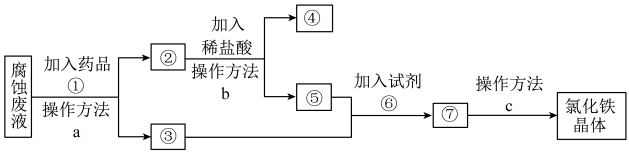
3 . 一种从腐蚀废液回收金属铜并获得氯化铁晶体的工艺流程如下。请根据流程,回答下列问题。(提示:为充分除去杂质,所加试剂均为过量)__________________ 。
(2)④所代表的物质是______ (用化学式表示)。
(3)操作方法a、b、c中是过滤的是______ (填序号)。
(4)若取2 mL溶液⑤加入试管中,然后滴加氢氧化钠溶液,产生白色沉淀,______ (补全实验现象),此过程涉及氧化还原反应的化学方程式是_________________ 。
(5)试剂⑥是 时,发生反应的化学方程式是
时,发生反应的化学方程式是__________________ 。
(2)④所代表的物质是
(3)操作方法a、b、c中是过滤的是
(4)若取2 mL溶液⑤加入试管中,然后滴加氢氧化钠溶液,产生白色沉淀,
(5)试剂⑥是
 时,发生反应的化学方程式是
时,发生反应的化学方程式是
您最近半年使用:0次
解题方法
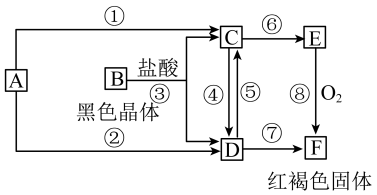
4 . 已知A为常见的金属单质,根据下图所示的关系:___________ ,B为___________ ,C为___________ ,D为___________ ,E为___________ ,F为___________ 。
(2)写出④⑤的离子方程式,⑧的化学方程式。
④___________ ,
⑤___________ ,
⑧___________ 。
(2)写出④⑤的离子方程式,⑧的化学方程式。
④
⑤
⑧
您最近半年使用:0次
解题方法
5 . 下列除杂方法或对应方程式错误的是
| 选项 | 物质(杂质) | 除杂方法或试剂 | 方程式 |
| A | 溶液 ( ( ) ) | 过量Fe,过滤 |  |
| B | 固体 ( ( ) ) | 水溶后通过量 ,结晶,过滤 ,结晶,过滤 | 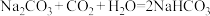 |
| C | 固体 ( ( ) ) | 水溶后加入过量NaOH |  |
| D |  ( ( ) ) | 过量Fe,过滤 |  |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
6 . 印刷电路板的制作原理是用FeCl3溶液腐蚀覆铜板上不需要的铜箔。下列说法错误的是
| A.Fe3+能溶解Cu,说明氧化性:Fe3+>Cu2+ |
| B.“腐蚀液”的颜色最终由黄色变为无色 |
| C.当有1mol电子转移时,溶液中Cu2+增加0.5mol |
D.该原理的离子方程式为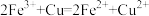 |
您最近半年使用:0次
7 . 铁是人类较早使用的金属之一,回答下列问题。
(1)下列所含铁元素只有还原性的物质是___________ (填字母)。
A.Fe B.FeCl3 C.FeSO4
(2)血红蛋白(Hb)中的铁元素呈正二价,能与O2分子结合成氧合血红蛋白(HbO)从而有输送氧的能力。NaNO2因具有氧化性,能使血红蛋白丧失与O2结合的能力,药品美蓝是其有效的解毒剂,下列说法中正确的是___________ (填字母)。
A.药品美蓝发生还原反应 B.药品美蓝是还原剂 C.药品美蓝被还原
(3)制备氢氧化亚铁时,现象由白色絮状沉淀最终转化为红褐色沉淀,请用化学方程式解释现象:___________ 。
(4)请设计实验检验在空气中放置的硫酸亚铁溶液已部分变质:___________ 。
(5)高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂。工业上湿法制备高铁酸钾的反应体系中有六种微粒:Fe(OH)3、ClO-、OH-、 、Cl-、H2O。写出并配平该反应的离子方程式
、Cl-、H2O。写出并配平该反应的离子方程式___________ ;若反应过程中转移了0.3 mol电子,则还原产物的物质的量为___________ mol。
(1)下列所含铁元素只有还原性的物质是
A.Fe B.FeCl3 C.FeSO4
(2)血红蛋白(Hb)中的铁元素呈正二价,能与O2分子结合成氧合血红蛋白(HbO)从而有输送氧的能力。NaNO2因具有氧化性,能使血红蛋白丧失与O2结合的能力,药品美蓝是其有效的解毒剂,下列说法中正确的是
A.药品美蓝发生还原反应 B.药品美蓝是还原剂 C.药品美蓝被还原
(3)制备氢氧化亚铁时,现象由白色絮状沉淀最终转化为红褐色沉淀,请用化学方程式解释现象:
(4)请设计实验检验在空气中放置的硫酸亚铁溶液已部分变质:
(5)高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂。工业上湿法制备高铁酸钾的反应体系中有六种微粒:Fe(OH)3、ClO-、OH-、
 、Cl-、H2O。写出并配平该反应的离子方程式
、Cl-、H2O。写出并配平该反应的离子方程式
您最近半年使用:0次
解题方法
8 . 下列离子能大量共存的是
A.无色酚酞试液呈红色的溶液中: 、 、 、 、 、 、 |
B.无色透明的溶液中: 、 、 、 、 、 、 |
C.含有大量 的溶液中: 的溶液中: 、 、 、 、 、 、 |
D.含有大量 的溶液中: 的溶液中: 、 、 、 、 、 、 |
您最近半年使用:0次
9 . 铁在地壳中含量丰富,也是重要的人体微量元素之一。下列有关说法正确的是
| A.铁与水蒸气反应生成氢氧化铁和氢气 |
| B.为了防止缺铁性贫血,麦片中可以添加微量的还原铁粉 |
| C.将饱和FeCl3溶液滴入沸水中,小心加热后制得红褐色Fe(OH)3胶体 |
| D.取新鲜菠菜切开表皮,在内部组织上滴加KSCN溶液,无颜色变化说明菠菜不含铁 |
您最近半年使用:0次
名校
解题方法
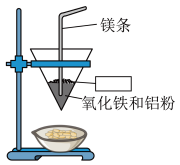
10 . 将铝与氧化铁混合制备单质铁的反应称为铝热反应,反应装置如图所示:_____ 。
(2)该铝热反应的化学方程式为_____ ,引发铝热反应的实验操作是_____ 。
(3)取少量反应所得的固体混合物,将其溶于足量稀 ,滴加KSCN溶液无明显现象,能否说明固体混合物中已无
,滴加KSCN溶液无明显现象,能否说明固体混合物中已无 ,请判断并说明理由
,请判断并说明理由_____ 。
(4)写出一种铝热反应的实际应用_____ 。
(2)该铝热反应的化学方程式为
(3)取少量反应所得的固体混合物,将其溶于足量稀
 ,滴加KSCN溶液无明显现象,能否说明固体混合物中已无
,滴加KSCN溶液无明显现象,能否说明固体混合物中已无 ,请判断并说明理由
,请判断并说明理由(4)写出一种铝热反应的实际应用
您最近半年使用:0次



