名校
1 . 综合利用废弃物,对资源利用和环境保护具有现实意义。以废铁屑(含少量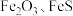 等杂质)为原料,制备硫酸亚铁晶体(
等杂质)为原料,制备硫酸亚铁晶体( ),流程示意图如下。
),流程示意图如下。
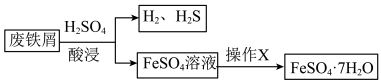
(1)酸浸过程中, 的作用是
的作用是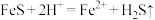 、
、 、
、___________ (用离子方程式表示)。
(2)酸浸时间对所得溶液的成分影响如下表所示。
①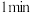 时检验,溶液变红,写出离子方程式
时检验,溶液变红,写出离子方程式___________
② 时检验,用离子方程式表示溶液未变红的原因
时检验,用离子方程式表示溶液未变红的原因___________ 。
③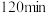 时检验,溶液复又变红,用文字说明原因
时检验,溶液复又变红,用文字说明原因___________ 。
(3)已知: 受热易失水。操作X为:
受热易失水。操作X为: ___________ 。
(4)测定所得硫酸亚铁晶体中 的含量,步骤如下:
的含量,步骤如下:
Ⅰ.称取 硫酸亚铁晶体样品,配制成
硫酸亚铁晶体样品,配制成 溶液。
溶液。
Ⅱ.取出 溶液,加入适量稀硫酸,滴入
溶液,加入适量稀硫酸,滴入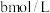 的
的 溶液,至反应完全共消耗
溶液,至反应完全共消耗 溶液
溶液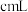 。
。
①依题意完善Ⅱ中 氧化
氧化 的离子方程式
的离子方程式________

 ___________
___________
 ___________
___________
②计算硫酸亚铁晶体样品中 的质量分数
的质量分数___________ 。
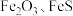 等杂质)为原料,制备硫酸亚铁晶体(
等杂质)为原料,制备硫酸亚铁晶体( ),流程示意图如下。
),流程示意图如下。
(1)酸浸过程中,
 的作用是
的作用是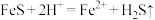 、
、 、
、(2)酸浸时间对所得溶液的成分影响如下表所示。
| 酸浸时间 | 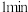 |  |  |
用 溶液检验 溶液检验 | 变红 | 未变红 | 变红 |
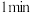 时检验,溶液变红,写出离子方程式
时检验,溶液变红,写出离子方程式②
 时检验,用离子方程式表示溶液未变红的原因
时检验,用离子方程式表示溶液未变红的原因③
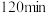 时检验,溶液复又变红,用文字说明原因
时检验,溶液复又变红,用文字说明原因(3)已知:
 受热易失水。操作X为:
受热易失水。操作X为: (4)测定所得硫酸亚铁晶体中
 的含量,步骤如下:
的含量,步骤如下:Ⅰ.称取
 硫酸亚铁晶体样品,配制成
硫酸亚铁晶体样品,配制成 溶液。
溶液。Ⅱ.取出
 溶液,加入适量稀硫酸,滴入
溶液,加入适量稀硫酸,滴入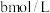 的
的 溶液,至反应完全共消耗
溶液,至反应完全共消耗 溶液
溶液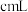 。
。①依题意完善Ⅱ中
 氧化
氧化 的离子方程式
的离子方程式
 ___________
___________
 ___________
___________②计算硫酸亚铁晶体样品中
 的质量分数
的质量分数
您最近一年使用:0次
2024-03-27更新
|
218次组卷
|
4卷引用:江西省丰城中学2023-2024学年高一下学期开学化学试题
名校
2 . 铁是人体不可缺少的微量元素,硫酸亚铁晶体(FeSO4·7H2O)在医药上作补血剂。某课外小组测定该补血剂中铁元素的含量,并检验该补血剂是否变质。实验步骤如下:
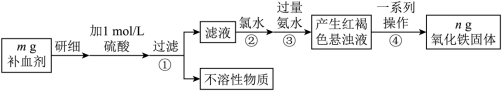
(1)实验中配制480 mL 1 mol/L的硫酸溶液,量取18.4 mol/L的浓硫酸_____ mL。
(2)步骤②加入过量氯水后发生反应的离子方程式为_______ 。
(3)步骤④中一系列操作步骤为______ 、洗涤、灼烧、冷却、称量。
(4)若实验无损耗,则该补血剂含铁元素的质量分数为_______ 。
(5)某同学发现部分补血剂药片表面发黄,取样品研细,溶于1 mol/L的硫酸溶液,过滤。取滤液加________ 溶液(填写化学式),溶液变红说明该补血剂已部分变质。
(6)下列检验(5)中滤液中是否有Fe2+应选用的试剂是___________。

(1)实验中配制480 mL 1 mol/L的硫酸溶液,量取18.4 mol/L的浓硫酸
(2)步骤②加入过量氯水后发生反应的离子方程式为
(3)步骤④中一系列操作步骤为
(4)若实验无损耗,则该补血剂含铁元素的质量分数为
(5)某同学发现部分补血剂药片表面发黄,取样品研细,溶于1 mol/L的硫酸溶液,过滤。取滤液加
(6)下列检验(5)中滤液中是否有Fe2+应选用的试剂是___________。
| A.氯水 | B.酸性KMnO4溶液 | C.铁粉 | D.FeCl3溶液 |
您最近一年使用:0次
名校
3 . 微量元素体检报告单显示,某儿童体内铁元素含量偏低。
(1)服用维生素C可使食物中的 转化为
转化为 。在这个过程中体现维生素C的
。在这个过程中体现维生素C的_______ (填“氧化性”或“还原性”)。缺铁性贫血患者应补充 ,一些补铁剂用硫酸亚铁制成药片时,外表包有一层特殊的糖衣,推测糖衣的作用是
,一些补铁剂用硫酸亚铁制成药片时,外表包有一层特殊的糖衣,推测糖衣的作用是_______ 。
(2)硫酸亚铁晶体 在医药上用作补血剂.某课外小组设计实验测定该补血剂中铁元素的含量,并检验该补血剂是否变质.实验步骤如下:
在医药上用作补血剂.某课外小组设计实验测定该补血剂中铁元素的含量,并检验该补血剂是否变质.实验步骤如下:
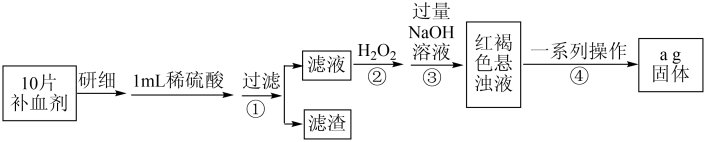
请回答下列问题:
i.取步骤①的滤液滴加 溶液后变为红色,说明滤液中含有
溶液后变为红色,说明滤液中含有_______ (填离子符号),加入 粉后红色褪去,写出加入铁粉时反应的离子方程式:
粉后红色褪去,写出加入铁粉时反应的离子方程式:_______ 。
ii.另取步骤①的滤液,检验其中是否存在 的试剂为
的试剂为_______ 。
iii.步骤②加入过量 的目的是
的目的是_______ 。
iv.一系列操作包括过滤、洗涤、灼烧,最后所得固体为_______ (写化学式)。
v.假设实验中的损耗忽略不计,若1片补血剂的质量为 ,则补血剂中铁元素的质量分数为
,则补血剂中铁元素的质量分数为_______ 。
(1)服用维生素C可使食物中的
 转化为
转化为 。在这个过程中体现维生素C的
。在这个过程中体现维生素C的 ,一些补铁剂用硫酸亚铁制成药片时,外表包有一层特殊的糖衣,推测糖衣的作用是
,一些补铁剂用硫酸亚铁制成药片时,外表包有一层特殊的糖衣,推测糖衣的作用是(2)硫酸亚铁晶体
 在医药上用作补血剂.某课外小组设计实验测定该补血剂中铁元素的含量,并检验该补血剂是否变质.实验步骤如下:
在医药上用作补血剂.某课外小组设计实验测定该补血剂中铁元素的含量,并检验该补血剂是否变质.实验步骤如下:
请回答下列问题:
i.取步骤①的滤液滴加
 溶液后变为红色,说明滤液中含有
溶液后变为红色,说明滤液中含有 粉后红色褪去,写出加入铁粉时反应的离子方程式:
粉后红色褪去,写出加入铁粉时反应的离子方程式:ii.另取步骤①的滤液,检验其中是否存在
 的试剂为
的试剂为iii.步骤②加入过量
 的目的是
的目的是iv.一系列操作包括过滤、洗涤、灼烧,最后所得固体为
v.假设实验中的损耗忽略不计,若1片补血剂的质量为
 ,则补血剂中铁元素的质量分数为
,则补血剂中铁元素的质量分数为
您最近一年使用:0次
2022-01-24更新
|
327次组卷
|
3卷引用:山东省济宁市2021-2022学年高一上学期期末考试化学试题
解题方法
4 . 测定冶金级高纯硅中铁元素的含量:将mg样品用氢氟酸和硝酸溶解处理,配成V mL溶液,用羟胺(NH2OH,难电离)将Fe3+还原为Fe2+后,加入邻二氮菲,形成橙红色物质。利用吸光度法测得吸光度为0.500(吸光度与Fe2+浓度的关系曲线如图所示)。
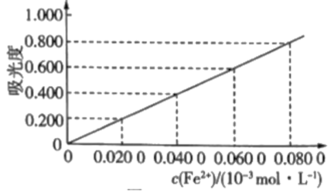
(1)酸性条件下,羟胺将Fe3+还原为Fe2+,同时产生一种无污染气体,该反应的离子方程式为___________ 。
(2)样品中铁元素的质量分数表达式为___________ (用字母表示)。

(1)酸性条件下,羟胺将Fe3+还原为Fe2+,同时产生一种无污染气体,该反应的离子方程式为
(2)样品中铁元素的质量分数表达式为
您最近一年使用:0次
名校
5 . 二氧化钛是一种常用的金属氧化物。工业上常用钛铁矿(主要成分为 ,其中Ti元素的化合价为
,其中Ti元素的化合价为 )来提取
)来提取 ,其中通常混有一定量的赤铁矿(主要成分为
,其中通常混有一定量的赤铁矿(主要成分为 ),该工艺流程如下:
),该工艺流程如下:

(1)结合流程,判断下列关于 的说法,错误的是_______。
的说法,错误的是_______。
(2)关于铁及其合金的性质,下列说法错误的是_______。
(3)将上述实验中得到的 溶于水,取2mL该溶液于试管中,向其中滴加几滴NaOH溶液。
溶于水,取2mL该溶液于试管中,向其中滴加几滴NaOH溶液。
①看到的现象是_______ ,写出相应的化学方程式_______ 、_______ 。
②再向上述试管中滴加足量的稀硝酸中,下列说法正确的是_______ 。
A.仅发生复分解反应
B.原试管中的沉淀可能同时含有 和
和
C.最后溶液中的盐仅有
(4)检验 中不含
中不含 的方法是
的方法是_______ ,现象是_______ 。
(5)根据②处的反应可知 的氧化性比
的氧化性比 的氧化性强,理由是
的氧化性强,理由是_______ 。
(6)经检测,某次使用的混合矿石中约含有质量分数50%的 ,40%的
,40%的 ,其它杂质中不含铁元素。若使用1吨该矿石冶炼
,其它杂质中不含铁元素。若使用1吨该矿石冶炼 ,能得到
,能得到
_______ 吨,同时得到副产物
_______ 吨(不考虑生产过程中的损失,均保留两位小数)。
 ,其中Ti元素的化合价为
,其中Ti元素的化合价为 )来提取
)来提取 ,其中通常混有一定量的赤铁矿(主要成分为
,其中通常混有一定量的赤铁矿(主要成分为 ),该工艺流程如下:
),该工艺流程如下:
(1)结合流程,判断下列关于
 的说法,错误的是_______。
的说法,错误的是_______。A. 发生复分解反应生成 发生复分解反应生成 |
B.煅烧 时,发生还原反应生成 时,发生还原反应生成 |
| C.流程中“结晶”的具体步骤是:加热浓缩、冷却结晶 |
D.保存 溶液时需要加铁粉 溶液时需要加铁粉 |
(2)关于铁及其合金的性质,下列说法错误的是_______。
| A.在元素周期表中,铁属于过渡元素 |
| B.生铁和钢的性质差异主要是碳含量的不同 |
| C.铁和不同非金属单质反应产物中的铁元素价态可能不同 |
| D.铁在氧气中燃烧后,可以使用磁铁验证是否有铁单质剩余 |
(3)将上述实验中得到的
 溶于水,取2mL该溶液于试管中,向其中滴加几滴NaOH溶液。
溶于水,取2mL该溶液于试管中,向其中滴加几滴NaOH溶液。①看到的现象是
②再向上述试管中滴加足量的稀硝酸中,下列说法正确的是
A.仅发生复分解反应
B.原试管中的沉淀可能同时含有
 和
和
C.最后溶液中的盐仅有

(4)检验
 中不含
中不含 的方法是
的方法是(5)根据②处的反应可知
 的氧化性比
的氧化性比 的氧化性强,理由是
的氧化性强,理由是(6)经检测,某次使用的混合矿石中约含有质量分数50%的
 ,40%的
,40%的 ,其它杂质中不含铁元素。若使用1吨该矿石冶炼
,其它杂质中不含铁元素。若使用1吨该矿石冶炼 ,能得到
,能得到

您最近一年使用:0次
解题方法
6 . 铁和氯是高中阶段重要的化学元素,请阅读下列信息,回答问题:
Ⅰ.绘制价类图(化合价-物质类别)是学习元素化合物性质的重要方法,如图是铁元素的价类二维图。
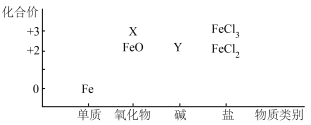
请回答下列问题:
(1)X、Y的化学式分别为___________ 、___________ 。
(2)FeO属于___________ (填“酸性”或“碱性”)氧化物,能与___________ (填试剂名称)反应生成FeCl2;从铁元素的价态分析,FeO与具有强氧化性的硝酸发生反应的氧化产物是___________ (填化学式)。
(3)FeCl3溶液能与铜片、NaOH溶液、KI溶液和KSCN溶液等发生反应,写出其中一个能体现Fe3+的氧化性的离子方程式___________ 。
Ⅱ.某品牌“84”消毒液包装上的说明如下图:
回答下列问题:
(4)该消毒液与洁厕灵同时使用会产生氯气,写出反应的离子方程式___________ 。
(5)理论上,一瓶上述“84”消毒液能从空气中吸收标准状况下___________ LCO2而变质(保留1位小数)。(已知:NaClO+CO2+H2O=NaHCO3+HClO)
Ⅰ.绘制价类图(化合价-物质类别)是学习元素化合物性质的重要方法,如图是铁元素的价类二维图。

请回答下列问题:
(1)X、Y的化学式分别为
(2)FeO属于
(3)FeCl3溶液能与铜片、NaOH溶液、KI溶液和KSCN溶液等发生反应,写出其中一个能体现Fe3+的氧化性的离子方程式
Ⅱ.某品牌“84”消毒液包装上的说明如下图:
| 84消毒液 有效成分:NaClO 规格:1000mL 质量分数:14.9% 物质的量浓度:2.2mol/L | 注意事项: 1.本品对棉织品有漂白脱色作用,有腐蚀性。 2.密封保存,请勿与洁厕灵同时使用。 3.保质期为一年。 |
(4)该消毒液与洁厕灵同时使用会产生氯气,写出反应的离子方程式
(5)理论上,一瓶上述“84”消毒液能从空气中吸收标准状况下
您最近一年使用:0次
名校
7 . 现有未知固体粉末,含有K+、Fe3+、Ba2+、 、Cl—中的几种。化学兴趣小组的同学进行了如下实验,回答下列问题:
、Cl—中的几种。化学兴趣小组的同学进行了如下实验,回答下列问题:
(1)取少量固体粉末溶于水中,固体完全溶解且溶液无色透明,证明该固体粉末中无___________ (填离子符号);
(2)有同学提出质疑,直接观察溶液颜色并不能作为判断的标准,可能含量太少观察不出来,取(1)中少量溶液于试管中加入___________ 溶液,发现溶液变为红色。
(3)另取(1)中少量溶液于试管中,滴加少量的稀硫酸,发现有白色沉淀产生,证明该固体粉末中有___________ (填离子符号),并写出离子方程式___________ 。
(4)另取(1)中少量溶液进行焰色试验,透过蓝色钴玻璃观察,火焰呈紫色,证明该固体粉末中有___________ (填离子符号);
(5)取(1)中少量溶液,加入硝酸银溶液,发现无明显现象,证明该固体粉末中无___________ (填离子符号),该固体粉末中一定有 ,原因是
,原因是___________ 。
 、Cl—中的几种。化学兴趣小组的同学进行了如下实验,回答下列问题:
、Cl—中的几种。化学兴趣小组的同学进行了如下实验,回答下列问题:(1)取少量固体粉末溶于水中,固体完全溶解且溶液无色透明,证明该固体粉末中无
(2)有同学提出质疑,直接观察溶液颜色并不能作为判断的标准,可能含量太少观察不出来,取(1)中少量溶液于试管中加入
(3)另取(1)中少量溶液于试管中,滴加少量的稀硫酸,发现有白色沉淀产生,证明该固体粉末中有
(4)另取(1)中少量溶液进行焰色试验,透过蓝色钴玻璃观察,火焰呈紫色,证明该固体粉末中有
(5)取(1)中少量溶液,加入硝酸银溶液,发现无明显现象,证明该固体粉末中无
 ,原因是
,原因是
您最近一年使用:0次
8 . 黑木耳富含蛋白质、铁、具有还原性的维生素C等,每100 g黑木耳含铁量高达185 mg。
I.为了确定黑木耳中含有铁元素,甲同学设计实验方案如下。____________ 。
(2)步骤④检验Fe3+所用试剂是_____________ (填化学式)溶液。
(3)已知:3Fe2++2[Fe(CN)6]3-=Fe3[Fe(CN)6]2↓,则滤液A中大量含有的阳离子 的离子符号为____________ 。
II.紫色的KMnO4溶液在酸性条件下具有强氧化性,其还原产物是无色的Mn2+。本实验用KMnO4酸性溶液来测定黑木耳中铁元素的含量,乙同学设计实验方案如下。_______ (填序号)。
a.Na b.Cu c.Fe
(5)步骤⑥的离子方程式为_______________ 。
(6)若乙同学实验操作规范,但测得含铁量远远偏高,其可能的原因是_______________ 。
I.为了确定黑木耳中含有铁元素,甲同学设计实验方案如下。
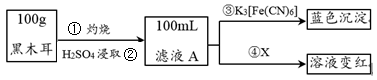
(2)步骤④检验Fe3+所用试剂是
(3)已知:3Fe2++2[Fe(CN)6]3-=Fe3[Fe(CN)6]2↓,则滤液A中大量含有的
II.紫色的KMnO4溶液在酸性条件下具有强氧化性,其还原产物是无色的Mn2+。本实验用KMnO4酸性溶液来测定黑木耳中铁元素的含量,乙同学设计实验方案如下。
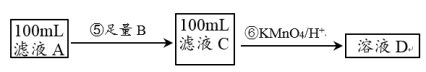
a.Na b.Cu c.Fe
(5)步骤⑥的离子方程式为
(6)若乙同学实验操作规范,但测得含铁量远远偏高,其可能的原因是
您最近一年使用:0次
9 . 铁在地壳中含量丰富,也是重要的人体微量元素之一。下列有关说法正确的是
| A.铁与水蒸气反应生成氢氧化铁和氢气 |
| B.为了防止缺铁性贫血,麦片中可以添加微量的还原铁粉 |
| C.将饱和FeCl3溶液滴入沸水中,小心加热后制得红褐色Fe(OH)3胶体 |
| D.取新鲜菠菜切开表皮,在内部组织上滴加KSCN溶液,无颜色变化说明菠菜不含铁 |
您最近一年使用:0次
名校
解题方法
10 . 硫酸亚铁晶体 在医药上做补血剂。某课外小组测定该补血剂中铁元素的含量,并检验该补血剂是否变质。实验步骤如下:
在医药上做补血剂。某课外小组测定该补血剂中铁元素的含量,并检验该补血剂是否变质。实验步骤如下:
(1)向操作①的滤液中滴加 溶液后变为红色,则该滤液中含有
溶液后变为红色,则该滤液中含有_______ (填离子符号)。
(2)操作②中反应的离子方程式:_______ 。
(3)操作③中反应的离子方程式:_______ 。
(4)操作④中系列操作的步骤:过滤、_______ 、_______ 、灼烧、冷却至室温、称量。
(5)假设实验中的损耗忽略不计,则每片补血剂含铁元素的质量为_______ g(用含a的代数式表示)。
 在医药上做补血剂。某课外小组测定该补血剂中铁元素的含量,并检验该补血剂是否变质。实验步骤如下:
在医药上做补血剂。某课外小组测定该补血剂中铁元素的含量,并检验该补血剂是否变质。实验步骤如下: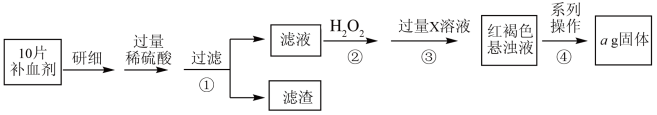
(1)向操作①的滤液中滴加
 溶液后变为红色,则该滤液中含有
溶液后变为红色,则该滤液中含有(2)操作②中反应的离子方程式:
(3)操作③中反应的离子方程式:
(4)操作④中系列操作的步骤:过滤、
(5)假设实验中的损耗忽略不计,则每片补血剂含铁元素的质量为
您最近一年使用:0次
2023-12-14更新
|
158次组卷
|
2卷引用:天津市新华中学2023-2024学年高一上学期第二次月考化学试卷



