1 . 铁在地壳中含量丰富,也是重要的人体微量元素之一。下列有关说法正确的是
| A.铁与水蒸气反应生成氢氧化铁和氢气 |
| B.为了防止缺铁性贫血,麦片中可以添加微量的还原铁粉 |
| C.将饱和FeCl3溶液滴入沸水中,小心加热后制得红褐色Fe(OH)3胶体 |
| D.取新鲜菠菜切开表皮,在内部组织上滴加KSCN溶液,无颜色变化说明菠菜不含铁 |
您最近一年使用:0次
名校
解题方法
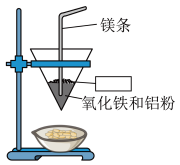
2 . 将铝与氧化铁混合制备单质铁的反应称为铝热反应,反应装置如图所示:_____ 。
(2)该铝热反应的化学方程式为_____ ,引发铝热反应的实验操作是_____ 。
(3)取少量反应所得的固体混合物,将其溶于足量稀 ,滴加KSCN溶液无明显现象,能否说明固体混合物中已无
,滴加KSCN溶液无明显现象,能否说明固体混合物中已无 ,请判断并说明理由
,请判断并说明理由_____ 。
(4)写出一种铝热反应的实际应用_____ 。
(2)该铝热反应的化学方程式为
(3)取少量反应所得的固体混合物,将其溶于足量稀
 ,滴加KSCN溶液无明显现象,能否说明固体混合物中已无
,滴加KSCN溶液无明显现象,能否说明固体混合物中已无 ,请判断并说明理由
,请判断并说明理由(4)写出一种铝热反应的实际应用
您最近一年使用:0次
名校
解题方法
3 .  溶液在工业上用于蚀刻铜箔电路板。从蚀刻后的废液中可回收铜并使蚀刻液再生,流程如图所示:
溶液在工业上用于蚀刻铜箔电路板。从蚀刻后的废液中可回收铜并使蚀刻液再生,流程如图所示: 溶液蚀刻铜箔的反应的离子方程式
溶液蚀刻铜箔的反应的离子方程式_____ 。
(2)从固体中分离出铜,试剂X是_____ 。
(3)若要使滤液再生为蚀刻液,可加入_____ 。
 溶液在工业上用于蚀刻铜箔电路板。从蚀刻后的废液中可回收铜并使蚀刻液再生,流程如图所示:
溶液在工业上用于蚀刻铜箔电路板。从蚀刻后的废液中可回收铜并使蚀刻液再生,流程如图所示: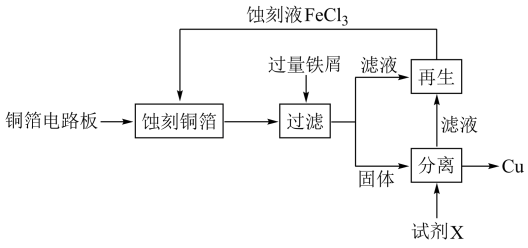
 溶液蚀刻铜箔的反应的离子方程式
溶液蚀刻铜箔的反应的离子方程式(2)从固体中分离出铜,试剂X是
(3)若要使滤液再生为蚀刻液,可加入
您最近一年使用:0次
解题方法
4 . 利用硫酸烧渣(主要含Fe2O3、FeO,还含有SiO2和CuO等)来制取FeSO4溶液。
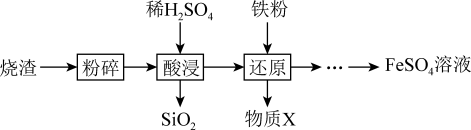
(1)“酸浸”时,Fe2O3发生反应的离子方程式是_______ 。
(2)“还原”时,铁粉将Fe3+、Cu2+还原为Fe2+和Cu。检验Fe3+是否已全部被还原,所选用试剂的化学式是______ 。
(3)实验室测定FeSO4溶液的浓度,常用K2Cr2O7标准溶液进行滴定。现称量2.940gK2Cr2O7(M=294g•mol-1)固体,配制成0.0100mol•L-1K2Cr2O7标准溶液。
①称量时,需用到的仪器有_______ 。
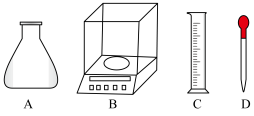
②根据计算,选用的容量瓶规格应为______ 。
A.100mL B.250mL C.500mL D.1000mL
(4)将(2)得到的FeSO4溶液进行下列操作,测定其物质的量浓度:
步骤一:取10.00mLFeSO4溶液,将其稀释成100.00mL溶液。
步骤二:取25.00mL稀释后的溶液,向其中加入0.100mol•L-1酸性KMnO4溶液。恰好反应时,记下消耗KMnO4溶液的体积。
步骤三:重复上述实验3次,平均消耗KMnO4溶液20.00mL。
已知:MnO +5Fe2++8H+=Mn2++5Fe3++4H2O
+5Fe2++8H+=Mn2++5Fe3++4H2O
①“步骤一”中稀释时所用的水需先进行加热煮沸,其目的是_______ 。
②试通过计算,求原FeSO4溶液的物质的量浓度是多少_______ ?(写出计算过程)

(1)“酸浸”时,Fe2O3发生反应的离子方程式是
(2)“还原”时,铁粉将Fe3+、Cu2+还原为Fe2+和Cu。检验Fe3+是否已全部被还原,所选用试剂的化学式是
(3)实验室测定FeSO4溶液的浓度,常用K2Cr2O7标准溶液进行滴定。现称量2.940gK2Cr2O7(M=294g•mol-1)固体,配制成0.0100mol•L-1K2Cr2O7标准溶液。
①称量时,需用到的仪器有

②根据计算,选用的容量瓶规格应为
A.100mL B.250mL C.500mL D.1000mL
(4)将(2)得到的FeSO4溶液进行下列操作,测定其物质的量浓度:
步骤一:取10.00mLFeSO4溶液,将其稀释成100.00mL溶液。
步骤二:取25.00mL稀释后的溶液,向其中加入0.100mol•L-1酸性KMnO4溶液。恰好反应时,记下消耗KMnO4溶液的体积。
步骤三:重复上述实验3次,平均消耗KMnO4溶液20.00mL。
已知:MnO
 +5Fe2++8H+=Mn2++5Fe3++4H2O
+5Fe2++8H+=Mn2++5Fe3++4H2O①“步骤一”中稀释时所用的水需先进行加热煮沸,其目的是
②试通过计算,求原FeSO4溶液的物质的量浓度是多少
您最近一年使用:0次
5 . 物质的性质决定着其在生产生活中的应用.下列对应关系错误的是
| 选项 | 性质 | 应用 |
| A | NaHCO3受热分解产生CO2 | 用作膨松剂 |
| B | NaClO具有强氧化性 | 84消毒液的有效成分 |
| C | Fe的金属性强于Cu | 用FeCl3溶液刻蚀Cu电路板 |
| D | 向盛有淀粉—KI溶液的试管中滴加几滴溴水,振荡,观察溶液颜色变化 | Br2的氧化性强于I2 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
6 . 现有金属单质A、B和气体甲、乙、丙及物质C、D、E、F、G,它们之间能发生如图反应(图中某些反应的产物及条件没有全部标出)
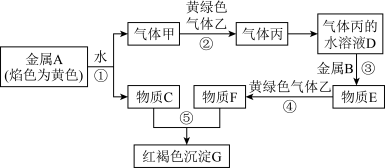
(1)物质G可以形成胶体和沉淀两种形式的分散系,实验室鉴别G的胶体和F的溶液,除了可通过观察颜色以外,还有的方法是_______ 。
(2)物质C中加入单质Al的离子反应方程式为_______________ ;
(3)向E的溶液加入NaOH溶液并且搅拌溶液,观察到的现象是______ ,请写出沉淀转化的化学方程式:________________ 。
(4)写出④离子反应方程式:________________ 。
(5)写出①发生的化学反应方程式的双线桥________ 。
(6)检验溶液F中阳离子实验方法是____________ 。
(7)向盛有H2O2溶液的试管中加入几滴酸化的物质E,溶液变成棕黄色,发生反应的离子方程式为__________________ 。

(1)物质G可以形成胶体和沉淀两种形式的分散系,实验室鉴别G的胶体和F的溶液,除了可通过观察颜色以外,还有的方法是
(2)物质C中加入单质Al的离子反应方程式为
(3)向E的溶液加入NaOH溶液并且搅拌溶液,观察到的现象是
(4)写出④离子反应方程式:
(5)写出①发生的化学反应方程式的双线桥
(6)检验溶液F中阳离子实验方法是
(7)向盛有H2O2溶液的试管中加入几滴酸化的物质E,溶液变成棕黄色,发生反应的离子方程式为
您最近一年使用:0次
解题方法
7 . 化合物X是一种蓝黑色(有时是粉红色)的固体,是一种由趋磁细菌制造的生物矿。某研究小组按如下流程探究该固体的组成:

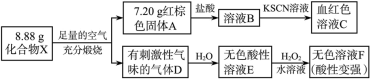
请回答:
(1)X的化学式为___________ 。
(2)请写出E反应生成F的化学方程式:___________ 。
(3)化合物X(只含两种元素)与盐酸反应,反应后得到浅绿色溶液,同时生成一种浅黄色不溶物和一种臭鸡蛋气味气体,请写出该反应的离子方程式:___________ 。


请回答:
(1)X的化学式为
(2)请写出E反应生成F的化学方程式:
(3)化合物X(只含两种元素)与盐酸反应,反应后得到浅绿色溶液,同时生成一种浅黄色不溶物和一种臭鸡蛋气味气体,请写出该反应的离子方程式:
您最近一年使用:0次
名校
解题方法
8 . 某班同学用如下实验探究Fe2+、Fe3+的性质:
(1)甲组同学取2mL0.1mol•L-1FeSO4溶液,加1滴KSCN溶液,无明显现象,再加几滴3%H2O2溶液(用H2SO4酸化至pH=1),溶液颜色变红。甲组同学通过上述实验分析Fe2+具有______ (填“氧化”或“还原”)性。写出上面划线处操作所发生反应的离子方程式______ 。
(2)针对Fe3++3SCN- Fe(SCN)3,下列说法正确的是
Fe(SCN)3,下列说法正确的是______ 。(不定项)
(3)乙组同学认为甲组的实验不够严谨,该组同学在2mLFeSO4溶液中先加入0.5mL煤油,再于液面下依次加入1滴KSCN溶液和13%H2O2溶液,溶液变红,煤油的作用是______ 。
(4)同时乙组同学查阅资料发现Fe2+与SCN-可发生反应,生成无色的电中性配合物。为证实该性质,乙组同学用FeCO3进行了如图所示的a和b两组实验:
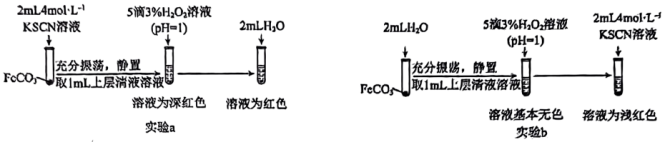
写出实验a中FeCO3与KSCN反应的离子方程式______ ,实验b的目的是______ 。
(5)反应S2O (aq)+2I-(aq)=2SO
(aq)+2I-(aq)=2SO (aq)+I2(aq)在加入Fe3+催化后,反应进程中的能量变化如图所示。已知:反应机理中有Fe2+出现。
(aq)+I2(aq)在加入Fe3+催化后,反应进程中的能量变化如图所示。已知:反应机理中有Fe2+出现。

①写出反应历程中“速率决定步骤”的热化学方程式:______ 。
②反应过程中由于Fe2+浓度较低而不容易被检测到,请回答Fe2+浓度较低的原因:______ 。
(6)溶液中Fe2+与邻二集非X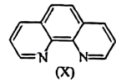 会生成橘黄色的配合物Y。
会生成橘黄色的配合物Y。
①邻二氮菲提供的配位原子是______ 。
②使用该方法时,需要控制pH在2~9之间,其原因为:______ 。
③取2.00mLc(Fe2+)=6.0×10-4mol/L的溶液,加入不同体积、浓度均为c(X)=6.0×10-4mol/L的邻二氮菲溶液,充分反应后加水定容至25mL,得到系列溶液,测其吸光度,结果如表:
已知吸光度A与有色物质的浓度 成正比。Fe2+和邻二氮菲X的吸光度近似为0。
成正比。Fe2+和邻二氮菲X的吸光度近似为0。
Fe2++nX=Y(橘黄色)
结合上面实验数据,通过计算回答Y中Fe2+的配位数(与中心原子或离子以配位键形式结合的配位原子数目):______ 。
(1)甲组同学取2mL0.1mol•L-1FeSO4溶液,加1滴KSCN溶液,无明显现象,再加几滴3%H2O2溶液(用H2SO4酸化至pH=1),溶液颜色变红。甲组同学通过上述实验分析Fe2+具有
(2)针对Fe3++3SCN-
 Fe(SCN)3,下列说法正确的是
Fe(SCN)3,下列说法正确的是| A.增大KSCN溶液的浓度,平衡常数增大 |
| B.向上述平衡体系中加入适量KCl圆体,平衡不移动 |
| C.加水稀释,平衡向左移动,且溶液的红色变浅 |
D.加入少量铁粉,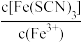 减小 减小 |
(4)同时乙组同学查阅资料发现Fe2+与SCN-可发生反应,生成无色的电中性配合物。为证实该性质,乙组同学用FeCO3进行了如图所示的a和b两组实验:

写出实验a中FeCO3与KSCN反应的离子方程式
(5)反应S2O
 (aq)+2I-(aq)=2SO
(aq)+2I-(aq)=2SO (aq)+I2(aq)在加入Fe3+催化后,反应进程中的能量变化如图所示。已知:反应机理中有Fe2+出现。
(aq)+I2(aq)在加入Fe3+催化后,反应进程中的能量变化如图所示。已知:反应机理中有Fe2+出现。
①写出反应历程中“速率决定步骤”的热化学方程式:
②反应过程中由于Fe2+浓度较低而不容易被检测到,请回答Fe2+浓度较低的原因:
(6)溶液中Fe2+与邻二集非X
 会生成橘黄色的配合物Y。
会生成橘黄色的配合物Y。①邻二氮菲提供的配位原子是
②使用该方法时,需要控制pH在2~9之间,其原因为:
③取2.00mLc(Fe2+)=6.0×10-4mol/L的溶液,加入不同体积、浓度均为c(X)=6.0×10-4mol/L的邻二氮菲溶液,充分反应后加水定容至25mL,得到系列溶液,测其吸光度,结果如表:
| V(X)/mL | 2.00 | 3.00 | 4.00 | 5.00 | 6.00 | 8.00 |
| 吸光度/A | 0.24 | 0.36 | 0.48 | 0.60 | 0.72 | 0.72 |
 成正比。Fe2+和邻二氮菲X的吸光度近似为0。
成正比。Fe2+和邻二氮菲X的吸光度近似为0。Fe2++nX=Y(橘黄色)
结合上面实验数据,通过计算回答Y中Fe2+的配位数(与中心原子或离子以配位键形式结合的配位原子数目):
您最近一年使用:0次
9 . 铁及其化合物在工农业生产中应用广泛,部分含铁物质的分类与相应化合价关系如图所示。下列说法错误的是


A. 、 、 均可由化合反应来制备 均可由化合反应来制备 | B. 在周期表中处在第四周期第ⅦB族 在周期表中处在第四周期第ⅦB族 |
C. 在纯氧中燃烧,可生成 在纯氧中燃烧,可生成 | D.能用 溶液鉴别 溶液鉴别 溶液和 溶液和 溶液 溶液 |
您最近一年使用:0次
解题方法
10 . 下列实验设计不能达到实验目的的是
| 实验目的 | 实验设计 | |
| A | 检验溶液中FeSO4是否被氧化 | 取少量待测液,滴加KSCN溶液,观察溶液颜色变化 |
| B | 除去CO2中的HCl | 通过饱和NaHCO3溶液洗气后干燥 |
| C | 测定HClO溶液的pH | 将待测液滴在湿润的pH试纸上,与标准比色卡对照 |
| D | 除去Na2CO3固体中的NaHCO3 | 将固体加热至恒重 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次



