解题方法
1 . 纳米磁性 在生物靶向材料、微波吸收材料及静电复印显影剂等方面都有极其广泛的用途。一种利用废旧镀锌铁皮制备纳米磁性
在生物靶向材料、微波吸收材料及静电复印显影剂等方面都有极其广泛的用途。一种利用废旧镀锌铁皮制备纳米磁性 的工艺流程如下:
的工艺流程如下: 溶于强碱时生成
溶于强碱时生成 。
。
(1)“碱洗”废旧镀锌铁皮的目的是___________(填字母)。
(2)“酸溶”后的溶液中阳离子主要有___________ 。
(3)“氧化”时发生的总反应离子方程式为___________ 。在酸性条件下, 很容易发生反应:
很容易发生反应: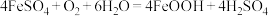 。为避免生成
。为避免生成 影响产品纯度,则“氧化”时应选择的加料方式为
影响产品纯度,则“氧化”时应选择的加料方式为___________ 。
(4)“氧化”后溶液中 的物质的量之比是1∶2,检验其中
的物质的量之比是1∶2,检验其中 可选用的试剂是___________。
可选用的试剂是___________。
(5)“分离”时 纳米粒子不能采用过滤法实现固液分离,理由是
纳米粒子不能采用过滤法实现固液分离,理由是___________ 。
(6)用重铬酸钾法(一种氧化还原滴定法)可测定产物 中的二价铁含量。若需配制浓度为
中的二价铁含量。若需配制浓度为 的
的 标准溶液
标准溶液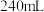 ,应准确称取
,应准确称取___________ g (保留4位有效数字,已知
(保留4位有效数字,已知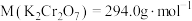 )。
)。
 在生物靶向材料、微波吸收材料及静电复印显影剂等方面都有极其广泛的用途。一种利用废旧镀锌铁皮制备纳米磁性
在生物靶向材料、微波吸收材料及静电复印显影剂等方面都有极其广泛的用途。一种利用废旧镀锌铁皮制备纳米磁性 的工艺流程如下:
的工艺流程如下:
 溶于强碱时生成
溶于强碱时生成 。
。(1)“碱洗”废旧镀锌铁皮的目的是___________(填字母)。
| A.去除油污 | B.溶解镀锌层 | C.去除铁锈 | D.钝化铁皮 |
(2)“酸溶”后的溶液中阳离子主要有
(3)“氧化”时发生的总反应离子方程式为
 很容易发生反应:
很容易发生反应: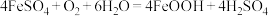 。为避免生成
。为避免生成 影响产品纯度,则“氧化”时应选择的加料方式为
影响产品纯度,则“氧化”时应选择的加料方式为(4)“氧化”后溶液中
 的物质的量之比是1∶2,检验其中
的物质的量之比是1∶2,检验其中 可选用的试剂是___________。
可选用的试剂是___________。A. 溶液 溶液 | B. 溶液 溶液 | C.酸性 溶液 溶液 | D. |
(5)“分离”时
 纳米粒子不能采用过滤法实现固液分离,理由是
纳米粒子不能采用过滤法实现固液分离,理由是(6)用重铬酸钾法(一种氧化还原滴定法)可测定产物
 中的二价铁含量。若需配制浓度为
中的二价铁含量。若需配制浓度为 的
的 标准溶液
标准溶液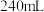 ,应准确称取
,应准确称取 (保留4位有效数字,已知
(保留4位有效数字,已知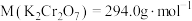 )。
)。
您最近一年使用:0次
名校
2 . 铁是人体必需的微量元素,铁摄入不足可能引起缺铁性贫血。小组同学利用化学实验进行菠菜中铁元素的检验和铁元素含量测定。
实验1.菠菜中铁元素的检验

(1)操作1的名称是_______ 。
(2)溶液②为浅红色,说明溶液①中含有_______ (填离子符号)。
(3)溶液③中_______ (填实验现象),证明溶液②中还含有 ,其推理过程是
,其推理过程是_______ 。
实验2.测定菠菜中铁元素的含量
i.沉淀法:向实验1滤液①中加入足量NaOH溶液,过滤、洗涤沉淀、加热烘干、称量。
(4)滤液①中加入足量NaOH溶液后生成的沉淀有_______ 、_______ ;在沉淀生成或后续处理过程中,沉淀转化发生的氧化还原 反应为_______ 。
ii.比色法:利用色度传感器测定其对光的透过率或者吸收率,颜色越深,吸收率越高。
测得不同浓度 的标准液吸收率如下图。
的标准液吸收率如下图。

(5) 菠菜处理后得到溶液(3)
菠菜处理后得到溶液(3) ,色度传感器测得吸收率为上图中a点,则
,色度传感器测得吸收率为上图中a点,则
_______  ,
, 菠菜中含铁
菠菜中含铁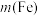 =
=_______ g。
实验1.菠菜中铁元素的检验

(1)操作1的名称是
(2)溶液②为浅红色,说明溶液①中含有
(3)溶液③中
 ,其推理过程是
,其推理过程是实验2.测定菠菜中铁元素的含量
i.沉淀法:向实验1滤液①中加入足量NaOH溶液,过滤、洗涤沉淀、加热烘干、称量。
(4)滤液①中加入足量NaOH溶液后生成的沉淀有
ii.比色法:利用色度传感器测定其对光的透过率或者吸收率,颜色越深,吸收率越高。
测得不同浓度
 的标准液吸收率如下图。
的标准液吸收率如下图。
(5)
 菠菜处理后得到溶液(3)
菠菜处理后得到溶液(3) ,色度传感器测得吸收率为上图中a点,则
,色度传感器测得吸收率为上图中a点,则
 ,
, 菠菜中含铁
菠菜中含铁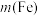 =
=
您最近一年使用:0次
2023-01-05更新
|
246次组卷
|
2卷引用:江西省萍乡市2022-2023学年高一上学期期末考试化学试题
解题方法
3 . 菠菜是常见食品,可以补充入体所必需的微量元素铁。某兴趣小组设计实验,探究菠菜中铁元素的价态并测定铁元素的含量,实验流程如下:

(1)上述实验中肯定不会用到下列仪器中的_______(填字母)。
(2)取少许水浸液于试管中,滴入几滴KSCN溶液,振荡,溶液颜色无明显变化,再滴加少量 和
和 ,溶液立即变红。据此探究实验可得到的结论是
,溶液立即变红。据此探究实验可得到的结论是_______ ,请写出滴加 发生反应的离子方程式
发生反应的离子方程式_______ 。
(3)该兴趣小组为了准确测得菠菜中铁的含量,设计如下实验方案:
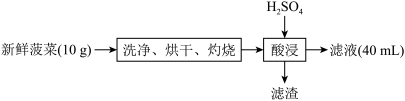
兴趣小组用“分光光度法”测得滤液中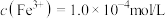 ,该菠菜中铁元素的含量为
,该菠菜中铁元素的含量为_______ mg/100g(保留三位有效数字)

(1)上述实验中肯定不会用到下列仪器中的_______(填字母)。
A. | B. | C. | D. |
 和
和 ,溶液立即变红。据此探究实验可得到的结论是
,溶液立即变红。据此探究实验可得到的结论是 发生反应的离子方程式
发生反应的离子方程式(3)该兴趣小组为了准确测得菠菜中铁的含量,设计如下实验方案:

兴趣小组用“分光光度法”测得滤液中
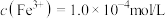 ,该菠菜中铁元素的含量为
,该菠菜中铁元素的含量为
您最近一年使用:0次
名校
4 . 为了测定铁铜合金的组成,将15.2g铁、铜合金加入200mL某浓度的稀硝酸中,待合金完全溶解后,共收集到NO气体4.48L(标准状况下),并测得反应后溶液中H+的浓度为0.5mol·L-1。若反应前后溶液的体积变化忽略不计,则下列判断正确的是
| A.反应后的溶液中可继续溶解铁铜合金质量最多为1.9g |
| B.上述合金中铁与铜的质量之比为2:3 |
| C.合金中,铁的质量分数为63.2% |
| D.原硝酸的物质的量浓度为c(HNO3)=4.5mol·L-1 |
您最近一年使用:0次
2021-06-23更新
|
2488次组卷
|
10卷引用:江西省新余市2021-2022学年高一下学期期末考试化学试题
江西省新余市2021-2022学年高一下学期期末考试化学试题江苏省南京市六校联考2020-2021学年高一下学期期末考试化学试题湖南长沙麓山国际实验中学2022-2023学年高一上学期期末线上化学试题(已下线)重难点03 氮及其化合物-【好题汇编】备战2023-2024学年高一化学下学期期末真题分类汇编(江苏专用)(已下线)考点12 氮及其化合物-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点12 氮及其化合物-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)专题07 常见非金属及其化合物-备战2022年高考化学学霸纠错(全国通用)宁夏石嘴山市第三中学2021-2022学年高三上学期第二次月考化学试题湖北省应城市第一高级中学2022-2023学年高一下学期第二次阶段性检测化学试题浙江金华第一中学2023-2024学年高一下学期4月期中考试化学试题
5 . 实验目的:为研究铁质材料与热浓硫酸的反应
(1)称取铁钉(碳素钢 ) 放入
放入 浓硫酸中,加热,充分反应后得到溶液
浓硫酸中,加热,充分反应后得到溶液 并收集到气体
并收集到气体 。
。
①甲同学认为 中除
中除 外还可能含有
外还可能含有 。若要确认其中是否含有
。若要确认其中是否含有 ,应选择加入的试剂为
,应选择加入的试剂为___________ (选填序号)
A. 溶液和氯水 B.铁粉和
溶液和氯水 B.铁粉和 溶液 C.浓氨水 D.酸性
溶液 C.浓氨水 D.酸性 溶液
溶液
②乙同学取 (标准状况)气体
(标准状况)气体 通入足量溴水中,然后加入足量
通入足量溴水中,然后加入足量 溶液,经适当操作后得到干燥固体
溶液,经适当操作后得到干燥固体 。据此推知气体
。据此推知气体 中
中 的体积分数为
的体积分数为___________ 。(保留三位有效数字)。
(2)分析上述实验中 体积分数的结果,丙同学认为气体Y中还可能含量有
体积分数的结果,丙同学认为气体Y中还可能含量有 和
和 气体。为此设计了下列探究实验装置(图中夹持仪器省略)。气体Y中还有
气体。为此设计了下列探究实验装置(图中夹持仪器省略)。气体Y中还有 的原因是
的原因是___________ 。

(3)装置A中试剂的作用是___________ ,反应的离子方程式___________ 。
(4)简述确认气体Y中含有 的实验现象
的实验现象___________ 。
(5)如果气体Y中含有 ,预计实验现象应是
,预计实验现象应是___________ 。
(1)称取铁钉(
 放入
放入 浓硫酸中,加热,充分反应后得到溶液
浓硫酸中,加热,充分反应后得到溶液 并收集到气体
并收集到气体 。
。①甲同学认为
 中除
中除 外还可能含有
外还可能含有 。若要确认其中是否含有
。若要确认其中是否含有 ,应选择加入的试剂为
,应选择加入的试剂为A.
 溶液和氯水 B.铁粉和
溶液和氯水 B.铁粉和 溶液 C.浓氨水 D.酸性
溶液 C.浓氨水 D.酸性 溶液
溶液②乙同学取
 (标准状况)气体
(标准状况)气体 通入足量溴水中,然后加入足量
通入足量溴水中,然后加入足量 溶液,经适当操作后得到干燥固体
溶液,经适当操作后得到干燥固体 。据此推知气体
。据此推知气体 中
中 的体积分数为
的体积分数为(2)分析上述实验中
 体积分数的结果,丙同学认为气体Y中还可能含量有
体积分数的结果,丙同学认为气体Y中还可能含量有 和
和 气体。为此设计了下列探究实验装置(图中夹持仪器省略)。气体Y中还有
气体。为此设计了下列探究实验装置(图中夹持仪器省略)。气体Y中还有 的原因是
的原因是
(3)装置A中试剂的作用是
(4)简述确认气体Y中含有
 的实验现象
的实验现象(5)如果气体Y中含有
 ,预计实验现象应是
,预计实验现象应是
您最近一年使用:0次
2021-10-10更新
|
285次组卷
|
5卷引用:2014-2015江西省临川市第一中学高一上学期期末化学试卷
解题方法
6 . 高效净水剂聚合氯化铝铁(PAFC)的组成可表示为[AlFe(OH)nCl6-n]m,该物质广泛应用于日常生活用水和工业废水的处理。
(1)为检测PAFC中铝和铁元素的含量,采用如图所示流程进行:
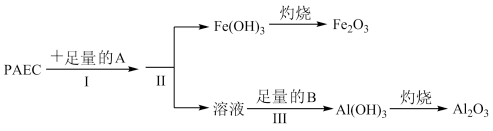
回答下列问题:
①PAFC中铁元素的化合价为__________ 。
②步骤I中的试剂A是__________ (从氢氧化钠溶液、氨水中选择)步骤III中的试剂B是__________ 。
③步骤II的操作是__________ 。
(2)某工厂欲以工业废料(铁、铁和铝的氧化物)为原料制取PAFC,设计如下流程:
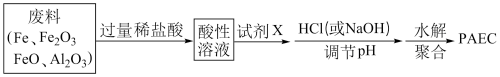
①所得酸性溶液中,不能确定是否一定存在的阳离子是_________ (填序号)。
A.Al3+ B.Fe2+ C.Fe3+ D.H+
为证明该离子确实存在,可采用的操作(必须指明所采用的试剂及观察到的现象)是:_____ 。
②往酸性溶液中加入试剂X的目的是(用离子方程式表示)___________ 。
(1)为检测PAFC中铝和铁元素的含量,采用如图所示流程进行:

回答下列问题:
①PAFC中铁元素的化合价为
②步骤I中的试剂A是
③步骤II的操作是
(2)某工厂欲以工业废料(铁、铁和铝的氧化物)为原料制取PAFC,设计如下流程:

①所得酸性溶液中,不能确定是否一定存在的阳离子是
A.Al3+ B.Fe2+ C.Fe3+ D.H+
为证明该离子确实存在,可采用的操作(必须指明所采用的试剂及观察到的现象)是:
②往酸性溶液中加入试剂X的目的是(用离子方程式表示)
您最近一年使用:0次
名校
7 . 往 100 g FeCl3 和 CuCl2 的混合溶液中加入铁粉。已知 FeCl3会先与铁粉发生反应:2FeCl3 + Fe =3FeCl2。下图为加入铁粉的质量与反应后剩余固体质量关系。下列说法不正确的是


| A.D 点对应纵坐标为 6.4 |
| B.B 点后溶液的颜色为蓝色 |
| C.该 100 g 溶液中的 CuCl2质量分数为 13.5% |
| D.取 DE 两点间(不含 D)的剩余固体加入盐酸,均有气泡产生 |
您最近一年使用:0次
2017-08-25更新
|
554次组卷
|
8卷引用:江西省南昌市第十中学2019-2020学年高一上学期期末考试化学试题
江西省南昌市第十中学2019-2020学年高一上学期期末考试化学试题(已下线)【南昌新东方】南昌十中2019-2020 高一(上)期末河南省许昌市长葛市第一高级中学2019-2020学年高一下学期期末考试化学试题四川省成都市第七中学2017-2018学年高一上学期入学考试化学试题新疆阿克苏市农一师中学2018届高三上学期第二次月考化学试题(已下线)第三章 铁 金属材料(能力提升)-2020-2021学年高一化学单元测试定心卷(人教版2019必修第一册)(已下线)第三章 金属及其化合物(能力提升)-2020-2021学年高一化学单元测试定心卷(人教版必修1)(已下线)3.2.3 铁的重要化合物(重点练)-2020-2021学年高一化学上学期十分钟同步课堂专练(人教版)
名校
8 . 硫酸亚铁晶体(FeSO4·7H2O)在医药上作补血剂。某课外小组测定该补血剂中铁元素的含量。实验步骤如下:

请回答下列问题:
(1)步骤①滤液中滴加KSCN溶液后滤液变为红色,则该溶液中含有__________________ (填离子符号),检验滤液中还存在Fe2+的方法为_________________________________________ 。(注明试剂、现象)
(2)步骤②加入过量H2O2的目的:____________________________________________ 。
(3)步骤③中反应的离子方程式:_____________________________________________ 。
(4)若实验无损耗,则每片补血剂含铁元素的质量__________ g。

请回答下列问题:
(1)步骤①滤液中滴加KSCN溶液后滤液变为红色,则该溶液中含有
(2)步骤②加入过量H2O2的目的:
(3)步骤③中反应的离子方程式:
(4)若实验无损耗,则每片补血剂含铁元素的质量
您最近一年使用:0次



