名校
解题方法
1 . 根据要求完成下列方程式。
(1)K3[Fe(C2O4)3]·3H2O(三草酸合铁酸钾)为亮绿色晶体,可用于晒制蓝图。晒制蓝图时,用K3[Fe(C2O4)3]·3H2O作感光剂,其光解反应的化学方程式为:2K3[Fe(C2O4)3] 2FeC2O4 +3K2C2O4 +2CO2↑。
2FeC2O4 +3K2C2O4 +2CO2↑。
①草酸亚铁在隔绝空气的条件下加热会分解,可以制得黑色粉末状的氧化亚铁,写出该反应的化学方程式___________ 。
②氢氧化亚铁的制备过程中要注意隔绝空气,否则白色沉淀会迅速转化为灰绿色,最后得到红褐色物质,写出该转化过程的化学方程式___________ 。
③高铁酸钠是新型的净水剂,在强碱中氢氧化铁可以被氯气氧化生成紫色的高铁酸根,完成该反应的离子方程式___________ 。
(2)黄血盐(K4[Fe(CN)6] )是合法的食品添加剂,用作抗结剂;黄血盐在溶液中遇到Fe3+ ,生成普鲁士蓝沉淀。
①铊是一种剧毒化学品,若出现了中毒症状,应立即就医,在医学上,医生通常建议中毒者服用一种可溶性普鲁士蓝(KFe[Fe(CN)6])解毒,Tl+ 与K+ 性质接近,铊可置换普鲁士兰中的钾后,形成不溶性物质,随粪便排出,对治疗经口急慢性铊中毒有一定疗效,写出解铊毒反应的离子方程式___________ 。
②无水黄血盐可被浓硫酸分解,生成三种常见的盐和一种常见的无色无味气体,分析完成该反应的化学方程式___________ 。(提示:反应中价态不变)
(3)基于生成滕氏蓝的化学反应原理发展起来的晒制蓝图技术在复印机诞生之前广泛用于工程图纸的复制。赤血盐溶液遇到Fe2+ ,可以生成蓝色的滕氏蓝沉淀,写出得到滕氏蓝沉淀反应的离子方程式___________ 。(已知:氯气遇到黄血盐可以得到赤血盐)
(1)K3[Fe(C2O4)3]·3H2O(三草酸合铁酸钾)为亮绿色晶体,可用于晒制蓝图。晒制蓝图时,用K3[Fe(C2O4)3]·3H2O作感光剂,其光解反应的化学方程式为:2K3[Fe(C2O4)3]
 2FeC2O4 +3K2C2O4 +2CO2↑。
2FeC2O4 +3K2C2O4 +2CO2↑。①草酸亚铁在隔绝空气的条件下加热会分解,可以制得黑色粉末状的氧化亚铁,写出该反应的化学方程式
②氢氧化亚铁的制备过程中要注意隔绝空气,否则白色沉淀会迅速转化为灰绿色,最后得到红褐色物质,写出该转化过程的化学方程式
③高铁酸钠是新型的净水剂,在强碱中氢氧化铁可以被氯气氧化生成紫色的高铁酸根,完成该反应的离子方程式
(2)黄血盐(K4[Fe(CN)6] )是合法的食品添加剂,用作抗结剂;黄血盐在溶液中遇到Fe3+ ,生成普鲁士蓝沉淀。
①铊是一种剧毒化学品,若出现了中毒症状,应立即就医,在医学上,医生通常建议中毒者服用一种可溶性普鲁士蓝(KFe[Fe(CN)6])解毒,Tl+ 与K+ 性质接近,铊可置换普鲁士兰中的钾后,形成不溶性物质,随粪便排出,对治疗经口急慢性铊中毒有一定疗效,写出解铊毒反应的离子方程式
②无水黄血盐可被浓硫酸分解,生成三种常见的盐和一种常见的无色无味气体,分析完成该反应的化学方程式
(3)基于生成滕氏蓝的化学反应原理发展起来的晒制蓝图技术在复印机诞生之前广泛用于工程图纸的复制。赤血盐溶液遇到Fe2+ ,可以生成蓝色的滕氏蓝沉淀,写出得到滕氏蓝沉淀反应的离子方程式
您最近一年使用:0次
2 . 铁是人体必需的微量元素之一,菠菜、黑木耳等食品中富含铁元素,其中菠菜中的铁元素至要以草酸亚铁 的形式存在,草酸亚铁粉末难溶于水。某小组设计实验检验和测定菠菜中的铁元素。
的形式存在,草酸亚铁粉末难溶于水。某小组设计实验检验和测定菠菜中的铁元素。
(1)草酸亚铁溶于稀硫酸的化学方程式是_______ 。
(2)菠菜的预处理

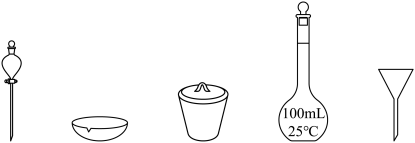
上述预处理流程中需要用到的仪器有烧杯、玻璃棒、酒精灯、_______ (从下图中选择,写出名称)。
(3)检验待测液中是否含有 、
、
(4)利用 标准溶液测定菠菜中铁元素的含量
标准溶液测定菠菜中铁元素的含量
步骤I:取10.00mL待测液于锥形瓶中,滴加 溶液至溶液显紫色。
溶液至溶液显紫色。
步骤II:向步骤I得到的混合液中加入过量锌粉至反应完全后,过滤、洗涤,将滤液及洗涤液全部收集到锥形瓶中。
步骤III:向步骤II所得待测液中加入适量稀 溶液,用
溶液,用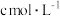 的
的 标准溶液滴定至终点,消耗
标准溶液滴定至终点,消耗 溶液VmL。
溶液VmL。
①步骤I滴加 溶液的目的是
溶液的目的是_______ 。
②步骤III滴加 溶液时发生反应的离子方程式为
溶液时发生反应的离子方程式为_______ 。
 的形式存在,草酸亚铁粉末难溶于水。某小组设计实验检验和测定菠菜中的铁元素。
的形式存在,草酸亚铁粉末难溶于水。某小组设计实验检验和测定菠菜中的铁元素。(1)草酸亚铁溶于稀硫酸的化学方程式是
(2)菠菜的预处理

上述预处理流程中需要用到的仪器有烧杯、玻璃棒、酒精灯、

(3)检验待测液中是否含有
 、
、
| 检验试剂 | 现象 | 结论 |
| ① | 溶液变为红色 | 滤液中含有 |
| ② | ③ | 滤液中含有 |
 标准溶液测定菠菜中铁元素的含量
标准溶液测定菠菜中铁元素的含量步骤I:取10.00mL待测液于锥形瓶中,滴加
 溶液至溶液显紫色。
溶液至溶液显紫色。步骤II:向步骤I得到的混合液中加入过量锌粉至反应完全后,过滤、洗涤,将滤液及洗涤液全部收集到锥形瓶中。
步骤III:向步骤II所得待测液中加入适量稀
 溶液,用
溶液,用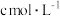 的
的 标准溶液滴定至终点,消耗
标准溶液滴定至终点,消耗 溶液VmL。
溶液VmL。①步骤I滴加
 溶液的目的是
溶液的目的是②步骤III滴加
 溶液时发生反应的离子方程式为
溶液时发生反应的离子方程式为
您最近一年使用:0次
名校
3 . 下列实验目的、实验操作及现象、结论都正确的是
| 选项 | 实验目的 | 实验及现象 | 结论 |
| A | 验证肉桂醛中含碳碳双键 | 向肉桂醛(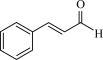 )中加入酸性KMnO4溶液 )中加入酸性KMnO4溶液 | 肉桂醛中含有碳碳双键 |
| B | 比较CuSO4和KMnO4的催化效果 | 向等体积等浓度的H2O2溶液中分别加入5滴等浓度的CuSO4溶液和KMnO4溶液,CuSO4溶液产生气泡速率快 | CuSO4催化H2O2溶液分解效果更好 |
| C | 验证菠菜中含有铁元素 | 将新鲜菠菜剪碎、研磨、溶解、过滤,向滤液中加入几滴KSCN溶液,溶液不变红 | 说明菠菜中不含铁元素 |
| D | 判断强酸和弱酸 | NaHCO3溶液显碱性,NaHSO3溶液显酸性 | 可以确定H2CO3是弱酸,无法判断H2SO3是否为弱酸 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-06-19更新
|
787次组卷
|
2卷引用:江西省赣州地区2023-2024学年十大教学能手选拔赛高中化学试题
解题方法
4 . 铁华粉最早记载于《开宝本草》,为铁粉与醋作用后的锈末,具有养血安神、平肝镇惊的功效,主治血虚、健忘。利用铁华粉进行的实验及其现象如下所示:
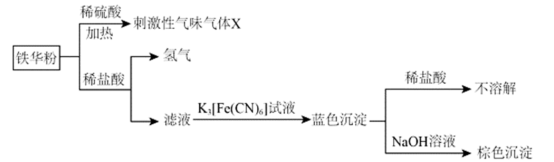
下列相关说法错误的是

下列相关说法错误的是
| A.X为醋酸 |
B.铁华粉中起治疗作用的成分可能为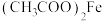 |
C.生成蓝色沉淀的离子方程式为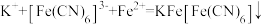 |
D.由上述实验可知, 结合 结合 的能力大于 的能力大于 |
您最近一年使用:0次
解题方法
5 . 根据下列操作及现象,能达到目的是
| 选项 | 操作及现象 | 实验目的 |
| A | 向20mLNa2CO3和NaOH混合溶液中,滴入几滴酚酞试液,用0.1000mol/L盐酸标准溶液滴定至粉红色 | 测定NaOH的浓度 |
| B | 向溶有SO2的BaCl2溶液中加入Fe(NO3)3溶液,有白色沉淀生成 | 说明 具有强氧化性 具有强氧化性 |
| C | 向5mL0.1mol/LKI溶液中滴加1mL0.1mol/LFeCl3溶液,充分反应后再滴加少量KSCN溶液,溶液变红 | 证明KI与FeCl3的反应属于可逆反应 |
| D | 分别向2mL乙醇和乙二醇中加入一粒绿豆大小的金属钠,乙二醇产生气泡的速度更快 | 证明乙二醇中羟基数目多 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
6 . 下列实验操作及现象均正确的是
| 选项 | 实验目的 | 实验操作 | 实验现象 |
| A | 探究硼酸和碳酸的酸性强弱 | 将足量硼酸滴入Na2CO3溶液中 | 有气泡产生 |
| B | 验证铜和浓硫酸反应的产物中有硫酸铜生成 | 直接向反应后的试管中加入蒸馏水 | 溶液变蓝 |
| C | 探究维生素C可以还原Fe3+ | 向盛有FeCl3溶液的试管中滴加适量浓维生素C溶液 | 溶液由黄色变为浅绿色 |
| D | 探究Fe3+和I-之间的反应为可逆反应 | 向氯化铁溶液中滴入少量 KI溶液,将反应后的溶液两等分,向其中一份滴入KSCN溶液,另一份滴淀粉溶液 | 一份溶液显血红色,另一份溶液显蓝色 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
7 . 下述实验能达到预期目的的是
| 编号 | 实验内容 | 实验目的 |
| A | 测同温同浓度Na2CO3和Na2SiO3水溶液的pH | 确定碳和硅两元素非金属性强弱 |
| B | 取久置的绿矾(FeSO4·7H2O)溶于水,加入KSCN溶液,观察溶液是否变为血红色 | 证明绿矾是否全部被氧化 |
| C | 取一定量铝箔与足量稀盐酸充分反应,逸出的气体通过碱石灰后,测其体积 | 确定铝箔中氧化铝含量 |
| D | 向CH2=CHCHO中滴入酸性KMnO4溶液,观察紫红色是否褪去 | 证明CH2=CHCHO中含有碳碳双键 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
8 . 将a g CuO和铜粉的混合物样品加入到体积为1L的H2SO4和Fe2(SO4)3的混合溶液中,样品完全溶解,溶液中只有Fe2+、Cu2+、H+三种阳离子,且三种阳离子物质的量之比为5︰3︰1(不考虑盐的水解及溶液体积的变化)。若测得反应后溶液的c(H+)=0.1 mol/L,下列说法正确的是
| A.原溶液中c(H2SO4)为0.05 mol/L |
| B.向反应前的溶液中加入足量铁粉,产生的气体体积为4.48L |
| C.混合物中铜的质量分数为60% |
| D.将足量的H2通入灼热的混合物,反应结束后,混合物的质量减少了0.8g |
您最近一年使用:0次
2021-08-06更新
|
1223次组卷
|
10卷引用:2023年第37届中国化学奥林匹克广西预选赛化学试题
2023年第37届中国化学奥林匹克广西预选赛化学试题2023年广西高中学生竞赛(高一、高二同卷)化学试题重庆市南开中学2020-2021学年高一上学期期末考试化学试题(已下线)专题六 铁及其化合物(B卷)-2021-2022学年高一化学优选好题单元专题双测卷(人教版2019必修第一册)(已下线)专题3.1.3 铁盐与亚铁盐(备作业)-【上好课】2021-2022学年高一化学同步备课系列(人教版2019必修第一册)江苏省泰州中学2021-2022学年高一上学期第二次月度检测化学试题湖北省荆州中学2021-2022学年高一上学期期末考试化学试题重庆市第七中学校2021-2022高一上学期第四次月检测化学试题湖北省襄阳市第四中学2021-2022学年高一下学期2月考试化学试题内蒙古鄂尔多斯市第一中学2022-2023 学年高一上学期期末考试化学试题
名校
解题方法
9 . 正三价铁元素有一定的氧化性,FeCl3溶液吸收 一定量SO2后溶液颜色发生变化。
(1)反应的离子方程式为_______ 。
(2)除H+、OH-、H2O外,上述反应后的溶液中一定含有的粒子有_______(填编号)。
(3)对还不能确定的粒子存在情况提出合理的假设:
假设1:只存在Fe3+;
假设2:只存在_______ ;
假设3:_______ 。
(4)设计实验方案进行实验。写出实验步骤以及预期现象和结论。
限选实验试剂: 3mol·L-1 H2SO4、l mol·L-1 NaOH、0.01 mol·L-1 KMnO4、20%KSCN、3%H2O2、淀粉- KI溶液、紫色石蕊试液、品红溶液。
(1)反应的离子方程式为
(2)除H+、OH-、H2O外,上述反应后的溶液中一定含有的粒子有_______(填编号)。
| A.Fe2+ | B.Fe3+ | C.Cl- | D.SO | E.H2SO3 |
假设1:只存在Fe3+;
假设2:只存在
假设3:
(4)设计实验方案进行实验。写出实验步骤以及预期现象和结论。
限选实验试剂: 3mol·L-1 H2SO4、l mol·L-1 NaOH、0.01 mol·L-1 KMnO4、20%KSCN、3%H2O2、淀粉- KI溶液、紫色石蕊试液、品红溶液。
| 实验步骤 | 预期现象和结论 |
| 步骤1: | |
| 步骤2: |
您最近一年使用:0次
2021-08-03更新
|
184次组卷
|
2卷引用:湖南省2012年高中学生化学竞赛试卷(B卷)
解题方法
10 . 某工厂利用FeCl3溶液腐蚀镀有铜的绝缘板生产电路板,一实验小组对该厂生产电路后所得的废液进行分析。取50.0mL废液,向其中加入0.64gCu,金属铜全部溶解。另取50.0mL废液,向其中加入足量的AgNO3,析出沉淀43.05g,下列说法正确的是
| A.原废液中含有的金属阳离子只有Fe2+和Cu2+ |
| B.该工厂原来使用的FeCl3溶液的物质的量浓度约为2mol/L |
| C.若向500mL废液中加入足量的稀HNO3溶液,在标况下产生NO气体4.48L,则原废液中Fe2+和Cu2+的物质的量浓度之比为2:1 |
| D.可以使用硫氰化钾溶液检验该废液中是否含有Fe2+ |
您最近一年使用:0次



