1 . 某同学在学习元素化合物知识的过程中,发现含有相同元素的物质间在一定条件下存在转化规律。含甲元素的部分物质可发生如下转化。

其中,A、B、C中甲元素的化合价依次升高;B,C为同类物质,且所含元素种类相同。请回答:
(1)若A是空气中含量最多的气体,C为红棕色气体。
①甲元素在元素周期表中的位置是______ 。
②下列说法正确的是______ (填字母)。
(2)若A为金属单质,C溶液遇KSCN溶液呈红色,F为黄绿色气体。
①B溶液与F反应的离子方程式是______ 。
②当5.6gA全部转化为D时,转移电子的物质的量为______ mol。

其中,A、B、C中甲元素的化合价依次升高;B,C为同类物质,且所含元素种类相同。请回答:
(1)若A是空气中含量最多的气体,C为红棕色气体。
①甲元素在元素周期表中的位置是
②下列说法正确的是
a.E、F可为氧气 b.常温下,B可为无色气体 c.③中甲元素的化合价发生了变化
(2)若A为金属单质,C溶液遇KSCN溶液呈红色,F为黄绿色气体。
①B溶液与F反应的离子方程式是
②当5.6gA全部转化为D时,转移电子的物质的量为
您最近一年使用:0次
2 . A、B、C、D、E、X是中学常见的无机物,存在如图转化关系(部分生成物和反应条件略去)。
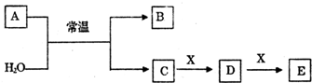
(1)若A为常见的金属单质,焰色反应呈黄色,X能使品红溶液褪色,写出C和E反应的离子方程式________________________________________ 。
(2)若A为电石(CaC2),X为深红棕色液体非金属单质,写出D + X → E反应的化学方程式为________________________________ 。
(3)若A为淡黄色粉末,回答下列问题:
①A与H2O反应的离子方程式为__________________________________ 。
②若X为非金属单质,通常为黑色粉末,写出D的结构式为______________ 。
③若X为一种造成温室效应的气体.则鉴别等浓度的D、E两种溶液,可选择的试剂为_________ 。
a.盐酸 b.BaCl2溶液 c.NaOH溶液 d.Ca(OH)2溶液
(4)若A为氧化物,X为常见的金属单质,在溶液D中滴加KSCN溶液会变红色。
①A与H2O反应的化学反应方程式为__________________________________ 。
②指明X 在元素周期表中位置为________________________ 。

(1)若A为常见的金属单质,焰色反应呈黄色,X能使品红溶液褪色,写出C和E反应的离子方程式
(2)若A为电石(CaC2),X为深红棕色液体非金属单质,写出D + X → E反应的化学方程式为
(3)若A为淡黄色粉末,回答下列问题:
①A与H2O反应的离子方程式为
②若X为非金属单质,通常为黑色粉末,写出D的结构式为
③若X为一种造成温室效应的气体.则鉴别等浓度的D、E两种溶液,可选择的试剂为
a.盐酸 b.BaCl2溶液 c.NaOH溶液 d.Ca(OH)2溶液
(4)若A为氧化物,X为常见的金属单质,在溶液D中滴加KSCN溶液会变红色。
①A与H2O反应的化学反应方程式为
②指明X 在元素周期表中位置为
您最近一年使用:0次
名校
3 . 高铁酸钾(K2FeO4)为高效净水剂,紫色固体,易溶于水,微溶于KOH溶液,具有强氧化性,在酸性溶液中完全、快速产生O2,在碱性溶液中较稳定。某实验小组制备高铁酸钾并探究性质。
(1)制备K2FeO4 (夹持装置略)

①Fe元素在元素周期表中的位置为__ 。
②A为氯气发生装置,A中离子反应方程式是__ 。
③将除杂装置B补充完整并标明所用试剂__ 。
④C中得到紫色固体和溶液,C中发生的主要反应为__ (用化学方程式表示)。
(2)探究K2FeO4的性质
①取C中紫色溶液,加入稀硫酸,产生黄绿色气体,得溶液a,经检验气体中含有Cl2,为证明是否K2FeO4氧化了Cl-而产生Cl2,设计以下方案:
i.由方案1中溶液变红可知a中含有__ 离子,但该离子的产生不能判断一定是K2FeO4将Cl-氧化,还可能有__ 产生(用化学式表示)。
ii.方案Ⅱ可证明K2FeO4氧化了Cl-,用KOH溶液洗涤的目的是__ 。
②根据K2FeO4的制备实验得出:氧化性Cl2__ FeO (填“>”或“<”),而方案Ⅱ实验表明,Cl2和FeO
(填“>”或“<”),而方案Ⅱ实验表明,Cl2和FeO 的氧化性强弱关系相反,原因是
的氧化性强弱关系相反,原因是__ 。
③资料表明,酸性溶液中的氧化性FeO >MnO
>MnO ,验证实验如下:将溶液b滴入MnSO4和足量H2SO4的混合溶液中,振荡后溶液呈浅紫色,该现象能否证明氧化性FeO
,验证实验如下:将溶液b滴入MnSO4和足量H2SO4的混合溶液中,振荡后溶液呈浅紫色,该现象能否证明氧化性FeO >MnO
>MnO ,若能,请说明理由;若不能,进一步设计实验方案,理由或方案:
,若能,请说明理由;若不能,进一步设计实验方案,理由或方案:__ 。
(1)制备K2FeO4 (夹持装置略)

①Fe元素在元素周期表中的位置为
②A为氯气发生装置,A中离子反应方程式是
③将除杂装置B补充完整并标明所用试剂
④C中得到紫色固体和溶液,C中发生的主要反应为
(2)探究K2FeO4的性质
①取C中紫色溶液,加入稀硫酸,产生黄绿色气体,得溶液a,经检验气体中含有Cl2,为证明是否K2FeO4氧化了Cl-而产生Cl2,设计以下方案:
| 方案Ⅰ | 取少量a,滴加KSCN溶液至过量,溶液呈红色 |
| 方案Ⅱ | 用KOH溶液充分洗涤 中所得固体,再用KOH溶液将K2FeO4溶出,得到紫色溶液b,取少量b,滴加盐酸,有Cl2产生。 中所得固体,再用KOH溶液将K2FeO4溶出,得到紫色溶液b,取少量b,滴加盐酸,有Cl2产生。 |
ii.方案Ⅱ可证明K2FeO4氧化了Cl-,用KOH溶液洗涤的目的是
②根据K2FeO4的制备实验得出:氧化性Cl2
 (填“>”或“<”),而方案Ⅱ实验表明,Cl2和FeO
(填“>”或“<”),而方案Ⅱ实验表明,Cl2和FeO 的氧化性强弱关系相反,原因是
的氧化性强弱关系相反,原因是③资料表明,酸性溶液中的氧化性FeO
 >MnO
>MnO ,验证实验如下:将溶液b滴入MnSO4和足量H2SO4的混合溶液中,振荡后溶液呈浅紫色,该现象能否证明氧化性FeO
,验证实验如下:将溶液b滴入MnSO4和足量H2SO4的混合溶液中,振荡后溶液呈浅紫色,该现象能否证明氧化性FeO >MnO
>MnO ,若能,请说明理由;若不能,进一步设计实验方案,理由或方案:
,若能,请说明理由;若不能,进一步设计实验方案,理由或方案:
您最近一年使用:0次
解题方法
4 . 硫酸亚铁铵[(NH4)2Fe(SO4)2•6H2O,相对分子质量392]晶体又称莫尔盐,易溶易电离但却比一般的亚铁盐稳定,因此广泛应用于制药、电镀以及定量分析。回答下列与之有关的问题:
(1)在莫尔盐所涉及的五种元素中:
①S元素在门捷列夫元素周期表中的位置是______________ ;
②其中处于同主族的两种元素非金属性更强的是:_____________ 。
(2)为检验莫尔盐是否变质,可用的试剂为_______________ 。
碘是合成人体甲状腺激素的重要原料,食盐中加KIO3是我国为解决普遍性碘缺乏问题的国家规定,下图是自动电位滴定法测定食盐中碘含量的实验过程:
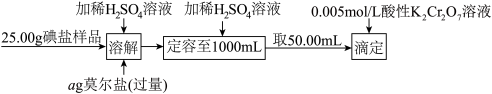
(3)已知“溶解”过程中IO3-的还原产物为碘单质,写出该反应的离子反应方程式:______________________________ 。
(4)取50. 00 mL样品,用0.005 mol/L酸性K2Cr2O7溶液滴定剩余Fe2+,滴定操作时使用的锥形瓶未干燥,导致结果_____________ (填“偏大”“偏小”或“无影响”)
(1)在莫尔盐所涉及的五种元素中:
①S元素在门捷列夫元素周期表中的位置是
②其中处于同主族的两种元素非金属性更强的是:
(2)为检验莫尔盐是否变质,可用的试剂为
碘是合成人体甲状腺激素的重要原料,食盐中加KIO3是我国为解决普遍性碘缺乏问题的国家规定,下图是自动电位滴定法测定食盐中碘含量的实验过程:

(3)已知“溶解”过程中IO3-的还原产物为碘单质,写出该反应的离子反应方程式:
(4)取50. 00 mL样品,用0.005 mol/L酸性K2Cr2O7溶液滴定剩余Fe2+,滴定操作时使用的锥形瓶未干燥,导致结果
您最近一年使用:0次
名校
5 . W是由A、B两种元素组成的AB2型化合物。
(1)若W和焦炭在高温下发生反应,所制得的半导体材料应用广泛。则W为________________ (填化学式)。
(2)若取两支试管分别加入少量W溶液,往一支试管中滴入KSCN溶液,无明显现象。往另一支试管中加入足量氯水,再加入适量CCl4,振荡,静置,下层溶液呈紫红色;往上层溶液中滴入KSCN溶液,溶液呈红色。
①W溶液中所含金属阳离子为________________ 。
②上述实验中,W与足量氯水反应的离子方程式为_________________________________________________________ 。
(3)若W是离子化合物,其阴、阳离子均含18个电子,且阴、阳离子个数比为1∶1。
①阴离子的电子式为___________________ 。
②1mol W与足量水充分反应,转移电子的物质的量为_____________ mol。
(4)若A、B是同主族元素,W溶于水生成一种二元弱酸。
①B在元素周期表中的位置为______________________________ 。
②如果常温下W为气体,W所形成的二元弱酸溶液中,含A元素的某微粒占所有含A元素微粒的物质的量分数与溶液pH的关系如下图所示,该微粒的化学式为______________________ ;
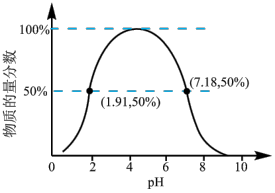
该二元弱酸的一级电离常数为Ka1,则pKa1=—lgKa1≈______________________ 。
③如果A元素的周期序数是B元素的两倍,W的水溶液被双氧水氧化的化学方程式为_________________ 。
(1)若W和焦炭在高温下发生反应,所制得的半导体材料应用广泛。则W为
(2)若取两支试管分别加入少量W溶液,往一支试管中滴入KSCN溶液,无明显现象。往另一支试管中加入足量氯水,再加入适量CCl4,振荡,静置,下层溶液呈紫红色;往上层溶液中滴入KSCN溶液,溶液呈红色。
①W溶液中所含金属阳离子为
②上述实验中,W与足量氯水反应的离子方程式为
(3)若W是离子化合物,其阴、阳离子均含18个电子,且阴、阳离子个数比为1∶1。
①阴离子的电子式为
②1mol W与足量水充分反应,转移电子的物质的量为
(4)若A、B是同主族元素,W溶于水生成一种二元弱酸。
①B在元素周期表中的位置为
②如果常温下W为气体,W所形成的二元弱酸溶液中,含A元素的某微粒占所有含A元素微粒的物质的量分数与溶液pH的关系如下图所示,该微粒的化学式为

该二元弱酸的一级电离常数为Ka1,则pKa1=—lgKa1≈
③如果A元素的周期序数是B元素的两倍,W的水溶液被双氧水氧化的化学方程式为
您最近一年使用:0次
6 . 某同学在学习元素化合物知识的过程中,发现含有相同元素的物质间在一定条件下存在转化规律,绘制出如下转化关系图(部分反应物或产物略去),并用于研究物质A、B、C、D的性质及其变化。
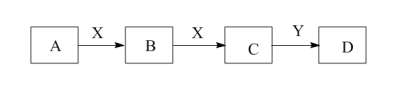
(1)若A是黄绿色气体,X是生活中应用最大量的金属,D是白色固体。
① 组成A的元素在周期表中的位置是______ 。
② 下列说法正确的是______ (填字母)。
a.B的水溶液中加入KSCN溶液,变为红色
b.C只具有还原性
c.若Y是碱,D放置在空气中会迅速变为灰绿色,最终变为红褐色
(2)若A、B、C、D的焰色反应均为黄色,X的固体俗称干冰。
① B转化为C的离子方程式是______ 。
② A用于呼吸面具或潜水艇中氧气的来源,则A和X反应生成1 mol B时,转移电子数为______ 。
③ C与Y反应生成X的离子方程式_________________ 。

(1)若A是黄绿色气体,X是生活中应用最大量的金属,D是白色固体。
① 组成A的元素在周期表中的位置是
② 下列说法正确的是
a.B的水溶液中加入KSCN溶液,变为红色
b.C只具有还原性
c.若Y是碱,D放置在空气中会迅速变为灰绿色,最终变为红褐色
(2)若A、B、C、D的焰色反应均为黄色,X的固体俗称干冰。
① B转化为C的离子方程式是
② A用于呼吸面具或潜水艇中氧气的来源,则A和X反应生成1 mol B时,转移电子数为
③ C与Y反应生成X的离子方程式
您最近一年使用:0次
解题方法
7 . A、B、C均为中学化学中的常见物质,它们含有一种相同的元素。请根据题中信息回答问题。
(1)A、B、C三种物质都由短周期元素组成,D是空气的主要成分之一,它们存在如下反应转化关系:
①若A是非金属单质,常温下为固态,A与C在一定条件下能发生反应,则C为______ ;A所形成的一种晶体具有高硬度、高熔点特性,它的晶体类型属于______
②若A是金属单质,则A在元素周期表的位置是______ ;已知mgA与足量Cl2反应,生成固体的质量为(m+3.55)g,则等质量的A与D反应完全,生成固体的质量至少为______ g
③若常温时C为红棕色气体,则A可能是______ 或______ ;工业上用A与D反应制取B的化学方程式为:______ 。
(2)已知A、B、C、D存在如图所示的反应转化关系:

①若D为生活中常见的金属单质,图中反应均为氧化还原反应,请设计一个检验B中阳离子的方案:________________________________ 。
②若D为强碱,A为常见正盐,A、B、C含有共同元素是生活中常见金属元素,图中反应均为非氧化还原反应,则B是______ ;除去B中混有的少量Mg(OH)2的操作步骤是:___________________ 。(有关答案填写化学式)
(1)A、B、C三种物质都由短周期元素组成,D是空气的主要成分之一,它们存在如下反应转化关系:

①若A是非金属单质,常温下为固态,A与C在一定条件下能发生反应,则C为
②若A是金属单质,则A在元素周期表的位置是
③若常温时C为红棕色气体,则A可能是
(2)已知A、B、C、D存在如图所示的反应转化关系:

①若D为生活中常见的金属单质,图中反应均为氧化还原反应,请设计一个检验B中阳离子的方案:
②若D为强碱,A为常见正盐,A、B、C含有共同元素是生活中常见金属元素,图中反应均为非氧化还原反应,则B是
您最近一年使用:0次
2011·湖北·一模
解题方法
8 . 有关物质存在如图所示转化关系(部分产物已略去)。

已知A、B是均能使澄清石灰水变浑浊的气体。M为无色液体,常用作有机溶剂,其结构与A相似且为非极性分子。C、E均难溶于水且E难溶于酸。
(1)单质N在X中燃烧可形成一种具有磁性的黑色物质,则构成N的元素在周期表中的位置为___________________________________ 。
(2)M的电子式为_______________________ ,Y的化学式为____________________ 。
(3)①写出离子方程式:A→C________________________________________________
②检验O中阴离子的方法为____________________________________________________________________________
(4)将M滴入O溶液中,观察到溶液变浑浊,请推断反应的化学方程式:___________________________________________ 。

已知A、B是均能使澄清石灰水变浑浊的气体。M为无色液体,常用作有机溶剂,其结构与A相似且为非极性分子。C、E均难溶于水且E难溶于酸。
(1)单质N在X中燃烧可形成一种具有磁性的黑色物质,则构成N的元素在周期表中的位置为
(2)M的电子式为
(3)①写出离子方程式:A→C
②检验O中阴离子的方法为
(4)将M滴入O溶液中,观察到溶液变浑浊,请推断反应的化学方程式:
您最近一年使用:0次



