1 . 在下列溶液中离子一定能大量共存的是
A.Na+、Ba2+、SO 、SO 、SO | B.Fe3+、Na+、I-、OH- |
C.K+、Na+、NO 、Cl- 、Cl- | D.NH 、Al3+、SO 、Al3+、SO 、OH- 、OH- |
您最近一年使用:0次
名校
解题方法
2 . 阅读下面科普信息,回答问题:
一个体重50kg的健康人含铁2g,这2g铁在人体中以Fe2+和Fe3+的形式存在。亚铁离子易被吸收,给贫血者补充铁时,应给予含亚铁离子的亚铁盐,如硫酸亚铁。服用维生素C,可使食物中的铁离子还原成亚铁离子,有利于铁的吸收。
(1)从铁元素的化合价角度看,Fe3+具有的性质是____ 。
(2)向沸水中滴加几滴饱和FeCl3溶液,至液体呈透明的红褐色,该分散系区别于其它分散系的本质是____ 。
(3)工业盐的主要成分是NaNO2,曾多次发生过因误食NaNO2而中毒的事件,其原因是NaNO2把人体内的Fe2+转化为Fe3+而失去与O2结合的能力。下列也能实现上述转化的物质是____ 。
A.Cl2 B.NaOH C.Fe D.KMnO4(H+)
工业盐中毒后,可服用维生素C来缓解中毒状况,这说明维生素C具有____ 性。
(4)电子工业需用30%的FeCl3溶液腐蚀敷在绝缘板上的铜,制造印刷电路板。请写出FeCl3溶液与铜反应的离子方程式____ ,检验反应后的溶液中还存在Fe3+的试剂及现象分别是____ ,____ 。
一个体重50kg的健康人含铁2g,这2g铁在人体中以Fe2+和Fe3+的形式存在。亚铁离子易被吸收,给贫血者补充铁时,应给予含亚铁离子的亚铁盐,如硫酸亚铁。服用维生素C,可使食物中的铁离子还原成亚铁离子,有利于铁的吸收。
(1)从铁元素的化合价角度看,Fe3+具有的性质是
(2)向沸水中滴加几滴饱和FeCl3溶液,至液体呈透明的红褐色,该分散系区别于其它分散系的本质是
(3)工业盐的主要成分是NaNO2,曾多次发生过因误食NaNO2而中毒的事件,其原因是NaNO2把人体内的Fe2+转化为Fe3+而失去与O2结合的能力。下列也能实现上述转化的物质是
A.Cl2 B.NaOH C.Fe D.KMnO4(H+)
工业盐中毒后,可服用维生素C来缓解中毒状况,这说明维生素C具有
(4)电子工业需用30%的FeCl3溶液腐蚀敷在绝缘板上的铜,制造印刷电路板。请写出FeCl3溶液与铜反应的离子方程式
您最近一年使用:0次
名校
3 . A~H分别表示中学化学中常见的某种物质,它们之间的相互转化关系如图所示(部分反应物、生成物未列出)。已知:C、D、E、F、G五种物质中均含有同一种元素;A为淡黄色固体化合物;G为红褐色固体,;C是一种黑色固体,具有磁性。
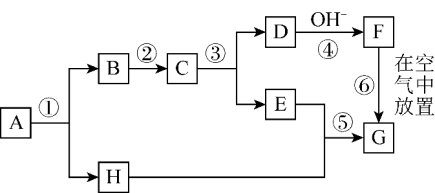
(1)请写出C的化学式____ 。
(2)在D溶液中滴加H溶液,描述发生的现象:____ 。
(3)写出①的化学方程式____ 。写出⑥的化学方程式____ 。
(4)检验E中阳离子可加入溶液,观察到现象是:____ 。

(1)请写出C的化学式
(2)在D溶液中滴加H溶液,描述发生的现象:
(3)写出①的化学方程式
(4)检验E中阳离子可加入溶液,观察到现象是:
您最近一年使用:0次
名校
解题方法
4 . 下列离子方程式正确的是
A.碳酸氢钠溶液中加入盐酸: HCO + H+ = CO2↑ + H2O + H+ = CO2↑ + H2O |
| B.铁粉投入FeCl3溶液中: Fe+ Fe3+=2Fe2+ |
C.向CaCl2溶液中通入CO2: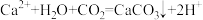 |
| D.氢氧化镁与醋酸作用:Mg(OH)2 + 2H+ = Mg2+ + 2H2O |
您最近一年使用:0次
名校
解题方法
5 . 下列离子方程式正确的是
A. 加入稀硫酸中: 加入稀硫酸中: |
B.向碳酸钙中滴加醋酸溶液: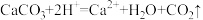 |
C.向氢氧化钡溶液中加入稀硫酸:Ba2++OH- + + H+ =BaSO4↓+H2O + H+ =BaSO4↓+H2O |
| D.氢氧化铁溶于氢碘酸中:OH-+H+= H2O |
您最近一年使用:0次
真题
名校
6 . 无水 常作为芳烃氯代反应的催化剂。某研究小组设计了如下流程,以废铁屑(含有少量碳和
常作为芳烃氯代反应的催化剂。某研究小组设计了如下流程,以废铁屑(含有少量碳和 杂质)为原料制备无水
杂质)为原料制备无水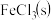 。
。
已知:氯化亚砜(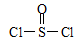 )熔点-101℃,沸点76℃,易水解。
)熔点-101℃,沸点76℃,易水解。
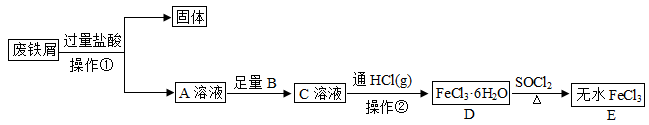
回答问题:
(1)操作①是过滤,用到的玻璃仪器有烧杯、玻璃棒和___________ 。
(2)为避免引入新的杂质,试剂B可以选用___________(填编号)。
(3)操作②是蒸发结晶,加热的同时通入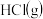 的目的是
的目的是___________ 。
(4)取少量 晶体,溶于水并滴加
晶体,溶于水并滴加 溶液,现象是
溶液,现象是___________ 。
(5)反应 的化学方程式为
的化学方程式为___________ 。
(6)由 转化成
转化成 的过程中可能产生少量亚铁盐,写出一种可能的还原剂
的过程中可能产生少量亚铁盐,写出一种可能的还原剂___________ ,并设计实验验证是该还原剂将 还原
还原___________ 。
 常作为芳烃氯代反应的催化剂。某研究小组设计了如下流程,以废铁屑(含有少量碳和
常作为芳烃氯代反应的催化剂。某研究小组设计了如下流程,以废铁屑(含有少量碳和 杂质)为原料制备无水
杂质)为原料制备无水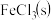 。
。已知:氯化亚砜(
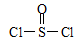 )熔点-101℃,沸点76℃,易水解。
)熔点-101℃,沸点76℃,易水解。
回答问题:
(1)操作①是过滤,用到的玻璃仪器有烧杯、玻璃棒和
(2)为避免引入新的杂质,试剂B可以选用___________(填编号)。
A. 溶液 溶液 | B. 水 水 | C. 水 水 | D. 溶液 溶液 |
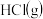 的目的是
的目的是(4)取少量
 晶体,溶于水并滴加
晶体,溶于水并滴加 溶液,现象是
溶液,现象是(5)反应
 的化学方程式为
的化学方程式为(6)由
 转化成
转化成 的过程中可能产生少量亚铁盐,写出一种可能的还原剂
的过程中可能产生少量亚铁盐,写出一种可能的还原剂 还原
还原
您最近一年使用:0次
2021-10-23更新
|
5917次组卷
|
12卷引用:2021年新高考海南化学高考真题
2021年新高考海南化学高考真题2021年海南高考化学试题变式题11-19(已下线)解密06 金属及其化合物(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)解密06 金属及其化合物(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)安徽省黄山市2022-2023学年高二下学期期末考试化学试题(已下线)【知识图鉴】单元讲练测必修第一册第三单元03巩固练(已下线)考点10 铁及其重要化合物(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)(已下线)考点14 铁及其化合物(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)黑龙江省七台河市勃利县高级中学2023-2024学年高三上学期9月月考化学试题(已下线)考点47 无机工艺流程(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)天津市滨海新区田家炳中学2023-2024学年高三上学期期中考试化学试题山东省菏泽外国语学校2023-2024学年高三上学期第一次月考化学试卷
解题方法
7 . 下述实验能达到预期目的是
| 编号 | 实验内容 | 实验目的或结论 |
| A | 将少量 溶液滴加到含有 溶液滴加到含有 、 、 的溶液 的溶液 | 确定 、 、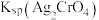 的相对大小 的相对大小 |
| B | 将 与浓 与浓 在蒸馏烧瓶中混合后加热至 在蒸馏烧瓶中混合后加热至 ,将从瓶内逸出的物质依次通过NaOH溶液、溴水 ,将从瓶内逸出的物质依次通过NaOH溶液、溴水 | 检验有无乙烯生成 |
| C | 将铁与稀硝酸混合,充分反应后再向溶液中加入KSCN溶液 | 探究铁能否被氧化成 |
| D | 向 溶液加入少量氯水,观察溶液是否变黄色 溶液加入少量氯水,观察溶液是否变黄色 | 确定 与 与 还原性强弱 还原性强弱 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2021-10-15更新
|
260次组卷
|
2卷引用:2021年海南高考化学试题变式题11-19
解题方法
8 . 下列实验操作或方法,目的可实现的是
| 操作或方法 | 实验目的 | |
| A | 向未知弱酸性试液中滴加含有SCN-的溶液 | 确定试液中Fe2+存在 |
| B | 工业酒精中加入无水硫酸铜 | 确定工业酒精中是否含有水 |
| C | 不加任何试剂 | 鉴别K2SO4、Cu(NO3)2、Ba(OH)2、NaOH |
| D | 通过澄清石灰水 | 鉴别SO2和CO2 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
9 . 下列物质中,可以用来鉴别苯酚、乙醇、苯、NaOH溶液、AgNO3溶液、KSCN溶液的一种试剂是
| A.溴水 | B.新制Cu(OH)2 |
| C.FeCl3溶液 | D.金属钠 |
您最近一年使用:0次
2021-04-16更新
|
261次组卷
|
11卷引用:2021年海南高考化学试题变式题1-10
2021年海南高考化学试题变式题1-10(已下线)2011-2012学年浙江省嘉兴八校高二上学期期中联考理科化学试卷2015-2016学年辽宁省营口市大石桥二中高二上学期期末化学试卷2015-2016学年江西省上高二中高二5月月考化学试卷2015-2016学年吉林梅河口五中高二下期末化学试卷甘肃省临夏中学2018-2019学年高二下学期第二次月考化学试题辽宁省丹东市2017-2018学年高二上学期期末质量监测化学试题江西省南昌市进贤县第一中学2019-2020学年高二下学期第一次月考化学试卷甘肃省武威第六中学2019-2020学年高二下学期第二次学段考试(期末)化学试题(理科)(已下线)【苏州新东方】2020年10月江苏省苏州市高新区第一中学高二化学独立作业山东省菏泽第一中学2021-2022学年高二4月线上检测化学试题
名校
10 . 铁及其重要化合物之间的部分转化关系如图所示。

(1)下列金属矿物中用于冶炼金属铁的是_______ (填序号);
a.金红石(TiO2) b.赤铁矿(Fe2O3) c.辉铜矿(Cu2S)
(2)实现Fe转化为Fe2+可选用足量的_______ (填序号);
a.稀盐酸 b.氢氧化钠溶液 c.稀硝酸
(3)在点燃的条件下,Fe与足量Cl2剧烈反应后,将产物溶于水,再滴加KSCN溶液,则溶液变为_______ 色,证明产物为FeCl3,写出氯气和铁反应的化学方程式为_______ ;
(4)某同学将FeSO4溶液与NaOH溶液混合,未观察到白色沉淀,分析原因是生成的Fe(OH)2易被空气中的O2氧化,请你设计一个防止Fe(OH)2被O2氧化的实验方案_______

(1)下列金属矿物中用于冶炼金属铁的是
a.金红石(TiO2) b.赤铁矿(Fe2O3) c.辉铜矿(Cu2S)
(2)实现Fe转化为Fe2+可选用足量的
a.稀盐酸 b.氢氧化钠溶液 c.稀硝酸
(3)在点燃的条件下,Fe与足量Cl2剧烈反应后,将产物溶于水,再滴加KSCN溶液,则溶液变为
(4)某同学将FeSO4溶液与NaOH溶液混合,未观察到白色沉淀,分析原因是生成的Fe(OH)2易被空气中的O2氧化,请你设计一个防止Fe(OH)2被O2氧化的实验方案
您最近一年使用:0次
2021-04-06更新
|
516次组卷
|
3卷引用:海南省儋州市第二中学2020-2021学年高一下学期3月月考化学(合格考)试题



