14-15高三上·辽宁沈阳·期末
名校
解题方法
1 . 为了验证Fe3+的性质,某化学兴趣小组设计了如图所示的一组实验,其中实验方案设计不合理的是

| A.④ | B.③ |
| C.③④ | D.①②③④⑤ |
您最近一年使用:0次
2023-08-16更新
|
942次组卷
|
43卷引用:第三章 铁 金属材料(A卷·知识通关练)-【单元测试】2022-2023学年高一化学分层训练AB卷(人教版2019必修第一册)
(已下线)第三章 铁 金属材料(A卷·知识通关练)-【单元测试】2022-2023学年高一化学分层训练AB卷(人教版2019必修第一册)(已下线)第三章 铁 金属材料(能力提升)-2020-2021学年高一化学单元测试定心卷(人教版2019必修第一册)新疆乌鲁木齐市第四中学2021-2022学年高一上学期期末考试化学试题宁夏石嘴山市第三中学2021-2022学年高一上学期期末考试化学试题(已下线)第12讲 铁、亚铁盐和铁盐-【暑假自学课】2022年新高一化学暑假精品课(鲁科版2019必修第一册)2014-2015天津市和平区高一上学期期末考试化学试卷2016-2017学年河北石家庄辛集中学高一上阶段考二化学卷河北省辛集中学2017-2018学年高一上学期12月月考化学试题河南省商丘市第一高级中学2017-2018学年高一上学期第二次月考化学试题黑龙江省大庆第一中学2017-2018学年高一上学期期末考试化学试题广西陆川县中学2017-2018学年高一上学期期末考试化学试题吉林省柳河中学2017-2018学年高一上学期期末考试化学试题【全国百强校】河北省石家庄市辛集中学2018-2019学年高一上学期第二次月考化学试题内蒙古自治区翁牛特旗乌丹第一中学2018-2019学年高一上学期期中考试化学试题山东省莒县第一中学2018-2019学年高一上学期12月月考化学试题西藏自治区拉萨市那曲第二高级中学2019-2020学年高一上学期期末考试化学试题河北省张家口市宣化区第一中学2019-2020学年高一3月月考化学试题江西省临川第一中学2019-2020学年高一上学期12月月考化学试题人教版(2019)高一必修第一册 第三章 第一节 铁及其化合物鲁科版(2019)高一必修第一册第3章 物质的性质与转化 第1节 铁的多样性人教版(2019)高一必修第一册 第三章 铁 金属材料 第一节 铁及其化合物(已下线)3.2.3 铁的重要化合物(重点练)-2020-2021学年高一化学上学期十分钟同步课堂专练(人教版)(已下线)3.1.2 铁的重要化合物(重点练)-2020-2021学年高一化学上学期十分钟同步课堂专练(人教版2019必修第一册)云南省普洱市景东彝族自治县第一中学2020-2021学年高一上学期月考化学试题江西省会昌中学2020-2021学年高一上学期第二次月考化学试题江西省新余市第四中学2020-2021学年高一上学期第二次段考化学试题云南省文山州砚山县第三高级中学2020-2021学年高一12月月考化学试题(已下线)3.1.2 铁盐和亚铁盐-2021-2022学年高一化学课后培优练(人教版2019必修第一册)吉林省长春外国语学校2021-2022学年高一上学期第二次月考化学试题(已下线)易错专题23 Fe2+和Fe3+的检验与转化-【突破易错·冲刺满分】2021-2022学年高一上学期化学期中期末易错专题(人教版2019)河北省辛集市第一中学2021-2022学年高一上学期第四次月考化学试题云南省大理市黄冈实验中学2021-2022学年高一上学期12月月考化学试题第2课时 铁盐和亚铁盐第1课时 亚铁盐和铁盐安徽省合肥市第三中学2023-2024学年高一上学期12月份学情调研化学试题(已下线)2014届辽宁省新民市第一高级中学高三上学期期末考试化学试卷(已下线)2015届宁夏银川市唐徕回民中学高三上学期期中考试化学试卷2015-2016学年福建省龙海二中高二下学期期末化学试卷2017届吉林省汪清六中高三上第二次月考化学试卷【校级联考】天津市静海区2019届高三上学期三校联考化学试题北京首都师范大学第二附属中学2021届高三9月月考化学试题上海市控江中学2021-2022学年高二上学期第一次月考化学试卷天津北京师范大学静海附属学校 (天津市静海区北师大实验学校)2023-2024学年高三上学期第二次阶段检测(期中)化学试题
2019高三·全国·专题练习
名校
解题方法
2 . 已知硝酸能将Fe2+氧化为Fe3+。某同学对未知物A盐的水溶液进行了鉴定,实验过程及现象如图所示:

| A.盐A一定是FeCl3 |
| B.白色沉淀B是AgCl |
| C.滤液C中一定含Fe3+ |
| D.无法确定A中是否含有Fe2+ |
您最近一年使用:0次
2023-07-20更新
|
926次组卷
|
9卷引用:第三章 铁 金属材料(A卷·知识通关练)-【单元测试】2022-2023学年高一化学分层训练AB卷(人教版2019必修第一册)
(已下线)第三章 铁 金属材料(A卷·知识通关练)-【单元测试】2022-2023学年高一化学分层训练AB卷(人教版2019必修第一册)(已下线)第三章 章末检测(1)——《高中新教材同步备课》(人教版 必修第一册)安徽省池州市第一中学2020-2021学年高一12月月考化学试题山西省沁县中学2020-2021学年高一上学期第二次月考化学试题江西省新建一中2020-2021学年高一下学期开学考试化学试题作业(十七) 亚铁盐和铁盐陕西省商洛市商州区高级中学2023-2024学年高一下学期3月月考化学试题(已下线)【走进新高考】(人教版必修一)3.2.2几种重要的金属化合物——铁的重要化合物 同步练习02(已下线)考点10 铁及其重要化合物(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)
3 . 为验证氧化性 ,某小组用如图所示装置进行实验(夹持仪器和A中加热装置已省略,气密性已检验)。
,某小组用如图所示装置进行实验(夹持仪器和A中加热装置已省略,气密性已检验)。
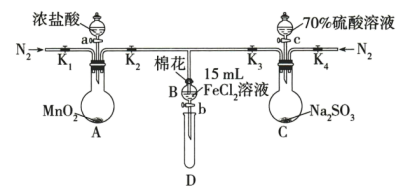
实验过程:
Ⅰ.打开止水夹K1~K4,通入一段时间N2,再将T型导管插入B中,继续通入N2,然后关闭K1,K3,K4。
Ⅱ.打开活塞a,滴加一定量的浓盐酸,给A加热。
Ⅲ.当B中溶液变黄时,停止加热,关闭K2。
Ⅳ.打开活塞b,使约2mL的溶液流入D试管中,检验其中的离子。
Ⅴ.打开K3和活塞c,加入70%的硫酸溶液,一段时间后关闭K3。
Ⅵ.更换试管D,重复过程Ⅳ,检验B中溶液的离子。
(1)过程Ⅰ的目的是_______ 。
(2)若向过程ⅢB中的黄色溶液中通入H2S气体,会观察到有淡黄色沉淀生成,写出该反应的化学方程式:_______ 。
(3)若将制取的SO2通入硫酸酸化的高锰酸钾溶液可使溶液褪色,其反应的离子方程式为_______ 。
(4)甲、乙、丙三位同学分别完成了上述实验,结论如下表所示。他们的检测结果一定能够证明氧化性 的是
的是_______ (填“甲”“乙”或“丙”)。
(5)将B中的FeCl2溶液换成100mLFeBr2溶液并向其中通入22.4LCl2(标准状况下),若溶液中有1/2的Br-被氧化成单质Br2,则原FeBr2溶液中FeBr2的物质的量浓度为_______ 。
 ,某小组用如图所示装置进行实验(夹持仪器和A中加热装置已省略,气密性已检验)。
,某小组用如图所示装置进行实验(夹持仪器和A中加热装置已省略,气密性已检验)。
实验过程:
Ⅰ.打开止水夹K1~K4,通入一段时间N2,再将T型导管插入B中,继续通入N2,然后关闭K1,K3,K4。
Ⅱ.打开活塞a,滴加一定量的浓盐酸,给A加热。
Ⅲ.当B中溶液变黄时,停止加热,关闭K2。
Ⅳ.打开活塞b,使约2mL的溶液流入D试管中,检验其中的离子。
Ⅴ.打开K3和活塞c,加入70%的硫酸溶液,一段时间后关闭K3。
Ⅵ.更换试管D,重复过程Ⅳ,检验B中溶液的离子。
(1)过程Ⅰ的目的是
(2)若向过程ⅢB中的黄色溶液中通入H2S气体,会观察到有淡黄色沉淀生成,写出该反应的化学方程式:
(3)若将制取的SO2通入硫酸酸化的高锰酸钾溶液可使溶液褪色,其反应的离子方程式为
(4)甲、乙、丙三位同学分别完成了上述实验,结论如下表所示。他们的检测结果一定能够证明氧化性
 的是
的是| 过程为Ⅳ,B溶液中含有的离子 | 过程Ⅵ,B溶液中含有的离子 | |
| 甲 | 有Fe3+无Fe2+ | 有Fe2+ |
| 乙 | 既有Fe3+又有Fe2+ | 有 |
| 丙 | 有Fe3+无Fe2+ | 有 |
您最近一年使用:0次
解题方法
4 . 下列转化关系不能通过一步反应实现的是
| A.Fe→FeCl2 | B.Fe2O3→Fe(OH)3 |
| C.FeCl3→FeCl2 | D.Fe(OH)3→FeCl3 |
您最近一年使用:0次
2022-08-15更新
|
819次组卷
|
5卷引用:第三章 铁 金属材料(B卷·能力提升练)-【单元测试】2022-2023学年高一化学分层训练AB卷(人教版2019必修第一册)
(已下线)第三章 铁 金属材料(B卷·能力提升练)-【单元测试】2022-2023学年高一化学分层训练AB卷(人教版2019必修第一册)课前-3.1.2铁及其化合物之间的转化关系(课前)-鲁科版2019必修第一册北京市首师附密云中学2021-2022学年高一上学期期中考试化学试题(已下线)考点巩固卷03 金属及其化合物(4大考点48题)-2024年高考化学一轮复习考点通关卷(新高考通用)12-2023新东方高二上期中考化学12
5 . 下列各组物质反应后,向产物中加入硫氰化钾溶液不会变红色的是
| A.铁与硫酸铜溶液反应 | B.铁在氯气中点燃 |
C.敞口露置的 溶液 溶液 | D.将铁锈溶解在稀盐酸中 |
您最近一年使用:0次
21-22高一·全国·单元测试
解题方法
6 . 电子工业常用FeCl3溶液腐蚀绝缘板上的铜箔,制造印刷电路板。从腐蚀废液(主要含FeCl3、FeCl2、CuCl2)中回收铜,并重新获得FeCl3溶液。废液处理流程如图:

(1)步骤(Ⅰ)中涉及反应的离子方程式:__ ;__ 。
(2)沉淀B中主要含有__ ,气体D是__ 。
(3)写出步骤(Ⅲ)中生成FeCl3的化学方程式__ 。
(4)步骤(Ⅲ)中,将氯气换成H2O2也能达到同样的目的,写出H2O2将Fe2+氧化为Fe3+的离子方程式:__ 。
(5)取FeCl3溶液加入少量KI溶液混合,再滴加淀粉溶液,溶液变蓝。该氧化还原反应的离子方程式为__ 。

(1)步骤(Ⅰ)中涉及反应的离子方程式:
(2)沉淀B中主要含有
(3)写出步骤(Ⅲ)中生成FeCl3的化学方程式
(4)步骤(Ⅲ)中,将氯气换成H2O2也能达到同样的目的,写出H2O2将Fe2+氧化为Fe3+的离子方程式:
(5)取FeCl3溶液加入少量KI溶液混合,再滴加淀粉溶液,溶液变蓝。该氧化还原反应的离子方程式为
您最近一年使用:0次
名校
解题方法
7 . 下列各组物质中,所加除杂试剂正确的是
| 主体物质 | 杂质 | 除杂试剂 | |
| A | FeCl2溶液 | FeCl3 | Cl2 |
| B | FeCl3溶液 | CuCl2 | Fe |
| C | NaHCO3溶液 | Na2CO3 | CO2 |
| D | FeSO4溶液 | Fe2(SO4)3 | Cu |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2021-12-27更新
|
1297次组卷
|
5卷引用:第三章 铁 金属材料
名校
解题方法
8 . 向含有一定物质的量的 和
和 的混合溶液中逐渐加入
的混合溶液中逐渐加入 粉至过量,该溶液的质量随加入铁粉的质量的变化关系图为
粉至过量,该溶液的质量随加入铁粉的质量的变化关系图为
 和
和 的混合溶液中逐渐加入
的混合溶液中逐渐加入 粉至过量,该溶液的质量随加入铁粉的质量的变化关系图为
粉至过量,该溶液的质量随加入铁粉的质量的变化关系图为A.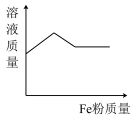 | B.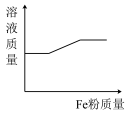 |
C.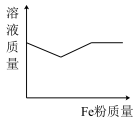 | D.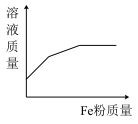 |
您最近一年使用:0次
2021-12-19更新
|
1258次组卷
|
14卷引用:第三章 铁 金属材料
第三章 铁 金属材料辽宁省辽阳市2021-2022学年高一上学期期末考试化学试题湖北省十堰市2021-2022学年高一上学期期末调研考试化学试题浙江省舟山市舟山中学2021-2022学年高一下学期开学考试化学试题湖南省部分校2021-2022学年高一上学期12月联考化学试题河南省洛阳市创新发展联盟2021-2022学年高一上学期第二次联考化学试题天津市耀华中学2022-2023学年高一上学期期末考试化学试题天津市耀华中学2022-2023学年高一上学期期末考试化学试题湖北省荆州市监利市2022-2023学年高一下学期2月调考化学试题浙江省瑞安市瑞祥高级中学2022-2023学年高一上学期期末考试化学试题山西省大同市第一中学校2023-2024学年高一上学期12月月考化学试题陕西省西安市阎良区关山中学2023-2024学年高一上学期第三次质量检测化学试题浙江省金华市曙光学校2023-2024学年高一上学期12月月考化学试题广西柳州高级中学2023-2024学年高一上学期寒假月考四化学试题
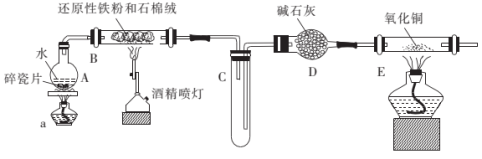
9 . 某校化学小组学生利用如图所示装置进行“铁与水蒸气反应”的实验,并对产物组成进行探究(图中夹持及尾气处理装置均已略去)。请回答下列问题:__ 。
(2)硬质玻璃管B中发生反应的化学方程式为__ 。
(3)实验中先点燃酒精灯a再点燃酒精喷灯,可能的原因是__ 。
(4)装置E中的现象是__ 。
(5)利用反应后的固体物质进行如图实验:___ 。
②该同学将上述实验中的新制氯水改为H2O2溶液,也能出现深红色溶液,用离子方程式表示溶液颜色加深的原因:__ 。
③电子工业中,人们常用FeCl3溶液腐蚀铜板来制作印刷电路板,请写出FeCl3溶液与铜反应的离子方程式:__ 。
(2)硬质玻璃管B中发生反应的化学方程式为
(3)实验中先点燃酒精灯a再点燃酒精喷灯,可能的原因是
(4)装置E中的现象是
(5)利用反应后的固体物质进行如图实验:
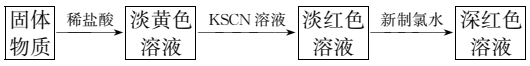
②该同学将上述实验中的新制氯水改为H2O2溶液,也能出现深红色溶液,用离子方程式表示溶液颜色加深的原因:
③电子工业中,人们常用FeCl3溶液腐蚀铜板来制作印刷电路板,请写出FeCl3溶液与铜反应的离子方程式:
您最近一年使用:0次
名校
解题方法
10 . 铁器时代是人类发展史中一个极为重要的时代,铁及其化合物在人类的生产、生活中都起了巨大的作用。
(1)有“中华第一剑”之称的虢国玉柄铁剑是我国目前出土的最早冶炼铁,玉柄铁剑,剑断锈连,剑身表面的铁锈的主要成分是___ (填标号)。
(2)长期放置的FeSO4溶液易被氧化而变质,实验室用绿矾FeSO4·xH2O配制FeSO4溶液时为了防止FeSO4溶液变质,经常向其中加入铁粉,其原因是___ (用离子方程式表示)。
(3)利用部分变质的FeSO4溶液制备Fe2O3:
部分变质的FeSO4溶液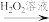 溶液I
溶液I 沉淀II
沉淀II Fe2O3
Fe2O3
①H2O2溶液的作用是___ 。
②“溶液I”的溶质为___ (填化学式),写出由“溶液I”到“沉淀II”反应的离子方程式:___ 。
③“操作III”的名称为___ 。
(4)为测定某绿矾FeSO4·xH2O中结晶水的含量,将石英玻璃管(带两端开关K1和K2)(设为装置A)称重,记为m1g。将该绿矾FeSO4·xH2O样品装入石英玻璃管中,再次将装置A称重,记为m2g。按图示连接好装置进行实验。

①将下列实验操作步骤正确排序:__ (填标号);重复上述操作步骤,直至装置A恒重,记为m3g。
a.点燃酒精灯,加热
b.熄灭酒精灯
c.关闭K1和K2
d.打开K1和K2,缓缓通入N2
e.称量装置A
f.冷却至室温
②根据实验记录,计算绿矾FeSO4·xH2O化学式中结晶水的数目x=___ (列出计算式即可)。
(1)有“中华第一剑”之称的虢国玉柄铁剑是我国目前出土的最早冶炼铁,玉柄铁剑,剑断锈连,剑身表面的铁锈的主要成分是
| A.Fe | B.FeO | C.Fe3O4 | D.Fe2O3 |
(3)利用部分变质的FeSO4溶液制备Fe2O3:
部分变质的FeSO4溶液
 溶液I
溶液I 沉淀II
沉淀II Fe2O3
Fe2O3①H2O2溶液的作用是
②“溶液I”的溶质为
③“操作III”的名称为
(4)为测定某绿矾FeSO4·xH2O中结晶水的含量,将石英玻璃管(带两端开关K1和K2)(设为装置A)称重,记为m1g。将该绿矾FeSO4·xH2O样品装入石英玻璃管中,再次将装置A称重,记为m2g。按图示连接好装置进行实验。

①将下列实验操作步骤正确排序:
a.点燃酒精灯,加热
b.熄灭酒精灯
c.关闭K1和K2
d.打开K1和K2,缓缓通入N2
e.称量装置A
f.冷却至室温
②根据实验记录,计算绿矾FeSO4·xH2O化学式中结晶水的数目x=
您最近一年使用:0次
2021-12-17更新
|
564次组卷
|
4卷引用:第三章 铁 金属材料(B卷)-2021-2022学年高一化学优选好题单元专题双测卷(人教版2019必修第一册)
(已下线)第三章 铁 金属材料(B卷)-2021-2022学年高一化学优选好题单元专题双测卷(人教版2019必修第一册)河北省保定市唐县第一中学2022-2023学年高一上学期第三次考试化学试题河北省定州市第二中学2022-2023学年高一上学期12月月考化学试题河北省百所学校大联考2021-2022学年高一12月联考化学试题



