解题方法
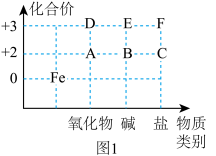
1 . 从化合价和物质类别两个视角认识元素及其化合物性质是重要的化学学习方式。图1是Fe及其化合物的化合价—物质类别二维图。回答下列问题:
2.若图1中的F为硫酸盐,请写出由物质D转化为物质F的离子方程式:___________ 。
3.图1中的B在潮湿的空气中很容易发生化合反应变成E,该反应的化学方程式为___________ 。
4.图1中的F与C在水溶液中转化的离子反应有: ,为了探究该反应存在一定的限度,某化学兴趣小组取
,为了探究该反应存在一定的限度,某化学兴趣小组取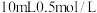 的
的 溶液于试管中,再加入
溶液于试管中,再加入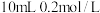 的
的 溶液,振荡,使试管中的物质充分反应一段时间。为了达到实验目的,则还需要再向试管中加入的下列试剂为 。
溶液,振荡,使试管中的物质充分反应一段时间。为了达到实验目的,则还需要再向试管中加入的下列试剂为 。
| A.电解法 | B.还原法 | C.热分解法 | D.物理方法 |
3.图1中的B在潮湿的空气中很容易发生化合反应变成E,该反应的化学方程式为
4.图1中的F与C在水溶液中转化的离子反应有:
 ,为了探究该反应存在一定的限度,某化学兴趣小组取
,为了探究该反应存在一定的限度,某化学兴趣小组取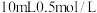 的
的 溶液于试管中,再加入
溶液于试管中,再加入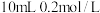 的
的 溶液,振荡,使试管中的物质充分反应一段时间。为了达到实验目的,则还需要再向试管中加入的下列试剂为 。
溶液,振荡,使试管中的物质充分反应一段时间。为了达到实验目的,则还需要再向试管中加入的下列试剂为 。| A.淀粉溶液 | B. 溶液 溶液 | C. | D.酸性高锰酸钾溶液 |
您最近一年使用:0次
解题方法
2 .  与
与 的反应常用来检验
的反应常用来检验 的存在:
的存在: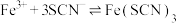 。若溶液中含有
。若溶液中含有 ,则加入
,则加入 溶液后的现象为
溶液后的现象为_______ ,向加入 后的混合溶液中再加入少量
后的混合溶液中再加入少量 固体,观察到的现象是
固体,观察到的现象是_______ ,产生该现象的原因是_______ 。
 与
与 的反应常用来检验
的反应常用来检验 的存在:
的存在: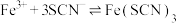 。若溶液中含有
。若溶液中含有 ,则加入
,则加入 溶液后的现象为
溶液后的现象为 后的混合溶液中再加入少量
后的混合溶液中再加入少量 固体,观察到的现象是
固体,观察到的现象是
您最近一年使用:0次
3 . 铁在人体中以 和
和 的形式存在。二价铁离子易被吸收,给贫血者补充铁时,应给予含二价铁离子的铁盐,如硫酸亚铁(
的形式存在。二价铁离子易被吸收,给贫血者补充铁时,应给予含二价铁离子的铁盐,如硫酸亚铁( )。某工厂的酸性废水中主要含有
)。某工厂的酸性废水中主要含有 、
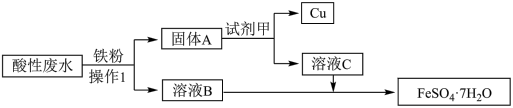
、 等离子,为了减少污染并变废为宝,工程师们设计了如下流程,回收铜和绿矾(
等离子,为了减少污染并变废为宝,工程师们设计了如下流程,回收铜和绿矾( )。
)。___________ →___________ →___________ (填离子符号)
(2)操作Ⅰ是___________ ,试剂甲是___________ ,获得的 需密闭保存,原因是
需密闭保存,原因是___________ 。
(3)检验溶液B中 是否除尽的实验方法是:
是否除尽的实验方法是:___________ 。
(4)在过量 溶液中滴加稀硫酸,再滴入几滴氯水,溶液立即变黄。上述反应的离子方程式为
溶液中滴加稀硫酸,再滴入几滴氯水,溶液立即变黄。上述反应的离子方程式为___________ 。
(5)向 溶液滴加NaOH溶液,会观察到的现象为
溶液滴加NaOH溶液,会观察到的现象为___________ 。
 和
和 的形式存在。二价铁离子易被吸收,给贫血者补充铁时,应给予含二价铁离子的铁盐,如硫酸亚铁(
的形式存在。二价铁离子易被吸收,给贫血者补充铁时,应给予含二价铁离子的铁盐,如硫酸亚铁( )。某工厂的酸性废水中主要含有
)。某工厂的酸性废水中主要含有 、
、 等离子,为了减少污染并变废为宝,工程师们设计了如下流程,回收铜和绿矾(
等离子,为了减少污染并变废为宝,工程师们设计了如下流程,回收铜和绿矾( )。
)。
(2)操作Ⅰ是
 需密闭保存,原因是
需密闭保存,原因是(3)检验溶液B中
 是否除尽的实验方法是:
是否除尽的实验方法是:(4)在过量
 溶液中滴加稀硫酸,再滴入几滴氯水,溶液立即变黄。上述反应的离子方程式为
溶液中滴加稀硫酸,再滴入几滴氯水,溶液立即变黄。上述反应的离子方程式为(5)向
 溶液滴加NaOH溶液,会观察到的现象为
溶液滴加NaOH溶液,会观察到的现象为
您最近一年使用:0次
解题方法
4 . 下列各组离子在溶液中能大量共存的是
A. 、 、 、 、 、 、 | B. 、 、 、 、 、 、 |
C. 、 、 、 、 、 、 | D. 、 、 、 、 、 、 |
您最近一年使用:0次
5 . Ⅰ.铁是人体必需元素,市场上常见补血剂有硫酸亚铁、葡萄糖酸亚铁、琥珀酸亚铁(速力菲片)等。某化学兴趣小组通过下列实验探究久置FeSO4补血剂是否变质并测定其中铁元素的含量。
(已知KSCN可被氧化剂氧化)___________ 。
(2)步骤④中最后一步反应的化学反应方程式为___________ 。
(3)可检验Fe(SO4)3中是否含有FeSO4的试剂是___________ 。
Ⅱ.高效净水剂聚合氯化铝铁(PAFC)的组成可表示为 ,其中A1、Fe元素均为+3价。某、工厂欲以工业废料(铁、铁和铝的氧化物)为原料制取PAFC,设计如下流程:
,其中A1、Fe元素均为+3价。某、工厂欲以工业废料(铁、铁和铝的氧化物)为原料制取PAFC,设计如下流程:___________ (填元素符号);不能确定的原因是
___________ (用离子方程式表示);为证明该离子确实存在,可采用的操作是___________ (指明所用试剂及观察到的现象)。
(5)调节pH的目的是___________ 。
(6)根据下列实验结果,求出氯化铝铁的化学式。
步骤①,取22.2g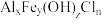 样品,加入足量硝酸溶解后,再加入AgNO3溶液至不再有沉淀生成,过滤,洗涤,干燥后,称得固体质量为28.7g。
样品,加入足量硝酸溶解后,再加入AgNO3溶液至不再有沉淀生成,过滤,洗涤,干燥后,称得固体质量为28.7g。
步骤②:将步骤①中滤液与洗涤液混合,加入过量NaOH溶液,过滤,洗涤,干燥后,称得固体质量为10.7g。
氯化铝铁的化学式为___________ 。
(已知KSCN可被氧化剂氧化)
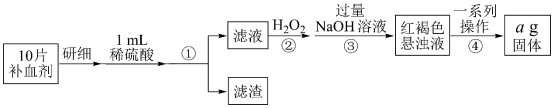
(2)步骤④中最后一步反应的化学反应方程式为
(3)可检验Fe(SO4)3中是否含有FeSO4的试剂是
Ⅱ.高效净水剂聚合氯化铝铁(PAFC)的组成可表示为
 ,其中A1、Fe元素均为+3价。某、工厂欲以工业废料(铁、铁和铝的氧化物)为原料制取PAFC,设计如下流程:
,其中A1、Fe元素均为+3价。某、工厂欲以工业废料(铁、铁和铝的氧化物)为原料制取PAFC,设计如下流程: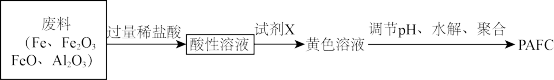
(5)调节pH的目的是
(6)根据下列实验结果,求出氯化铝铁的化学式。
步骤①,取22.2g
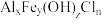 样品,加入足量硝酸溶解后,再加入AgNO3溶液至不再有沉淀生成,过滤,洗涤,干燥后,称得固体质量为28.7g。
样品,加入足量硝酸溶解后,再加入AgNO3溶液至不再有沉淀生成,过滤,洗涤,干燥后,称得固体质量为28.7g。步骤②:将步骤①中滤液与洗涤液混合,加入过量NaOH溶液,过滤,洗涤,干燥后,称得固体质量为10.7g。
氯化铝铁的化学式为
您最近一年使用:0次
解题方法
6 . 在一定条件下,铁及其化合物具有如图所示的转化关系。丙为白色固体,其悬浊液在空气中会迅速变为灰绿色,最终变为红褐色。请回答下列问题:
(1)根据分析可知丙为___________ (填化学式);甲可能是___________ (填字母),乙可能是___________ 。(填字母)
A.稀硝酸 B. 溶液 C.
溶液 C. D.
D. 溶液
溶液
(2)工业上高炉炼铁可以实现③的转化,所得到的炽热的铁水注入模具之前,模具必须进行充分的干燥处理,原因是___________ (填化学方程式)。
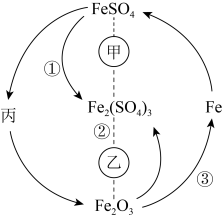
(1)根据分析可知丙为
A.稀硝酸 B.
 溶液 C.
溶液 C. D.
D. 溶液
溶液(2)工业上高炉炼铁可以实现③的转化,所得到的炽热的铁水注入模具之前,模具必须进行充分的干燥处理,原因是
您最近一年使用:0次
解题方法
7 . 实验小组发现新配制的 溶液放置一段时间,由浅绿色溶液变为黄色浊液A,进行如下探究。
溶液放置一段时间,由浅绿色溶液变为黄色浊液A,进行如下探究。
资料:i.胶体可以透过滤纸。
ii. 与
与 溶液反应,生成蓝色沉淀
溶液反应,生成蓝色沉淀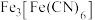 。
。
(1)探究A中的成分,进行如下实验。
取少量A,过滤得到红褐色沉淀和黄色透明液体B。
取少量B于试管中,加入 溶液,有蓝色沉淀。
溶液,有蓝色沉淀。
取少量B于试管中,加入_______ (填试剂),液体变为红色。
用激光笔照射B,看到一条光亮的“通路”。
综合上述实验,说明A中铁元素的存在形态有 、
、 、
、_______ 和_______ 。
进一步探究B显黄色的原因。_______ (用离子方程式表示)。
(3)由上述实验得出:B显黄色的主要原因不是因为含有 ,而是因为含有
,而是因为含有_______ ,理由是:_______ 。
测定A的变质程度并分析对后续实验的影响。
(4)取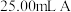 ,加入足量稀硫酸,可与
,加入足量稀硫酸,可与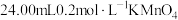 溶液恰好完全反应。已知
溶液恰好完全反应。已知 在酸性环境下被还原为
在酸性环境下被还原为 ,A中
,A中 的浓度为
的浓度为_______  ,说明其主要成分仍然是
,说明其主要成分仍然是 。
。
(5)下列实验可以使用A进行的是_______ (填字母)。
a.向A中滴入NaOH溶液,制备纯净的 沉淀
沉淀
b.用A处理含有+6价Cr的酸性废水,将剧毒的+6价Cr还原至低毒的+3价
 溶液放置一段时间,由浅绿色溶液变为黄色浊液A,进行如下探究。
溶液放置一段时间,由浅绿色溶液变为黄色浊液A,进行如下探究。资料:i.胶体可以透过滤纸。
ii.
 与
与 溶液反应,生成蓝色沉淀
溶液反应,生成蓝色沉淀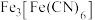 。
。(1)探究A中的成分,进行如下实验。
取少量A,过滤得到红褐色沉淀和黄色透明液体B。
取少量B于试管中,加入
 溶液,有蓝色沉淀。
溶液,有蓝色沉淀。取少量B于试管中,加入
用激光笔照射B,看到一条光亮的“通路”。
综合上述实验,说明A中铁元素的存在形态有
 、
、 、
、进一步探究B显黄色的原因。
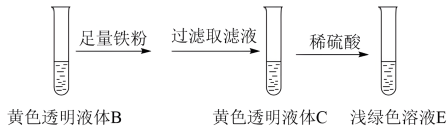
(3)由上述实验得出:B显黄色的主要原因不是因为含有
 ,而是因为含有
,而是因为含有测定A的变质程度并分析对后续实验的影响。
(4)取
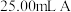 ,加入足量稀硫酸,可与
,加入足量稀硫酸,可与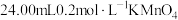 溶液恰好完全反应。已知
溶液恰好完全反应。已知 在酸性环境下被还原为
在酸性环境下被还原为 ,A中
,A中 的浓度为
的浓度为 ,说明其主要成分仍然是
,说明其主要成分仍然是 。
。(5)下列实验可以使用A进行的是
a.向A中滴入NaOH溶液,制备纯净的
 沉淀
沉淀b.用A处理含有+6价Cr的酸性废水,将剧毒的+6价Cr还原至低毒的+3价
您最近一年使用:0次
名校
解题方法
8 . 铁黑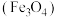 是一种颜料。工业利用硫酸亚铁
是一种颜料。工业利用硫酸亚铁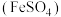 ,以及氨水、空气等,经过下列反应来制备铁黑。
,以及氨水、空气等,经过下列反应来制备铁黑。
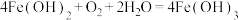
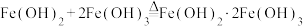

(1)硫酸亚铁溶液中混有少量 杂质,除杂的操作是:
杂质,除杂的操作是:___________ 。
(2)过滤和干燥之间一般还需要___________ 操作,否则制备的铁黑质量___________ (偏高、偏低、不影响)。
(3)若制备1吨铁黑,需通入标准状况下___________ 立方米的空气(氧气体积分数按20%计,保留1位小数)。
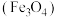 是一种颜料。工业利用硫酸亚铁
是一种颜料。工业利用硫酸亚铁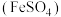 ,以及氨水、空气等,经过下列反应来制备铁黑。
,以及氨水、空气等,经过下列反应来制备铁黑。
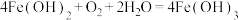
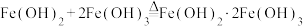

(1)硫酸亚铁溶液中混有少量
 杂质,除杂的操作是:
杂质,除杂的操作是:(2)过滤和干燥之间一般还需要
(3)若制备1吨铁黑,需通入标准状况下
您最近一年使用:0次
名校
解题方法
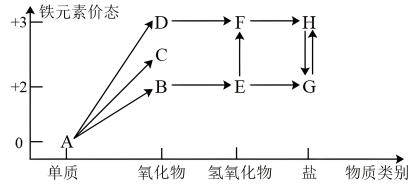
9 . 铁是人类较早使用的金属之一,下图为铁元素的价类二维图,其中的箭头表示部分物质间的转化关系。运用铁及其化合物的知识,回答下列问题。___________ ;E→F反应的化学方程式是___________ ,该反应过程的现象为___________ 。
(2)电子工业需要用30%的 溶液腐蚀敷在绝缘板上的铜,制造印刷电路,请写出
溶液腐蚀敷在绝缘板上的铜,制造印刷电路,请写出 溶液与铜反应的离子方程式:
溶液与铜反应的离子方程式:___________ 。
(3)城市饮用水处理新技术用 、高铁酸钠代替
、高铁酸钠代替 ,如果以单位质量的氧化剂所得到的电子数来表示消毒效率,那么
,如果以单位质量的氧化剂所得到的电子数来表示消毒效率,那么 、
、 、
、 的消毒效率由大到小的顺序是
的消毒效率由大到小的顺序是___________ 。
(2)电子工业需要用30%的
 溶液腐蚀敷在绝缘板上的铜,制造印刷电路,请写出
溶液腐蚀敷在绝缘板上的铜,制造印刷电路,请写出 溶液与铜反应的离子方程式:
溶液与铜反应的离子方程式:(3)城市饮用水处理新技术用
 、高铁酸钠代替
、高铁酸钠代替 ,如果以单位质量的氧化剂所得到的电子数来表示消毒效率,那么
,如果以单位质量的氧化剂所得到的电子数来表示消毒效率,那么 、
、 、
、 的消毒效率由大到小的顺序是
的消毒效率由大到小的顺序是
您最近一年使用:0次
10 . I.“铁与水反应”的实验,并检验产物的性质:
(1)写出“铁与水反应”反应的化学方程式为_______ 。
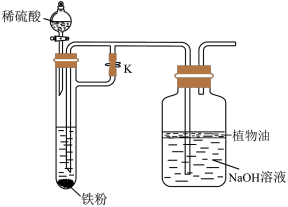
Ⅱ.制备氢氧化亚铁:设计如下实验能较长时间观察到白色Fe(OH)2沉淀,选用稀硫酸、铁粉、NaOH溶液进行实验,装置如图。_______ 。
(3)实验时,先_______ (填“打开”或“关闭”)止水夹K,然后打开分液漏斗的玻璃塞和活塞,使稀硫酸与铁粉反应,一段时间后,_______ (填“打开”或“关闭”)止水夹K,制得白色Fe(OH)2沉淀,且沉淀能持续一段时间不变色。
Ⅲ.探究FeCl2溶液、FeCl3溶液的性质
(4)从物质类别角度判断FeCl2属于_______ ,因此可以与某些碱反应。
(5)预测FeCl2具有氧化性,因此可以与Zn反应,此时Zn体现_______ 性。
(6)预测FeCl2具有还原性,预测依据是_______ ,因此可以与酸性KMnO4溶液反应。
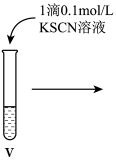
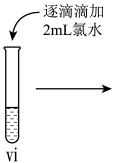
(7)进行如下实验操作:
①i中的现象是_______ ,用化学方程式表示产生该现象的原因:_______ 、_______ 。
②ⅱ中反应的离子方程式是_______ 。
③ⅲ中的现象是_______ 。
④ⅳ中反应的离子方程式是_______ 。小组同学探究ⅵ中褪色原因,提出两种假设:a.铁离子被转化,b.SCN-被转化。分别向褪色后的溶液中滴加0.1mol/LFeCl3溶液和KSCN溶液各1滴,观察到_______ 现象,得出结论:假设b成立。
(1)写出“铁与水反应”反应的化学方程式为
Ⅱ.制备氢氧化亚铁:设计如下实验能较长时间观察到白色Fe(OH)2沉淀,选用稀硫酸、铁粉、NaOH溶液进行实验,装置如图。
(3)实验时,先
Ⅲ.探究FeCl2溶液、FeCl3溶液的性质
(4)从物质类别角度判断FeCl2属于
(5)预测FeCl2具有氧化性,因此可以与Zn反应,此时Zn体现
(6)预测FeCl2具有还原性,预测依据是
(7)进行如下实验操作:
| 序号 | 操作 | |
| ⅰ | 滴加NaOH溶液 | ||
| ⅱ | 加入少量锌粉 | ||
| ⅲ | 滴加酸性KMnO4溶液 | ||
| 操作 |
|
|
|
| 现象 | 溶液由棕黄色变为浅绿色 | 无明显现象 | 溶液变为红色,而后红色褪去 |
②ⅱ中反应的离子方程式是
③ⅲ中的现象是
④ⅳ中反应的离子方程式是
您最近一年使用:0次