名校
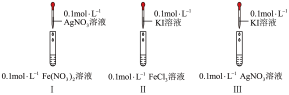
1 . 通过如下实验,比较 、
、 、
、 的氧化性。
的氧化性。
(1)实验室 溶液通常盛放在
溶液通常盛放在___________ 试剂瓶中。
(2)Ⅱ中反应的离子方程式为___________ 。
(3)I、Ⅱ中的现象说明___________。
(4)实验后,I试管壁上的黑色沉淀可用___________洗去。
(5)写出检验I中是否含有 的方法。
的方法。___________ 。
(6)检验Ⅱ中是否含有 不可选用:___________。(不定项)
不可选用:___________。(不定项)
(7)推测Ⅲ中未发生 氧化
氧化 的原因
的原因___________ 。
 、
、 、
、 的氧化性。
的氧化性。
| 实验现象 |
I中产生黑色沉淀,滴加 溶液,变红 溶液,变红 | |
| Ⅱ中溶液呈棕黄色,滴加淀粉溶液,变蓝 | |
| Ⅲ中产生黄色沉淀,滴加淀粉溶液,未变蓝 |
(1)实验室
 溶液通常盛放在
溶液通常盛放在(2)Ⅱ中反应的离子方程式为
(3)I、Ⅱ中的现象说明___________。
A.氧化性顺序: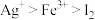 | B.氧化性顺序: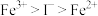 |
C.还原性顺序: | D.还原性顺序: |
(4)实验后,I试管壁上的黑色沉淀可用___________洗去。
| A.酒精 | B.二硫化碳 | C.浓硝酸 | D.热盐酸 |
(5)写出检验I中是否含有
 的方法。
的方法。(6)检验Ⅱ中是否含有
 不可选用:___________。(不定项)
不可选用:___________。(不定项)| A.氢氧化钠溶液 | B.酸性高辒酸钾溶液 | C.硫氰化钾溶液 | D.稀氨水 |
(7)推测Ⅲ中未发生
 氧化
氧化 的原因
的原因
您最近一年使用:0次
2 . 电子工业常用 左右的
左右的 溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板。为了从腐蚀废液中回收铜,并重新获得
溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板。为了从腐蚀废液中回收铜,并重新获得 溶液,某同学设计如图方案:
溶液,某同学设计如图方案: 的
的 溶液,需要的主要玻璃仪器除了量筒外还有
溶液,需要的主要玻璃仪器除了量筒外还有___________ 。
(2) 溶液与铜箔发生反应的离子方程式为
溶液与铜箔发生反应的离子方程式为___________ 。
(3)试剂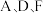 的化学式分别是
的化学式分别是___________ 、___________ 、___________ 。用 溶液制取
溶液制取 晶体的方法是
晶体的方法是___________ 。
A.蒸发结晶 B.降温结晶
 左右的
左右的 溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板。为了从腐蚀废液中回收铜,并重新获得
溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板。为了从腐蚀废液中回收铜,并重新获得 溶液,某同学设计如图方案:
溶液,某同学设计如图方案: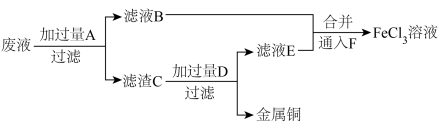
 的
的 溶液,需要的主要玻璃仪器除了量筒外还有
溶液,需要的主要玻璃仪器除了量筒外还有(2)
 溶液与铜箔发生反应的离子方程式为
溶液与铜箔发生反应的离子方程式为(3)试剂
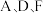 的化学式分别是
的化学式分别是 溶液制取
溶液制取 晶体的方法是
晶体的方法是A.蒸发结晶 B.降温结晶
您最近一年使用:0次
名校
解题方法
3 . 配制溶液:
称量→溶解→冷却→操作①→洗涤→注入→混匀→操作②→摇匀→装瓶贴标签
(1)操作①为___________ 、操作②为___________ 。
(2)用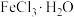 配制
配制 溶液时,应称量
溶液时,应称量___________ g固体(保留两位小数),需要的定量仪器为___________ 。
(3)配置溶液时,不慎掉入镀层缺损的镀铜小铁钉,写出可能发生的反应的离子方程式___________ 。
称量→溶解→冷却→操作①→洗涤→注入→混匀→操作②→摇匀→装瓶贴标签
(1)操作①为
(2)用
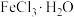 配制
配制 溶液时,应称量
溶液时,应称量(3)配置溶液时,不慎掉入镀层缺损的镀铜小铁钉,写出可能发生的反应的离子方程式
您最近一年使用:0次
名校
解题方法
4 . 电路板广泛用于计算机、手机等电子产品中。某兴趣小组拟制作带有“化学”标志的电路板并对废液进行回收利用。
I.制作电路板
小组同学取一小块覆铜板,用油性笔在铜板上写出“化学”标志,然后浸入 溶液中,一段时间后,取出覆铜板并用水洗净,获得带有图案的印刷电路板和废液(如图所示)。
溶液中,一段时间后,取出覆铜板并用水洗净,获得带有图案的印刷电路板和废液(如图所示)。_______ 。
(2)取少量废液于试管中,_______ (填操作和现象),则废液中含有 。
。
Ⅱ.回收废液
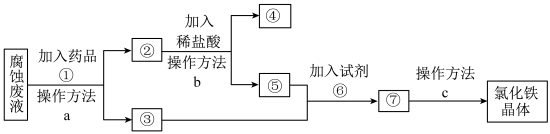
该组同学查阅资料:一种从腐蚀废液回收金属铜并获得氯化铁晶体的工艺流程如图。
(3)废液100mL,加入铁粉,其固体质量的变化如图所示,假设溶液体积不变,_______ 。
②原混合溶液中 的物质的量
的物质的量_______ 。
③ 点溶液中
点溶液中 的物质的量浓度
的物质的量浓度_______ 。
(4)操作方法 中是过滤的是
中是过滤的是_______ (填序号)。
(5)若取2mL溶液⑤加入试管中,然后滴加氢氧化钠溶液,产生白色沉淀,_______ (补全实验现象),此过程涉及氧化还原反应的化学方程式是:_______ 。
(6)试剂⑥是 时,发生反应的化学方程式是
时,发生反应的化学方程式是_______ 。
I.制作电路板
小组同学取一小块覆铜板,用油性笔在铜板上写出“化学”标志,然后浸入
 溶液中,一段时间后,取出覆铜板并用水洗净,获得带有图案的印刷电路板和废液(如图所示)。
溶液中,一段时间后,取出覆铜板并用水洗净,获得带有图案的印刷电路板和废液(如图所示)。
(2)取少量废液于试管中,
 。
。Ⅱ.回收废液
该组同学查阅资料:一种从腐蚀废液回收金属铜并获得氯化铁晶体的工艺流程如图。
(3)废液100mL,加入铁粉,其固体质量的变化如图所示,假设溶液体积不变,
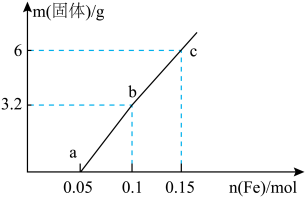
②原混合溶液中
 的物质的量
的物质的量③
 点溶液中
点溶液中 的物质的量浓度
的物质的量浓度(4)操作方法
 中是过滤的是
中是过滤的是(5)若取2mL溶液⑤加入试管中,然后滴加氢氧化钠溶液,产生白色沉淀,
(6)试剂⑥是
 时,发生反应的化学方程式是
时,发生反应的化学方程式是
您最近一年使用:0次
名校
解题方法
5 . 四氧化三铁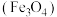 磁性纳米颗粒稳定、容易生产且用途广泛,是临床诊断、生物技术和环境化学领域多种潜在应用的有力工具。
磁性纳米颗粒稳定、容易生产且用途广泛,是临床诊断、生物技术和环境化学领域多种潜在应用的有力工具。
(1)中国科学院上海硅酸盐研究所研制出“纳米药物分子运输车”,该“运输车”可提高肿瘤的治疗效果,其结构如图所示。下列有关说法正确的是___________。
(2)① 能和稀硫酸反应,写出反应的离子方程式
能和稀硫酸反应,写出反应的离子方程式___________ 。
②验证反应后溶液中含有 的最恰当的试剂是
的最恰当的试剂是___________ 。
A.氯水 B.酸性高锰酸钾溶液 C.硫氰化钾溶液 D. 溶液
溶液
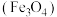 磁性纳米颗粒稳定、容易生产且用途广泛,是临床诊断、生物技术和环境化学领域多种潜在应用的有力工具。
磁性纳米颗粒稳定、容易生产且用途广泛,是临床诊断、生物技术和环境化学领域多种潜在应用的有力工具。(1)中国科学院上海硅酸盐研究所研制出“纳米药物分子运输车”,该“运输车”可提高肿瘤的治疗效果,其结构如图所示。下列有关说法正确的是___________。

| A.该“运输车”中四氧化三铁和二氧化硅都属于氧化物 |
| B.四氧化三铁起到“磁性导航仪”的作用 |
| C.该“运输车”属于混合物 |
| D.该“运输车”分散于水中所得的分散系属于胶体 |
 能和稀硫酸反应,写出反应的离子方程式
能和稀硫酸反应,写出反应的离子方程式②验证反应后溶液中含有
 的最恰当的试剂是
的最恰当的试剂是A.氯水 B.酸性高锰酸钾溶液 C.硫氰化钾溶液 D.
 溶液
溶液
您最近一年使用:0次
名校
解题方法
6 . 以废铁屑(含少量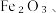 FeS等杂质)为原料,制备硫酸亚铁晶体
FeS等杂质)为原料,制备硫酸亚铁晶体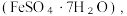 流程示意图如下:
流程示意图如下: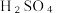 的作用是
的作用是
_________ (用离子方程式表示)。过程中产生的有毒气体,可用___________ 溶液吸收。
(2)酸浸时间对所得溶液的成分影响如下表所示。
用文字说明导致上述颜色变化的可能原因。___________
(3)已知: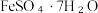 受热易失水,则操作X为:蒸发浓缩、
受热易失水,则操作X为:蒸发浓缩、________ 、过滤、洗涤。FeSO4强热后继续分解,推测产物为___________ 、Fe2O3和SO3。
测定所得硫酸亚铁晶体中的含量,步骤如下:
Ⅰ.称取ag硫酸亚铁晶体样品,配制成100mL溶液。
Ⅱ.取出10mL溶液,加入适量稀硫酸,滴入 的
的 溶液,至反应完全,共消耗
溶液,至反应完全,共消耗 溶液cmL。(反应原理:
溶液cmL。(反应原理:
(4)计算硫酸亚铁晶体样品中 质量分数
质量分数___________ 。
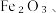 FeS等杂质)为原料,制备硫酸亚铁晶体
FeS等杂质)为原料,制备硫酸亚铁晶体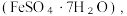 流程示意图如下:
流程示意图如下:
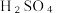 的作用是
的作用是
(2)酸浸时间对所得溶液的成分影响如下表所示。
| 酸浸时间 | 1min | 30min | 120min |
| 用KSCN溶液检验 | 变红 | 未变红 | 变红 |
(3)已知:
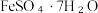 受热易失水,则操作X为:蒸发浓缩、
受热易失水,则操作X为:蒸发浓缩、测定所得硫酸亚铁晶体中的含量,步骤如下:
Ⅰ.称取ag硫酸亚铁晶体样品,配制成100mL溶液。
Ⅱ.取出10mL溶液,加入适量稀硫酸,滴入
 的
的 溶液,至反应完全,共消耗
溶液,至反应完全,共消耗 溶液cmL。(反应原理:
溶液cmL。(反应原理:
(4)计算硫酸亚铁晶体样品中
 质量分数
质量分数
您最近一年使用:0次
名校
解题方法
7 . 向含有Fe3+、Fe2+、Cu2+的蚀刻铜箔回收液中,加入一定量铁粉,反应一段时间后,对反应后的混合物进行分析,下列说法错误的是
| A.若有固体剩余,则该固体一定含有Cu |
| B.若有固体剩余,则该溶液可能含有Cu2+ |
| C.若无固体剩余,则该溶液不可能含有Fe3+ |
| D.无论固体是否剩余,该溶液中一定含有Fe2+ |
您最近一年使用:0次
名校
解题方法
8 . 将铝与氧化铁混合制备单质铁的反应称为铝热反应,反应装置如图所示:_____ 。
(2)该铝热反应的化学方程式为_____ ,引发铝热反应的实验操作是_____ 。
(3)取少量反应所得的固体混合物,将其溶于足量稀 ,滴加KSCN溶液无明显现象,能否说明固体混合物中已无
,滴加KSCN溶液无明显现象,能否说明固体混合物中已无 ,请判断并说明理由
,请判断并说明理由_____ 。
(4)写出一种铝热反应的实际应用_____ 。
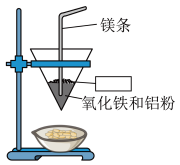
(2)该铝热反应的化学方程式为
(3)取少量反应所得的固体混合物,将其溶于足量稀
 ,滴加KSCN溶液无明显现象,能否说明固体混合物中已无
,滴加KSCN溶液无明显现象,能否说明固体混合物中已无 ,请判断并说明理由
,请判断并说明理由(4)写出一种铝热反应的实际应用
您最近一年使用:0次
名校
解题方法
9 .  溶液在工业上用于蚀刻铜箔电路板。从蚀刻后的废液中可回收铜并使蚀刻液再生,流程如图所示:
溶液在工业上用于蚀刻铜箔电路板。从蚀刻后的废液中可回收铜并使蚀刻液再生,流程如图所示: 溶液蚀刻铜箔的反应的离子方程式
溶液蚀刻铜箔的反应的离子方程式_____ 。
(2)从固体中分离出铜,试剂X是_____ 。
(3)若要使滤液再生为蚀刻液,可加入_____ 。
 溶液在工业上用于蚀刻铜箔电路板。从蚀刻后的废液中可回收铜并使蚀刻液再生,流程如图所示:
溶液在工业上用于蚀刻铜箔电路板。从蚀刻后的废液中可回收铜并使蚀刻液再生,流程如图所示: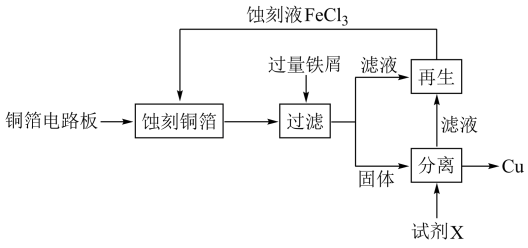
 溶液蚀刻铜箔的反应的离子方程式
溶液蚀刻铜箔的反应的离子方程式(2)从固体中分离出铜,试剂X是
(3)若要使滤液再生为蚀刻液,可加入
您最近一年使用:0次
名校
10 . 二氧化钛是一种常用的金属氧化物。工业上常用钛铁矿(主要成分为 ,其中Ti元素的化合价为
,其中Ti元素的化合价为 )来提取
)来提取 ,其中通常混有一定量的赤铁矿(主要成分为
,其中通常混有一定量的赤铁矿(主要成分为 ),该工艺流程如下:
),该工艺流程如下:

(1)结合流程,判断下列关于 的说法,错误的是_______。
的说法,错误的是_______。
(2)关于铁及其合金的性质,下列说法错误的是_______。
(3)将上述实验中得到的 溶于水,取2mL该溶液于试管中,向其中滴加几滴NaOH溶液。
溶于水,取2mL该溶液于试管中,向其中滴加几滴NaOH溶液。
①看到的现象是_______ ,写出相应的化学方程式_______ 、_______ 。
②再向上述试管中滴加足量的稀硝酸中,下列说法正确的是_______ 。
A.仅发生复分解反应
B.原试管中的沉淀可能同时含有 和
和
C.最后溶液中的盐仅有
(4)检验 中不含
中不含 的方法是
的方法是_______ ,现象是_______ 。
(5)根据②处的反应可知 的氧化性比
的氧化性比 的氧化性强,理由是
的氧化性强,理由是_______ 。
(6)经检测,某次使用的混合矿石中约含有质量分数50%的 ,40%的
,40%的 ,其它杂质中不含铁元素。若使用1吨该矿石冶炼
,其它杂质中不含铁元素。若使用1吨该矿石冶炼 ,能得到
,能得到
_______ 吨,同时得到副产物
_______ 吨(不考虑生产过程中的损失,均保留两位小数)。
 ,其中Ti元素的化合价为
,其中Ti元素的化合价为 )来提取
)来提取 ,其中通常混有一定量的赤铁矿(主要成分为
,其中通常混有一定量的赤铁矿(主要成分为 ),该工艺流程如下:
),该工艺流程如下:
(1)结合流程,判断下列关于
 的说法,错误的是_______。
的说法,错误的是_______。A. 发生复分解反应生成 发生复分解反应生成 |
B.煅烧 时,发生还原反应生成 时,发生还原反应生成 |
| C.流程中“结晶”的具体步骤是:加热浓缩、冷却结晶 |
D.保存 溶液时需要加铁粉 溶液时需要加铁粉 |
(2)关于铁及其合金的性质,下列说法错误的是_______。
| A.在元素周期表中,铁属于过渡元素 |
| B.生铁和钢的性质差异主要是碳含量的不同 |
| C.铁和不同非金属单质反应产物中的铁元素价态可能不同 |
| D.铁在氧气中燃烧后,可以使用磁铁验证是否有铁单质剩余 |
(3)将上述实验中得到的
 溶于水,取2mL该溶液于试管中,向其中滴加几滴NaOH溶液。
溶于水,取2mL该溶液于试管中,向其中滴加几滴NaOH溶液。①看到的现象是
②再向上述试管中滴加足量的稀硝酸中,下列说法正确的是
A.仅发生复分解反应
B.原试管中的沉淀可能同时含有
 和
和
C.最后溶液中的盐仅有

(4)检验
 中不含
中不含 的方法是
的方法是(5)根据②处的反应可知
 的氧化性比
的氧化性比 的氧化性强,理由是
的氧化性强,理由是(6)经检测,某次使用的混合矿石中约含有质量分数50%的
 ,40%的
,40%的 ,其它杂质中不含铁元素。若使用1吨该矿石冶炼
,其它杂质中不含铁元素。若使用1吨该矿石冶炼 ,能得到
,能得到

您最近一年使用:0次