名校
1 . 某校化学小组学生利用如图所示装置进行“铁与水反应”的实验,并利用产物进一步制取 晶体(图中夹持及尾气处理装置均已略去)。
晶体(图中夹持及尾气处理装置均已略去)。
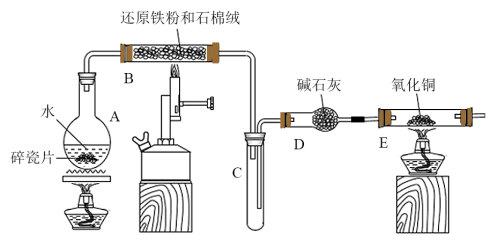
(1)装置A中碎瓷片的作用是___________ ;装置B中发生反应的化学方程式是___________ 。
(2)停止反应,待B管冷却后,取其中的固体,加入过量稀盐酸充分反应,过滤。简述检验滤液中 的方法。
的方法。___________
(3)该小组学生利用上述滤液制取 晶体,设计流程如下:
晶体,设计流程如下:

①步骤I中加入的试剂可以是___________ 。
a.酸性 溶液 b.铁粉 c.稀
溶液 b.铁粉 c.稀 d.
d. 溶液
溶液
②步骤Ⅰ中也可以通入 ,写出发生反应的离子方程式
,写出发生反应的离子方程式___________ 。
③已知 的溶解度随温度升高而变大,则步骤Ⅱ从
的溶解度随温度升高而变大,则步骤Ⅱ从 稀溶液中得到
稀溶液中得到 晶体的主要操作包括:
晶体的主要操作包括:__________________________ 。
(4)高铁酸盐(如高铁酸钾 )有强氧化性,是一种绿色的水处理剂。高铁酸盐可通过在碱性条件下氧化
)有强氧化性,是一种绿色的水处理剂。高铁酸盐可通过在碱性条件下氧化 制备。完成以下离子方程式:
制备。完成以下离子方程式:
_____ +_____
+_____ +______=______
+______=______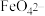 +_____
+_____ +_____,
+_____,______________
该反应中被氧化的元素是___________ ,每生成1mol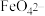 转移
转移___________ 个电子。
 晶体(图中夹持及尾气处理装置均已略去)。
晶体(图中夹持及尾气处理装置均已略去)。
(1)装置A中碎瓷片的作用是
(2)停止反应,待B管冷却后,取其中的固体,加入过量稀盐酸充分反应,过滤。简述检验滤液中
 的方法。
的方法。(3)该小组学生利用上述滤液制取
 晶体,设计流程如下:
晶体,设计流程如下:
①步骤I中加入的试剂可以是
a.酸性
 溶液 b.铁粉 c.稀
溶液 b.铁粉 c.稀 d.
d. 溶液
溶液②步骤Ⅰ中也可以通入
 ,写出发生反应的离子方程式
,写出发生反应的离子方程式③已知
 的溶解度随温度升高而变大,则步骤Ⅱ从
的溶解度随温度升高而变大,则步骤Ⅱ从 稀溶液中得到
稀溶液中得到 晶体的主要操作包括:
晶体的主要操作包括:(4)高铁酸盐(如高铁酸钾
 )有强氧化性,是一种绿色的水处理剂。高铁酸盐可通过在碱性条件下氧化
)有强氧化性,是一种绿色的水处理剂。高铁酸盐可通过在碱性条件下氧化 制备。完成以下离子方程式:
制备。完成以下离子方程式:_____
 +_____
+_____ +______=______
+______=______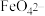 +_____
+_____ +_____,
+_____,该反应中被氧化的元素是
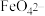 转移
转移
您最近一年使用:0次
10-11高三上·福建莆田·期中
解题方法
2 . 某校化学实验兴趣小组在“探究溴水与氯化亚铁溶液反应”的实验中发现:在足量的稀氯化亚铁溶液中,加入1—2滴溴水,振荡后溶液呈黄色。查阅资料显示:溴水是溴(Br2)的水溶液,呈黄色;溴水中含有溴单质。
(1)提出问题:Fe3+、Br2,谁的氧化性更强。
(2)猜想:
①甲同学认为氧化性:Fe3+>Br2,故上述实验现象不是发生化学反应所致,则溶液呈黄色是含_______ (填化学式,下同)所致
②乙同学认为氧化性:Br2>Fe3+,故上述实验现象是发生化学反应所致,则溶液呈黄色是含_______ 所致。
(3)设计实验并验证
丙同学为验证乙同学的观点,选用下列某些试剂设计出两种方案进行实验,并通过观察实验现象,证明了乙同学的观点确实是正确的。
除氯化亚铁溶液和溴水外,还有供选用的试剂:
a、酚酞试液;b、CCl4;c、无水酒精;d、KSCN溶液。
请你在下表中写出丙同学选用的试剂及实验中观察到的现象(试剂填序号)
(4)结论:氧化性:Br2>Fe3+。故在足量的稀氯化亚铁溶液中,加入1—2滴溴水,溶液呈黄色所发生的离子反应方程式为_______
(5)实验后的思考
①根据上述实验推测,若在溴化亚铁溶液中通入氯气,首先被氧化的离子是_______ (填离子的化学式)。
②在100mLFeBr2溶液中通入2.24LCl2(标准状况),溶液中有1/2的Br-被氧气成单质Br2,则原FeBr2溶液中FeBr2的物质的量浓度为_______ 。
(1)提出问题:Fe3+、Br2,谁的氧化性更强。
(2)猜想:
①甲同学认为氧化性:Fe3+>Br2,故上述实验现象不是发生化学反应所致,则溶液呈黄色是含
②乙同学认为氧化性:Br2>Fe3+,故上述实验现象是发生化学反应所致,则溶液呈黄色是含
(3)设计实验并验证
丙同学为验证乙同学的观点,选用下列某些试剂设计出两种方案进行实验,并通过观察实验现象,证明了乙同学的观点确实是正确的。
除氯化亚铁溶液和溴水外,还有供选用的试剂:
a、酚酞试液;b、CCl4;c、无水酒精;d、KSCN溶液。
请你在下表中写出丙同学选用的试剂及实验中观察到的现象(试剂填序号)
| 选用试剂 | 实验现象 | |
| 方案1 | ||
| 方案2 |
(5)实验后的思考
①根据上述实验推测,若在溴化亚铁溶液中通入氯气,首先被氧化的离子是
②在100mLFeBr2溶液中通入2.24LCl2(标准状况),溶液中有1/2的Br-被氧气成单质Br2,则原FeBr2溶液中FeBr2的物质的量浓度为
您最近一年使用:0次
2019-01-30更新
|
445次组卷
|
7卷引用:上海市长宁区2022-2023学年高一上学期学业综合评价化学试题
上海市长宁区2022-2023学年高一上学期学业综合评价化学试题(已下线)专题九 铁及其化合物(已下线)2011届福建省莆田一中高三上学期期中考试化学试卷(已下线)2012届福建省莆田一中高三第一学段考试化学试卷(已下线)2015届河南郑州市第四十七中学高三上第一次(10月)月考化学试卷(已下线)2014届浙江省衢州第二中学高三上学期期中考试化学试卷2016届河南省周口中英文学校高三上学期期中测试化学试卷
名校
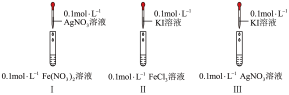
3 . 通过如下实验,比较 、
、 、
、 的氧化性。
的氧化性。
(1)实验室 溶液通常盛放在
溶液通常盛放在___________ 试剂瓶中。
(2)Ⅱ中反应的离子方程式为___________ 。
(3)I、Ⅱ中的现象说明___________。
(4)实验后,I试管壁上的黑色沉淀可用___________洗去。
(5)写出检验I中是否含有 的方法。
的方法。___________ 。
(6)检验Ⅱ中是否含有 不可选用:___________。(不定项)
不可选用:___________。(不定项)
(7)推测Ⅲ中未发生 氧化
氧化 的原因
的原因___________ 。
 、
、 、
、 的氧化性。
的氧化性。
| 实验现象 |
I中产生黑色沉淀,滴加 溶液,变红 溶液,变红 | |
| Ⅱ中溶液呈棕黄色,滴加淀粉溶液,变蓝 | |
| Ⅲ中产生黄色沉淀,滴加淀粉溶液,未变蓝 |
(1)实验室
 溶液通常盛放在
溶液通常盛放在(2)Ⅱ中反应的离子方程式为
(3)I、Ⅱ中的现象说明___________。
A.氧化性顺序: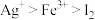 | B.氧化性顺序: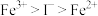 |
C.还原性顺序: | D.还原性顺序: |
(4)实验后,I试管壁上的黑色沉淀可用___________洗去。
| A.酒精 | B.二硫化碳 | C.浓硝酸 | D.热盐酸 |
(5)写出检验I中是否含有
 的方法。
的方法。(6)检验Ⅱ中是否含有
 不可选用:___________。(不定项)
不可选用:___________。(不定项)| A.氢氧化钠溶液 | B.酸性高辒酸钾溶液 | C.硫氰化钾溶液 | D.稀氨水 |
(7)推测Ⅲ中未发生
 氧化
氧化 的原因
的原因
您最近一年使用:0次
名校
4 . 某实验小组为了探究铁及其化合物的有关性质设计了如下实验:

现象Ⅱ:生成白色沉淀,3min后沉淀基本变为红褐色
现象Ⅲ:生成白色沉淀,3min后沉淀颜色几乎不变
(1)实验I中的现象为_______ ,该现象说明 具有
具有_______ 性,确定滤液A中不含 操作及现象为
操作及现象为_______ 。
(2)用化学方程式表示“现象Ⅱ”中沉淀由白色变为红褐色的原因_______ 。
(3)探究“现象Ⅲ”中白色沉淀的组成:
①查阅资料发现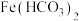 在水中不存在,由此对沉淀的组成作如下假设:
在水中不存在,由此对沉淀的组成作如下假设:
假设a:依据 溶液呈碱性,推测沉淀可能为
溶液呈碱性,推测沉淀可能为_______ ;(填化学式)
假设b:依据 溶液中存在的微粒,推测沉淀还可能为
溶液中存在的微粒,推测沉淀还可能为_______ ;(填化学式)
②验证上述假设的实验过程及现象如下,说明假设_______ 正确。(填“a”或“b”)
ⅰ.将白色沉淀进行充分洗涤后加入稀硫酸,沉淀完全溶解并产生无色气泡;
ⅱ.向ⅰ所得溶液中滴入KSCN试剂,溶液不变红;
ⅲ.向ⅱ所得溶液中再滴入少量新制氯水,溶液立即变为红色。
③实验小组发现,若将白色沉淀在空气中久置,最终也会变为红褐色。
(4)为探究溶液酸碱性对 还原性的影响,对比实验Ⅱ,设计了下图所示实验Ⅳ:
还原性的影响,对比实验Ⅱ,设计了下图所示实验Ⅳ:
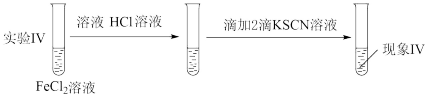
现象Ⅳ:溶液略显红色,3min后溶液颜色没有明显变深
根据实验Ⅰ~Ⅳ,避免 被空气氧化的措施有
被空气氧化的措施有_______ 。(写两条)

现象Ⅱ:生成白色沉淀,3min后沉淀基本变为红褐色
现象Ⅲ:生成白色沉淀,3min后沉淀颜色几乎不变
(1)实验I中的现象为
 具有
具有 操作及现象为
操作及现象为(2)用化学方程式表示“现象Ⅱ”中沉淀由白色变为红褐色的原因
(3)探究“现象Ⅲ”中白色沉淀的组成:
①查阅资料发现
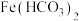 在水中不存在,由此对沉淀的组成作如下假设:
在水中不存在,由此对沉淀的组成作如下假设:假设a:依据
 溶液呈碱性,推测沉淀可能为
溶液呈碱性,推测沉淀可能为假设b:依据
 溶液中存在的微粒,推测沉淀还可能为
溶液中存在的微粒,推测沉淀还可能为②验证上述假设的实验过程及现象如下,说明假设
ⅰ.将白色沉淀进行充分洗涤后加入稀硫酸,沉淀完全溶解并产生无色气泡;
ⅱ.向ⅰ所得溶液中滴入KSCN试剂,溶液不变红;
ⅲ.向ⅱ所得溶液中再滴入少量新制氯水,溶液立即变为红色。
③实验小组发现,若将白色沉淀在空气中久置,最终也会变为红褐色。
(4)为探究溶液酸碱性对
 还原性的影响,对比实验Ⅱ,设计了下图所示实验Ⅳ:
还原性的影响,对比实验Ⅱ,设计了下图所示实验Ⅳ:
现象Ⅳ:溶液略显红色,3min后溶液颜色没有明显变深
根据实验Ⅰ~Ⅳ,避免
 被空气氧化的措施有
被空气氧化的措施有
您最近一年使用:0次
2023-02-16更新
|
295次组卷
|
2卷引用:上海市实验学校2022-2023学年高一下学期期末考试化学试题
名校
5 . 某班同学用如下实验探究 、
、 的性质。回答下列问题:
的性质。回答下列问题:
(1)甲组同学通过研究 对
对 稳定性的影响,得到如图所示结果,增强
稳定性的影响,得到如图所示结果,增强 稳定性的措施为
稳定性的措施为___________ 。 与的反应,进行如图所示实验:
与的反应,进行如图所示实验: 与
与 反应的离子方程式为
反应的离子方程式为___________ 。
为了探究白色沉淀产生的原因,同学们查阅资料得知:
i.CuSCN是难溶于水的白色固体;
ii.的化学性质与 相似;
相似;
iii.
实验方案如下:
(3) 与
与 反应的离子方程式为
反应的离子方程式为___________ 。
(4) 可用作补铁剂,使用时建议与维生素C同服。同学甲猜测维生素C可将
可用作补铁剂,使用时建议与维生素C同服。同学甲猜测维生素C可将 转化为
转化为 ,以利于人体吸收。为了验证这一猜想,设计了如下实验:
,以利于人体吸收。为了验证这一猜想,设计了如下实验:
由上述实验能否得出“维生素C可将 转化为
转化为 ”的结论?
”的结论?___________ (填“能”或“否”)请说明理由___________ 。
 、
、 的性质。回答下列问题:
的性质。回答下列问题:(1)甲组同学通过研究
 对
对 稳定性的影响,得到如图所示结果,增强
稳定性的影响,得到如图所示结果,增强 稳定性的措施为
稳定性的措施为
 与的反应,进行如图所示实验:
与的反应,进行如图所示实验:
 与
与 反应的离子方程式为
反应的离子方程式为为了探究白色沉淀产生的原因,同学们查阅资料得知:
i.CuSCN是难溶于水的白色固体;
ii.的化学性质与
 相似;
相似;iii.

实验方案如下:
| 实验方案 | 实验现象 |
步骤1:取 溶液,向其中滴加3滴 溶液,向其中滴加3滴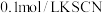 溶液 溶液 | 无明显现象 |
步骤2:取 溶液,向其中滴加3滴 溶液,向其中滴加3滴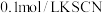 溶液 溶液 | 产生白色沉淀 |
 与
与 反应的离子方程式为
反应的离子方程式为(4)
 可用作补铁剂,使用时建议与维生素C同服。同学甲猜测维生素C可将
可用作补铁剂,使用时建议与维生素C同服。同学甲猜测维生素C可将 转化为
转化为 ,以利于人体吸收。为了验证这一猜想,设计了如下实验:
,以利于人体吸收。为了验证这一猜想,设计了如下实验:| 实验方案 | 实验现象 |
取适量 溶液于试管中,加入维生素C片,振荡溶解后,滴加酸性高锰酸钾溶液。 溶液于试管中,加入维生素C片,振荡溶解后,滴加酸性高锰酸钾溶液。 | 紫色褪去 |
 转化为
转化为 ”的结论?
”的结论?
您最近一年使用:0次
名校
解题方法
6 . 铁元素是重要的金属元素,含有铁元素的物质,在人类的生产生活中有着重要的应用。 是炼铁工业中的主反应.硫铁矿烧渣中含有大量
是炼铁工业中的主反应.硫铁矿烧渣中含有大量 ,工业上常用于制取绿矾
,工业上常用于制取绿矾 。铁元素的常见价态有
。铁元素的常见价态有 、
、 价,实验室可用赤血盐
价,实验室可用赤血盐 溶液检验
溶液检验 ,黄血盐
,黄血盐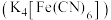 溶液检验
溶液检验 。下列关于铁及其化合物的性质与用途,不具有对应关系的是
。下列关于铁及其化合物的性质与用途,不具有对应关系的是
 是炼铁工业中的主反应.硫铁矿烧渣中含有大量
是炼铁工业中的主反应.硫铁矿烧渣中含有大量 ,工业上常用于制取绿矾
,工业上常用于制取绿矾 。铁元素的常见价态有
。铁元素的常见价态有 、
、 价,实验室可用赤血盐
价,实验室可用赤血盐 溶液检验
溶液检验 ,黄血盐
,黄血盐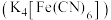 溶液检验
溶液检验 。下列关于铁及其化合物的性质与用途,不具有对应关系的是
。下列关于铁及其化合物的性质与用途,不具有对应关系的是A. 具有还原性,可用作食品抗氧化剂 具有还原性,可用作食品抗氧化剂 |
B. 属于碱性氧化物,可用作粉刷墙壁的红色涂料 属于碱性氧化物,可用作粉刷墙壁的红色涂料 |
C. 溶液中 溶液中 具有较强的氧化性,可制作印刷电路板 具有较强的氧化性,可制作印刷电路板 |
D. 胶体具有吸附性,可用作自来水的净水剂 胶体具有吸附性,可用作自来水的净水剂 |
您最近一年使用:0次
名校
解题方法
7 . 铁元素及其化合物在生活生产中有广泛的用途。回答下列问题:
(1)Fe3+与SCN-的反应常用来检验Fe3+的存在: Fe3+ + 3SCN- Fe(SCN)3
Fe(SCN)3
若溶液中含有Fe3+,则加入KSCN溶液后的现象为_________ 向加入KSCN后的混合溶液中再加入少量NaOH固体,观察到的现象是_____________ ,产生该现象的原因是________________ 。
(2)向FeSO4溶液中滴入NaOH溶液,会观察到先产生白色沉淀,后迅速变为灰绿色,久置后变为红褐色,用化学方程式说明产生该现象的原因__________________ 。
(3)FeCl3溶液常被用作蚀刻剂腐蚀印刷电路板: 2Fe3++ Cu==2Fe2+ + Cu2+在过量FeCl3溶液腐蚀印刷电路板后的溶液中,加入过量铁粉,依次发生______ 、________ 两个反应(写离子方程式),若最后溶液中有固体剩余,则溶液中不可能含有的离子是____ 。
(4)FeCl2溶液在空气中容易被氧化,0.1 mol· L-1的FeCl2溶液暴露在空气中,20min 后,Fe2+的浓度变为0.05 mol· L-1,则20 min内,以Fe2+ 表示的平均反应速率为_____________ 若要验证该溶液中Fe2+未被完全氧化,则可以需要加入_____ 若出现_________ 现象,则证明Fe2+未被完全氧化。
(5)下列有关铁及其化合物的说法正确的是________
A.铁是第四周期第VIIIB族元素
B.亚铁盐只有还原性,没有氧化性
C.铁粉和铜粉的混合物可用磁铁吸引的方法分离
D.工业上通常采用电解法来冶炼单质铁
E.Fe3O4是一种纯净物
F.铁粉和氧化铝的混合物是一种铝热剂
(1)Fe3+与SCN-的反应常用来检验Fe3+的存在: Fe3+ + 3SCN-
 Fe(SCN)3
Fe(SCN)3 若溶液中含有Fe3+,则加入KSCN溶液后的现象为
(2)向FeSO4溶液中滴入NaOH溶液,会观察到先产生白色沉淀,后迅速变为灰绿色,久置后变为红褐色,用化学方程式说明产生该现象的原因
(3)FeCl3溶液常被用作蚀刻剂腐蚀印刷电路板: 2Fe3++ Cu==2Fe2+ + Cu2+在过量FeCl3溶液腐蚀印刷电路板后的溶液中,加入过量铁粉,依次发生
(4)FeCl2溶液在空气中容易被氧化,0.1 mol· L-1的FeCl2溶液暴露在空气中,20min 后,Fe2+的浓度变为0.05 mol· L-1,则20 min内,以Fe2+ 表示的平均反应速率为
(5)下列有关铁及其化合物的说法正确的是
A.铁是第四周期第VIIIB族元素
B.亚铁盐只有还原性,没有氧化性
C.铁粉和铜粉的混合物可用磁铁吸引的方法分离
D.工业上通常采用电解法来冶炼单质铁
E.Fe3O4是一种纯净物
F.铁粉和氧化铝的混合物是一种铝热剂
您最近一年使用:0次
2022高一·上海·专题练习
解题方法
8 . 下列说法正确的是
| A.Fe3+的水溶液呈红褐色,Fe2+的水溶液呈浅绿色 |
| B.Fe3+具有氧化性,Fe2+具有还原性 |
| C.Fe3+的溶液中滴入含KSCN的溶液,立即出现红色沉淀 |
| D.铁粉可以和水蒸气在高温下反应生成Fe2O3 |
您最近一年使用:0次
9 . 下列陈述I、II正确并且有因果关系的是
| 选项 | 陈述I | 陈述II |
| A | Cl2有氧化性 | Cl2能使湿润的红色布条褪色 |
| B | SO2有漂白性 | SO2能使酸性KMnO4溶液褪色 |
| C | Al有还原性 | 利用铝热反应冶炼金属Mn |
| D | Fe3+有氧化性 | Fe3+遇KSCN溶液显血红色 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
10 . 已知下述四个实验均能发生化学反应:
下列判断不正确的是( )
| ① | ② | ③ | ④ |
| 将铁钉放入硫酸铜溶液中 | 向硫酸亚铁溶液中滴入几滴氯水 | 将铜丝放入氯化铁溶液中 | 向FeCl2溶液中滴入KSCN溶液,无明显现象,再滴入氯水,变红 |
| A.实验①中铁钉只做还原剂 |
| B.实验②中Fe2+只显还原性 |
| C.实验③中发生的是置换反应 |
| D.上述实验证明:氧化性:Fe3+>Cu2+>Fe2+,Fe2+遇KSCN溶液无红色物质生成 |
您最近一年使用:0次
2021-01-29更新
|
140次组卷
|
7卷引用:上海市嘉定区第一中学2021-2022学年高一下学期期期末考试化学试题