1 . 已知三氯化铁的熔点为306℃,沸点为315℃,易溶于水并且有强烈的吸水性,能吸收空气里的水分而潮解。某学习小组的同学对氯气与铁的反应及产物做了如下探究实验。_______ 。
(2)B中收集器里盛放冷水的作用是_______ 。D中碱石灰的作用是_______ 、_______ 。
(3)反应一段时间后熄灭酒精灯,冷却后将硬质玻璃管及收集器中的物质一并快速转移至锥形瓶中,加入过量的稀盐酸,充分反应后,进行如下实验:
固体混合物 淡黄色溶液
淡黄色溶液 淡红色溶液
淡红色溶液 深红色溶液
深红色溶液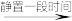 红色褪去
红色褪去
①试剂X为_______ (填化学式)。
②淡红色溶液中加入过量H2O2后溶液红色加深的原因是_______ 。
(4)该小组同学对上述溶液红色褪去的原因进行探究。
①取褪色后的溶液三份,分别进行以下实验,研究溶液中存在的微粒。
a.一份中滴加FeCl3溶液无明显变化,说明_______ ;
b.另一份滴加试剂X,溶液出现红色,说明_______ ;
c.还有一份滴加稀盐酸和BaCl2溶液,产生白色沉淀,说明_______ 。
②另取FeCl3溶液滴加2滴试剂X,溶液变红,再通入O2,无明显变化。实验②的目的是_______ ;得出结论:_______ 。
(2)B中收集器里盛放冷水的作用是
(3)反应一段时间后熄灭酒精灯,冷却后将硬质玻璃管及收集器中的物质一并快速转移至锥形瓶中,加入过量的稀盐酸,充分反应后,进行如下实验:
固体混合物
 淡黄色溶液
淡黄色溶液 淡红色溶液
淡红色溶液 深红色溶液
深红色溶液 红色褪去
红色褪去①试剂X为
②淡红色溶液中加入过量H2O2后溶液红色加深的原因是
(4)该小组同学对上述溶液红色褪去的原因进行探究。
①取褪色后的溶液三份,分别进行以下实验,研究溶液中存在的微粒。
a.一份中滴加FeCl3溶液无明显变化,说明
b.另一份滴加试剂X,溶液出现红色,说明
c.还有一份滴加稀盐酸和BaCl2溶液,产生白色沉淀,说明
②另取FeCl3溶液滴加2滴试剂X,溶液变红,再通入O2,无明显变化。实验②的目的是
您最近一年使用:0次
2022-07-02更新
|
1042次组卷
|
4卷引用:上海市控江中学2021-2022学年高一下学期期末考试化学试题
上海市控江中学2021-2022学年高一下学期期末考试化学试题上海市复兴高级中学2022-2023学年高一下学期5月学科能力评估化学试题(已下线)专题01 金属及其化合物 -【好题汇编】备战2023-2024学年高一化学下学期期末真题分类汇编(上海专用)河北省秦皇岛市昌黎第一中学2023届高三第一次调研考试化学试题
21-22高一下·上海浦东新·期末
名校
2 . 为探索工业含铝、铁、铜合金废料的再利用,某同学实设计的回收利用方案如下:
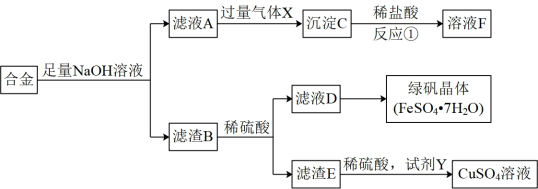
(1)滤渣B的主要成分为_______ ,溶液F的主要成分为_______ 。
(2)检验滤液D是否含有 的方法为
的方法为_______ 。
(3)从滤液D得到绿矾晶体,须进行的操作为:_______ 、_______ 、过滤洗涤、干燥。
(4)试剂Y可能为_______ 。
A.NO B. C.
C. D.
D.
与直接用浓硫酸与E反应制备 相比,用稀硫酸和试剂Y更符合“绿色化学”,的要求,原因是
相比,用稀硫酸和试剂Y更符合“绿色化学”,的要求,原因是_______ 、_______ 。
(5)若气体X为 ,请写出“滤液A”与过量气体X反应的离子方程式:
,请写出“滤液A”与过量气体X反应的离子方程式:_______ 。

(1)滤渣B的主要成分为
(2)检验滤液D是否含有
 的方法为
的方法为(3)从滤液D得到绿矾晶体,须进行的操作为:
(4)试剂Y可能为
A.NO B.
 C.
C. D.
D.
与直接用浓硫酸与E反应制备
 相比,用稀硫酸和试剂Y更符合“绿色化学”,的要求,原因是
相比,用稀硫酸和试剂Y更符合“绿色化学”,的要求,原因是(5)若气体X为
 ,请写出“滤液A”与过量气体X反应的离子方程式:
,请写出“滤液A”与过量气体X反应的离子方程式:
您最近一年使用:0次
21-22高一下·上海浦东新·期末
名校
3 . 通过一步反应不能实现的是
A.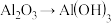 | B.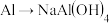 |
C.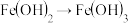 | D. |
您最近一年使用:0次
名校
4 . 在稀硫酸中加入铜粉,铜粉不溶解,再通入或滴入某种物质X(必要时可加热),发现铜粉逐渐溶解,则X不可能是
A. | B. | C. | D. |
您最近一年使用:0次
5 . 除去下列物质中含有的少量杂质(括号内为杂质),所用除杂试剂合理的是
A. 溶液( 溶液( ):氨水 ):氨水 | B.Fe(Al):NaOH溶液 |
C. ( ( ):KSCN溶液 ):KSCN溶液 | D. ( ( ):品红溶液 ):品红溶液 |
您最近一年使用:0次
名校
解题方法
6 . 铁是人体必需的微量元素,严重缺铁时需要服用补铁剂。实验小组为研究某补铁剂中铁元素的价态及其含量,设计并进行了如下实验:
【查阅资料】
Ⅰ.该补铁剂不溶于水,但能溶于人体中的胃液(含盐酸)。
Ⅱ.KSCN中的硫元素为 价。
价。
实验Ⅰ.检验该补铁剂中铁元素的价态。

(1)试剂1是_______ ,试剂2是_______ (写出物质名称)。
(2)加入试剂2后溶液变为浅红色,此现象说明溶液①中含有_______ (填微粒符号)。
(3)能证明溶液①中含有 的实验现象是
的实验现象是_______ 。
(4)写出上述条件下 与
与 发生反应的离子方程式:
发生反应的离子方程式:_______ 。
(5)甲同学猜测深红色溶液③迅速变为无色溶液④的原因,可能是溶液中的 与
与 发生了化学反应。甲同学猜测的理论依据是
发生了化学反应。甲同学猜测的理论依据是_______ 。
实验Ⅱ.测定该补铁剂中铁元素的含量。

(6)计算每片该补铁剂含铁元素的质量为_______ g。
【查阅资料】
Ⅰ.该补铁剂不溶于水,但能溶于人体中的胃液(含盐酸)。
Ⅱ.KSCN中的硫元素为
 价。
价。实验Ⅰ.检验该补铁剂中铁元素的价态。

(1)试剂1是
(2)加入试剂2后溶液变为浅红色,此现象说明溶液①中含有
(3)能证明溶液①中含有
 的实验现象是
的实验现象是(4)写出上述条件下
 与
与 发生反应的离子方程式:
发生反应的离子方程式:(5)甲同学猜测深红色溶液③迅速变为无色溶液④的原因,可能是溶液中的
 与
与 发生了化学反应。甲同学猜测的理论依据是
发生了化学反应。甲同学猜测的理论依据是实验Ⅱ.测定该补铁剂中铁元素的含量。

(6)计算每片该补铁剂含铁元素的质量为
您最近一年使用:0次
名校
解题方法
7 . 除去下列物质中的杂质(括号内为杂质),选择试剂及操作方法均正确的是。
A. ,饱和碳酸钠溶液,洗气 ,饱和碳酸钠溶液,洗气 |
B. 溶液 溶液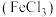 ,铜粉,过滤 ,铜粉,过滤 |
C.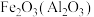 ,NaOH溶液,过滤 ,NaOH溶液,过滤 |
D. 溶液 溶液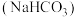 ,通足量 ,通足量 |
您最近一年使用:0次
8 . 为减少 排放,可利用如图所示的工艺流程,下列说法正确的是
排放,可利用如图所示的工艺流程,下列说法正确的是

 排放,可利用如图所示的工艺流程,下列说法正确的是
排放,可利用如图所示的工艺流程,下列说法正确的是
| A.对流程内每个反应而言,一共有两种元素涉及了化合价变化 |
B.其中一步反应的离子方程式为: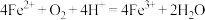 |
C.该过程总反应相当于仅消耗 与 与 生成 生成 |
D.通入足量 后,取样滴加 后,取样滴加 溶液不会变血红 溶液不会变血红 |
您最近一年使用:0次
2022-06-29更新
|
296次组卷
|
2卷引用:上海交通大学附属中学2021-2022 学年高一下学期阶段性考试化学试题
名校
9 . 铝、铁是生产、生活中常见的金属,其合金与盐在各领域都有着广泛的应用。
(1)铝合金是一种建筑装潢材料,它具有坚硬、轻巧、耐用的特性。铝合金的下列性质与这些特性无关的是
(2)铝元素在周期表中的位置是_______ 。写出 与稀硫酸反应的离子方程式
与稀硫酸反应的离子方程式_______ 。铁粉与水蒸气在高温条件下反应,生成的固态产物是_______ 。
(3)焊接金属时常用的焊接液为氯化铵,其作用是消除焊接金属表面的铁锈。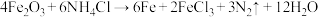 ;上述反应中当生成3.36L氮气(标准状况)时,转移的电子数为
;上述反应中当生成3.36L氮气(标准状况)时,转移的电子数为_______ 个,有同学认为,该反应产物中不应该有Fe生成,他的理由是(用化学方程式表示原因)_______ 。
(4)现有仪器和药品:试管和胶头滴管,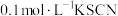 溶液、
溶液、 酸性
酸性 溶液、
溶液、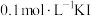 溶液、氯水等。请你设计一个简单实验,探究铁与稀硝酸完全反应后铁可能的价态,填写下列实验报告:
溶液、氯水等。请你设计一个简单实验,探究铁与稀硝酸完全反应后铁可能的价态,填写下列实验报告:
(1)铝合金是一种建筑装潢材料,它具有坚硬、轻巧、耐用的特性。铝合金的下列性质与这些特性无关的是
| A.不易生锈 | B.导电性好 | C.密度小 | D.硬度大 |
 与稀硫酸反应的离子方程式
与稀硫酸反应的离子方程式(3)焊接金属时常用的焊接液为氯化铵,其作用是消除焊接金属表面的铁锈。
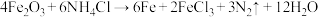 ;上述反应中当生成3.36L氮气(标准状况)时,转移的电子数为
;上述反应中当生成3.36L氮气(标准状况)时,转移的电子数为(4)现有仪器和药品:试管和胶头滴管,
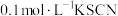 溶液、
溶液、 酸性
酸性 溶液、
溶液、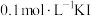 溶液、氯水等。请你设计一个简单实验,探究铁与稀硝酸完全反应后铁可能的价态,填写下列实验报告:
溶液、氯水等。请你设计一个简单实验,探究铁与稀硝酸完全反应后铁可能的价态,填写下列实验报告:| 实验步骤 | 操作 | 现象与结论 |
| 第一步 | 取少量液体装于试管,向试管中滴入几滴 溶液。 溶液。 | |
| 第二步 |  。 。 |
您最近一年使用:0次
2022-06-28更新
|
231次组卷
|
2卷引用:上海市宜川中学2021-2022学年高一下学期期末考试化学试题
10 . 能将溶液中的 转化成
转化成 的物质是
的物质是
 转化成
转化成 的物质是
的物质是A. | B. | C. | D. |
您最近一年使用:0次



