名校
1 . 向一定质量 和
和 的混合溶液中逐渐加入足量的锌粒,下列图像能正确反映对应关系的是
的混合溶液中逐渐加入足量的锌粒,下列图像能正确反映对应关系的是
 和
和 的混合溶液中逐渐加入足量的锌粒,下列图像能正确反映对应关系的是
的混合溶液中逐渐加入足量的锌粒,下列图像能正确反映对应关系的是A.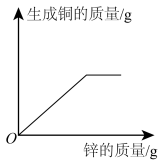 | B.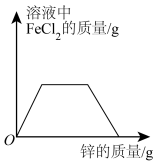 |
C.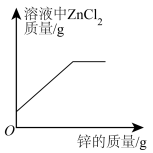 | D.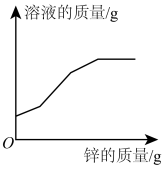 |
您最近一年使用:0次
2023-09-28更新
|
206次组卷
|
4卷引用:安徽省九师联盟2023-2024学年高三上学期9月月考化学试题
2 . 下列实验操作、现象和结论均正确且有对应关系的是
| 选项 | 实验操作、现象 | 结论 |
| A | 将铁片溶于稀硫酸中,滴加铁氰化钾溶液,产生蓝色沉淀 | 说明铁片表面没有生成 |
| B | 在酸性 溶液中滴加葡萄糖溶液,溶液褪色 溶液中滴加葡萄糖溶液,溶液褪色 | 说明葡萄糖具有还原性 |
| C | 在硫酸四氨合铜溶液中加入乙醇,析出蓝色晶体 | 说明乙醇具有吸水性 |
| D | 在2mL0.1  溶液中滴加少量新制的氯水,溶液变黄色 溶液中滴加少量新制的氯水,溶液变黄色 | 说明还原性: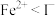 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
3 . 下列有关物质的性质和用途说法不正确 的是
| A.利用高纯单质硅的半导体性能,可以制成光电池 |
| B.国庆节天安门广场燃放烟花,色彩绚丽,利用了某些金属元素的焰色试验 |
| C.Na2O2与CO2反应放出氧气,可用于制作呼吸面具 |
| D.用氯化铁溶液刻蚀覆铜板制作印刷电路板,铜与FeCl3发生置换反应 |
您最近一年使用:0次
名校
解题方法
4 . 如图所示为部分物质(或其溶液)间的转化关系(除水外,其他反应物、生成物均已列出)。已知 为紫红色金属单质,
为紫红色金属单质, 为能使带火星的木条复燃的气体,
为能使带火星的木条复燃的气体, 为红褐色沉淀,
为红褐色沉淀, 的焰色试验呈紫色(透过蓝色钴玻璃),回答下列问题。
的焰色试验呈紫色(透过蓝色钴玻璃),回答下列问题。

(1)写出下列物质的化学式:A___________ 、G___________ 。
(2)I加热分解产生的固体产物俗称___________ ,写出其一种用途:___________ 。
(3)F与H作用生成I的化学方程式为___________ ; 与
与 反应的离子方程式为
反应的离子方程式为___________ 。
(4)除去D溶液中混有的J,最好使用的方法是___________ (用离子方程式表示)。
 为紫红色金属单质,
为紫红色金属单质, 为能使带火星的木条复燃的气体,
为能使带火星的木条复燃的气体, 为红褐色沉淀,
为红褐色沉淀, 的焰色试验呈紫色(透过蓝色钴玻璃),回答下列问题。
的焰色试验呈紫色(透过蓝色钴玻璃),回答下列问题。
(1)写出下列物质的化学式:A
(2)I加热分解产生的固体产物俗称
(3)F与H作用生成I的化学方程式为
 与
与 反应的离子方程式为
反应的离子方程式为(4)除去D溶液中混有的J,最好使用的方法是
您最近一年使用:0次
解题方法
5 . 向少量 粉末中加入适量盐酸,反应后得到的
粉末中加入适量盐酸,反应后得到的 溶液呈棕黄色。回答下列问题:
溶液呈棕黄色。回答下列问题:
(1)赤铁矿的主要成分为 ,
, 俗称
俗称_______ ,请写出 的一种用途:
的一种用途:_______ 。
(2)取少量 溶液置于试管中,加入过量铁粉,该反应的离子方程式为
溶液置于试管中,加入过量铁粉,该反应的离子方程式为_______ 。
(3)向(2)反应后的溶液中加入NaOH溶液,产生的白色沉淀最终变为红褐色,请解释沉淀颜色变化的原因:_______ (用化学方程式表示)。
(4)在小烧杯中加入20mL蒸馏水,加热至沸腾后,向沸水中滴入几滴 溶液,继续煮沸至溶液呈
溶液,继续煮沸至溶液呈_______ 色,即可制得 胶体。
胶体。
(5)取另一烧杯也加入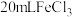 溶液,将此烧杯(编号甲)与盛有
溶液,将此烧杯(编号甲)与盛有 胶体的烧杯(编号乙)一起放黑暗处:分别用激光笔照射烧杯中的液体,可以看到
胶体的烧杯(编号乙)一起放黑暗处:分别用激光笔照射烧杯中的液体,可以看到_______ (填“编号甲”或“编号乙”)烧杯中的液体会产生丁达尔效应。这个实验可以用来区别_______ 。
 粉末中加入适量盐酸,反应后得到的
粉末中加入适量盐酸,反应后得到的 溶液呈棕黄色。回答下列问题:
溶液呈棕黄色。回答下列问题:(1)赤铁矿的主要成分为
 ,
, 俗称
俗称 的一种用途:
的一种用途:(2)取少量
 溶液置于试管中,加入过量铁粉,该反应的离子方程式为
溶液置于试管中,加入过量铁粉,该反应的离子方程式为(3)向(2)反应后的溶液中加入NaOH溶液,产生的白色沉淀最终变为红褐色,请解释沉淀颜色变化的原因:
(4)在小烧杯中加入20mL蒸馏水,加热至沸腾后,向沸水中滴入几滴
 溶液,继续煮沸至溶液呈
溶液,继续煮沸至溶液呈 胶体。
胶体。(5)取另一烧杯也加入
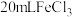 溶液,将此烧杯(编号甲)与盛有
溶液,将此烧杯(编号甲)与盛有 胶体的烧杯(编号乙)一起放黑暗处:分别用激光笔照射烧杯中的液体,可以看到
胶体的烧杯(编号乙)一起放黑暗处:分别用激光笔照射烧杯中的液体,可以看到
您最近一年使用:0次
6 . 铁及其化合物在生产生活中有重要用途。某化学兴趣小组同学设计以下实验探究铁及其化合物性质。
Ⅰ.氢氧化亚铁的制备:
两组同学分别设计如下实验探究能较长时间观察到白色Fe(OH)2沉淀的制取方法。
A组实验:用NaOH溶液和FeSO4溶液直接反应。(如图1)
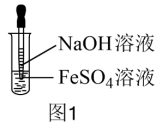
(1) FeSO4可由铁粉还原Fe2(SO4)3制得,反应的离子方程式是:_______ 。
(2)该方法能观察到白色Fe(OH)2沉淀,但沉淀颜色快速发生变化,其颜色变化为_______ 。
B组实验:选用稀硫酸、铁粉、NaOH溶液进行实验,装置如图2。

(3)实验时,先_______ (填“打开”或“关闭”)止水夹K,然后打开分液漏斗的玻璃塞和活塞,使稀硫酸与铁粉反应,一段时间后, _______ (填“打开”或“关闭”)止水夹K,制得白色Fe(OH)2沉淀,且沉淀能持续一段时间不变色。
Ⅱ.“铁与水反应”的实验,并检验产物的性质:

(4)①A装置的作用是_______ B中反应的化学方程式为_______ 。
②D的作用是_______ 。
③点燃E处酒精灯之前应进行的操作是_______ 。
Ⅰ.氢氧化亚铁的制备:
两组同学分别设计如下实验探究能较长时间观察到白色Fe(OH)2沉淀的制取方法。
A组实验:用NaOH溶液和FeSO4溶液直接反应。(如图1)

(1) FeSO4可由铁粉还原Fe2(SO4)3制得,反应的离子方程式是:
(2)该方法能观察到白色Fe(OH)2沉淀,但沉淀颜色快速发生变化,其颜色变化为
B组实验:选用稀硫酸、铁粉、NaOH溶液进行实验,装置如图2。

(3)实验时,先
Ⅱ.“铁与水反应”的实验,并检验产物的性质:

(4)①A装置的作用是
②D的作用是
③点燃E处酒精灯之前应进行的操作是
您最近一年使用:0次
7 . 下图中A~J均为中学化学中常见的物质,它们之间有如下转化关系。其中,A、D为金属单质,A 是地壳中含量最多的金属。(反应过程中生成的水及其它产物已略去),D的合金目前用量最大用途最广。请回答以下问题:
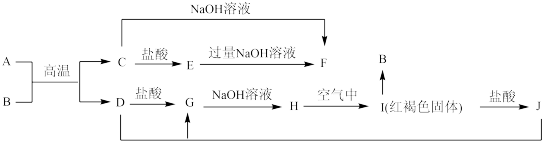
(1)C是_______ ,H是_______ (填化学式)。
(2)写出J与D反应转化为G的离子方程式:_______ 。
(3)A在常温下也可与NaOH溶液反应生成F,写出此反应的化学方程式:_______ 。
(4)写出H在空气中生成I对应方程式_______ 。
(5)写出一种B的用途_______ 。

(1)C是
(2)写出J与D反应转化为G的离子方程式:
(3)A在常温下也可与NaOH溶液反应生成F,写出此反应的化学方程式:
(4)写出H在空气中生成I对应方程式
(5)写出一种B的用途
您最近一年使用:0次



