解题方法
1 . 进行利用覆铜板制作图案的实验时,主要实验过程如下:

下列说法不正确 的是

下列说法
| A.覆铜板上写“化学”两字的笔,不能用水溶性墨水的笔 |
B.将覆铜板浸没在 溶液中,除了“化学”两字外的覆铜层几乎都被溶解反应了 溶液中,除了“化学”两字外的覆铜层几乎都被溶解反应了 |
| C.“腐蚀液”反应前后离子种类发生变化,离子总数目保持不变 |
D.使用后的“腐蚀液”,可加入铁粉、氯水等,实现 的回收和 的回收和 溶液的再生 溶液的再生 |
您最近一年使用:0次
名校
解题方法
2 . 已知 某溶液(该溶液称为
某溶液(该溶液称为 )中仅含有两种溶质
)中仅含有两种溶质 和
和 ,且物质的量浓度依次为
,且物质的量浓度依次为 和
和 ,向该溶液中投入
,向该溶液中投入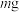 铁粉恰好完全反应,释放出的气体体积为
铁粉恰好完全反应,释放出的气体体积为 。下列叙述正确的是
。下列叙述正确的是
 某溶液(该溶液称为
某溶液(该溶液称为 )中仅含有两种溶质
)中仅含有两种溶质 和
和 ,且物质的量浓度依次为
,且物质的量浓度依次为 和
和 ,向该溶液中投入
,向该溶液中投入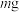 铁粉恰好完全反应,释放出的气体体积为
铁粉恰好完全反应,释放出的气体体积为 。下列叙述正确的是
。下列叙述正确的是A. 中 中 的物质的量为 的物质的量为 |
B.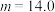 |
C.反应后所得溶液中氧化产物与还原产物的物质的量之比为 |
D.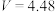 |
您最近一年使用:0次
3 . 实验室由硫铁矿烧渣(主要成分为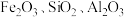 )制备软磁性材料
)制备软磁性材料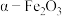 ,主要转化流程如下。
,主要转化流程如下。
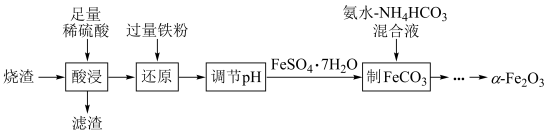
已知: 为酸性氧化物。
为酸性氧化物。
回答下列问题:
(1)“酸浸”时, 与稀硫酸反应的化学方程式为
与稀硫酸反应的化学方程式为______________ ;“滤渣”中主要成分的化学式为______________ 。
(2)“还原”时,加入过量铁粉的主要目的是______________ ;该过程除生成 外,还会生成
外,还会生成_______ (填化学式)。
(3)根据表格信息,“调节 ”时的
”时的 范围为
范围为_______ 。
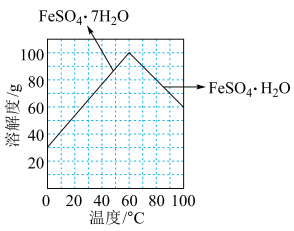
(4)“调节 ”后获得
”后获得 晶体,根据如图所示的绿矾溶解度曲线,补充完整“调节
晶体,根据如图所示的绿矾溶解度曲线,补充完整“调节 ”后获得
”后获得 晶体的实验操作:向
晶体的实验操作:向 溶液中先加入稀硫酸酸化,在
溶液中先加入稀硫酸酸化,在 氛围中,
氛围中,_______ ,过滤,少量冰水洗涤,低温干燥,得到 晶体。
晶体。
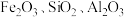 )制备软磁性材料
)制备软磁性材料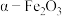 ,主要转化流程如下。
,主要转化流程如下。
离子 | 开始沉淀 | 完全沉淀 |
| 5.8 | 8.8 |
| 1.6 | 2.8 |
| 3.2 | 5.0 |
 为酸性氧化物。
为酸性氧化物。回答下列问题:
(1)“酸浸”时,
 与稀硫酸反应的化学方程式为
与稀硫酸反应的化学方程式为(2)“还原”时,加入过量铁粉的主要目的是
 外,还会生成
外,还会生成(3)根据表格信息,“调节
 ”时的
”时的 范围为
范围为(4)“调节
 ”后获得
”后获得 晶体,根据如图所示的绿矾溶解度曲线,补充完整“调节
晶体,根据如图所示的绿矾溶解度曲线,补充完整“调节 ”后获得
”后获得 晶体的实验操作:向
晶体的实验操作:向 溶液中先加入稀硫酸酸化,在
溶液中先加入稀硫酸酸化,在 氛围中,
氛围中, 晶体。
晶体。
您最近一年使用:0次
解题方法
4 . 下列实验现象与操作相对应的是
| 操作 | 现象 | |
| A | 向 固体滴加几滴水,用温度计测定温度变化 固体滴加几滴水,用温度计测定温度变化 | 温度升高 |
| B | 用玻璃棒蘸取 与水反应后的溶液,涂抹在 与水反应后的溶液,涂抹在 试纸上 试纸上 | 试纸变蓝 |
| C | 在盛有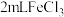 溶液中加入过量铁粉 溶液中加入过量铁粉 | 溶液由浅绿色变为棕黄色 |
| D | 将镁条投入冷水中,滴加两滴酚酞,充分反应 | 无明显现象 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
5 . 类比推断是学习化学的重要方法,下列推断正确的是
A. 可改写为 可改写为 ,则 ,则 也可改写为 也可改写为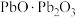 ( (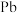 为IVA族元素) 为IVA族元素) |
B. 可由化合反应制备,则 可由化合反应制备,则 也可以由化合反应制备 也可以由化合反应制备 |
C. 与硝酸和氢碘酸反应均为氧化还原反应,则 与硝酸和氢碘酸反应均为氧化还原反应,则 与这两种酸反应也为氧化还原反应 与这两种酸反应也为氧化还原反应 |
D. 与 与 溶液不反应,则 溶液不反应,则 与 与 溶液也不反应 溶液也不反应 |
您最近一年使用:0次
6 . 糕点礼盒中经常放入食品脱氧剂。有一种常见固体脱氧剂的组成为铁粉、炭粉、氯化钠等,下列对脱氧剂所涉及的物质的说法正确的是
| A.过量的铁粉与稀硝酸反应的产物为硝酸铁 |
B.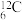 和 和 互为同素异形体 互为同素异形体 |
C.氯化钠的形成过程可表示为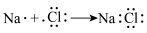 |
| D.该脱氧剂在潮湿的环境中会形成原电池 |
您最近一年使用:0次
2023-07-18更新
|
63次组卷
|
2卷引用:河南省焦作市2022-2023学年高一下学期6月期末考试化学试题
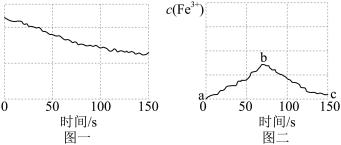
7 . 利用传感器和信息处理终端对氯水的实验进行数据采集与分析得到以下图像,图一表示氯水长时间放置在空气中,随着反应进行某种量的变化;图二表示将过量铁粉加入氯水中, 浓度的变化曲线。下列说法错误的是
浓度的变化曲线。下列说法错误的是
 浓度的变化曲线。下列说法错误的是
浓度的变化曲线。下列说法错误的是
A.图一可表示: 随光照时间的变化曲线 随光照时间的变化曲线 |
B.图一可表示 随光照时间的变化曲线 随光照时间的变化曲线 |
C.图二ab段测得有 ,可能是Fe与 ,可能是Fe与 反应生成的 反应生成的 |
D.图二bc段表明溶液中的反应以 为主 为主 |
您最近一年使用:0次
8 . 从刻蚀印刷电路板的废液(主要成分为FeCl2、FeCl3、CuCl2)中回收铜并制备氯化铁晶体的一种工业流程如图:

回答下列问题:
(1)操作I的名称是___________ ,试剂a的化学式为___________ 。
(2)用FeCl3溶液刻蚀铜电路板的化学方程式为___________ 。
(3)试剂c可选用___________ (填标号)。若选择上述试剂,反应I中氧化剂与还原剂的物质的量之比为___________ 。
A.Zn B.H2O2 C.NaOH D.稀H2SO4
(4)为检验氯化铁晶体中是否混有FeCl2,某同学设计方案为:取少许样品于试管中,滴加稀硝酸。若观察到产生气泡,试管口附近有___________ 色气体产生,则混有FeCl2.从环保角度考虑,该实验方案存在的不足之处是___________ 。
(5)取1.000g产物溶于水中,加入足量NaOH溶液,经过滤、洗涤、灼烧后,所得红棕色固体的质量为0.320g,则该产物中铁元素的质量分数为___________ %。

回答下列问题:
(1)操作I的名称是
(2)用FeCl3溶液刻蚀铜电路板的化学方程式为
(3)试剂c可选用
A.Zn B.H2O2 C.NaOH D.稀H2SO4
(4)为检验氯化铁晶体中是否混有FeCl2,某同学设计方案为:取少许样品于试管中,滴加稀硝酸。若观察到产生气泡,试管口附近有
(5)取1.000g产物溶于水中,加入足量NaOH溶液,经过滤、洗涤、灼烧后,所得红棕色固体的质量为0.320g,则该产物中铁元素的质量分数为
您最近一年使用:0次
9 . 二氧化铈可用在化妆品中起到抗紫外线作用,工业上以氟碳铈矿(CeCO3F,含Fe2O3、SiO2、Al2O3等杂质)为原料制备二氧化铈、硫酸铝铵晶体 和硫酸亚铁铵
和硫酸亚铁铵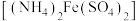 晶体,其工艺流程如图所示:
晶体,其工艺流程如图所示:
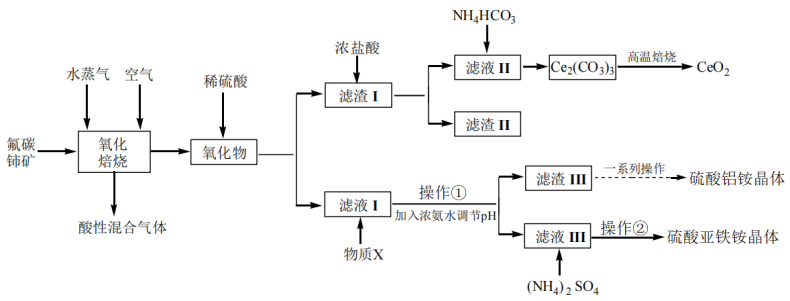
已知:①CeO2不溶于稀硫酸,也不溶于NaOH溶液,Ce2O3易溶于强酸。
②常见离子开始沉淀和完全沉淀pH表
回答下列问题:
(1)“氧化焙烧”时,气体与矿料逆流而行进行投料,其目的是___________ ,此时,发生化学方程式为___________ 。
(2)“滤渣Ⅰ”的主要成分是___________ 和___________ (填化学式)。虽浓盐酸价格便宜,但用于溶解“滤渣Ⅰ”的缺点是___________ ,若用稀硫酸和双氧水代替浓盐酸,则发生反应的离子方程式为___________ 。
(3)“滤液Ⅰ”中加入物质X的目的是___________ 。
(4)“操作①”加入浓氨水调节pH后,溶液pH范围是___________ 。
(5)“滤渣Ⅲ”在制备硫酸铝铵晶体过程中,理论上需加入稀硫酸和(NH4)2SO4的物质的量之比为___________ 。
 和硫酸亚铁铵
和硫酸亚铁铵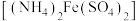 晶体,其工艺流程如图所示:
晶体,其工艺流程如图所示:
已知:①CeO2不溶于稀硫酸,也不溶于NaOH溶液,Ce2O3易溶于强酸。
②常见离子开始沉淀和完全沉淀pH表
| 离子 |  |  |  |
| 开始沉淀时的pH | 7.6 | 1.5 | 3.4 |
| 完全沉淀时的pH | 9.6 | 2.8 | 4.7 |
(1)“氧化焙烧”时,气体与矿料逆流而行进行投料,其目的是
(2)“滤渣Ⅰ”的主要成分是
(3)“滤液Ⅰ”中加入物质X的目的是
(4)“操作①”加入浓氨水调节pH后,溶液pH范围是
(5)“滤渣Ⅲ”在制备硫酸铝铵晶体过程中,理论上需加入稀硫酸和(NH4)2SO4的物质的量之比为
您最近一年使用:0次
解题方法
10 . 用硫铁矿烧渣(主要成分为 和少量
和少量 )为原料可以制得绿矾(
)为原料可以制得绿矾( )产品,其制备流程如下。
)产品,其制备流程如下。
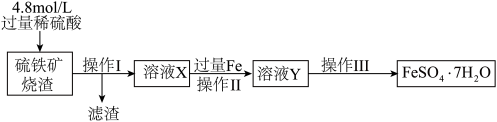
已知: 不能与稀硫酸反应。
不能与稀硫酸反应。
Ⅰ、配制250mL4.8mol/L的稀硫酸溶液
(1)需要用到的玻璃仪器主要是量筒、烧杯、玻璃棒、胶头滴管和___________ (填仪器名称)。
(2)下列操作会引起结果偏高的是___________(选填字母序号)。
Ⅱ、绿矾的制备流程图中
(3)工艺生产中,常将硫铁矿烧渣粉碎,这样做的目的是___________ 。
(4)往溶液X中加过量铁粉时,溶液颜色由棕黄色变为浅绿色且有气泡产生,该过程中反应的离子方程式为___________ 和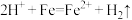 。
。
(5)操作Ⅲ指的是蒸发浓缩、___________ (填操作名称)、过滤、洗涤、干燥。检验溶液Y是否含有 的试剂是
的试剂是___________ (选填字母编号)。
A.KSCN溶液 B.酸性 溶液 C.新制氯水
溶液 C.新制氯水
(6)充分灼烧15.0g绿矾产品,可得到4.0g某种红棕色固体。则该红棕色固体是___________ ,该绿矾产品的纯度为___________ (结果保留一位小数)。
 和少量
和少量 )为原料可以制得绿矾(
)为原料可以制得绿矾( )产品,其制备流程如下。
)产品,其制备流程如下。
已知:
 不能与稀硫酸反应。
不能与稀硫酸反应。Ⅰ、配制250mL4.8mol/L的稀硫酸溶液
(1)需要用到的玻璃仪器主要是量筒、烧杯、玻璃棒、胶头滴管和
(2)下列操作会引起结果偏高的是___________(选填字母序号)。
| A.未洗涤玻璃棒 | B.容量瓶未干燥,含有少量蒸馏水 |
| C.摇匀后液面下降,补充水 | D.定容时俯视刻度线 |
Ⅱ、绿矾的制备流程图中
(3)工艺生产中,常将硫铁矿烧渣粉碎,这样做的目的是
(4)往溶液X中加过量铁粉时,溶液颜色由棕黄色变为浅绿色且有气泡产生,该过程中反应的离子方程式为
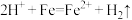 。
。(5)操作Ⅲ指的是蒸发浓缩、
 的试剂是
的试剂是A.KSCN溶液 B.酸性
 溶液 C.新制氯水
溶液 C.新制氯水(6)充分灼烧15.0g绿矾产品,可得到4.0g某种红棕色固体。则该红棕色固体是
您最近一年使用:0次



