22-23高一下·浙江·期中
1 . 将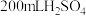 和
和 的混合溶液分成两等份。向其中一份中加入足量铁粉,充分反应后测的固体质量减少
的混合溶液分成两等份。向其中一份中加入足量铁粉,充分反应后测的固体质量减少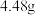 ;向另一份中加入足量
;向另一份中加入足量 溶液,经过滤、洗涤、干燥、称量,得到
溶液,经过滤、洗涤、干燥、称量,得到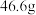 白色沉淀。请计算:
白色沉淀。请计算:
(1)其中一份溶液中加入足量的铁粉发生的反应有两个,写出对应的离子方程式:①___________ 、②___________ 。
(2)原溶液中
___________  ;
;
(3)原溶液中 和
和 的物质的量浓度之比为
的物质的量浓度之比为___________ 。
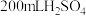 和
和 的混合溶液分成两等份。向其中一份中加入足量铁粉,充分反应后测的固体质量减少
的混合溶液分成两等份。向其中一份中加入足量铁粉,充分反应后测的固体质量减少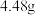 ;向另一份中加入足量
;向另一份中加入足量 溶液,经过滤、洗涤、干燥、称量,得到
溶液,经过滤、洗涤、干燥、称量,得到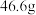 白色沉淀。请计算:
白色沉淀。请计算:(1)其中一份溶液中加入足量的铁粉发生的反应有两个,写出对应的离子方程式:①
(2)原溶液中

 ;
;(3)原溶液中
 和
和 的物质的量浓度之比为
的物质的量浓度之比为
您最近一年使用:0次
解题方法
2 . 有一稀硫酸和硝酸铁的混合溶液,向其中加入铁粉,溶液中的Fe2+浓度如图所示(不考虑溶液体积的变化):
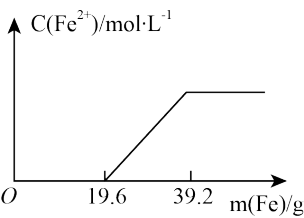
溶液中H2SO4与Fe(NO3)3的物质的量之比为_______

溶液中H2SO4与Fe(NO3)3的物质的量之比为
您最近一年使用:0次
3 . 有硫酸、硫酸亚铁、硫酸铁的混合溶液100 mL,已知溶液中各阳离子的物质的量浓度相等,SO 的物质的量浓度为3.0 mol·L−1。请计算:
的物质的量浓度为3.0 mol·L−1。请计算:
(1)SO 的物质的量为
的物质的量为_______ mol。
(2)理论上此溶液最多可溶解铁粉的质量为_______ g。
 的物质的量浓度为3.0 mol·L−1。请计算:
的物质的量浓度为3.0 mol·L−1。请计算:(1)SO
 的物质的量为
的物质的量为(2)理论上此溶液最多可溶解铁粉的质量为
您最近一年使用:0次
名校
4 . 完成下面有关计算,并在空白处填写结果。
(1)若将0.6mol钠、铁、铝分别投入100mL1mol·L-1盐酸中,在标准状况下,产生氢气的体积之比是___ 。
(2)一定量的苏打和小苏打固体分别与足量的稀盐酸反应,若产生的气体体积在标况下均为33.6L,则二者消耗HCl的物质的量之比为___ ,需要二者的固体质量之比为___ 。
(3)将6g铁粉加入200mLFe2(SO4)3和CuSO4的混合溶液中,充分反应得到200mL0.5mol/LFeSO4溶液和5.2g固体沉淀物。则反应后生成铜的质量为___ ,原Fe2(SO4)3溶液的物质的量浓度为____ 。
(1)若将0.6mol钠、铁、铝分别投入100mL1mol·L-1盐酸中,在标准状况下,产生氢气的体积之比是
(2)一定量的苏打和小苏打固体分别与足量的稀盐酸反应,若产生的气体体积在标况下均为33.6L,则二者消耗HCl的物质的量之比为
(3)将6g铁粉加入200mLFe2(SO4)3和CuSO4的混合溶液中,充分反应得到200mL0.5mol/LFeSO4溶液和5.2g固体沉淀物。则反应后生成铜的质量为
您最近一年使用:0次
名校
5 . 印刷电路板是由高分子材料和铜箔复合而成,刻制印刷电路时,要用FeCl3溶液作为“腐蚀液”,生成CuCl2和FeCl2。现有一包铁粉和铜粉的混合粉末17.6g,使其完全溶解恰好需要200mL3.0mol/L的FeCl3溶液。假设溶液反应前后体积不变,试计算:(注意:无计算过程不给分)
(1)混合粉末中铜的质量___________ ;
(2)反应后溶液中FeCl2的物质的量浓度___________ 。
(1)混合粉末中铜的质量
(2)反应后溶液中FeCl2的物质的量浓度
您最近一年使用:0次
解题方法
6 . 向铁和氧化铁的混合物中加入500mL0.20mol·L-1稀盐酸后恰好完全反应,得到只含一种金属离子的浅绿色溶液,并收集到448mL氢气(标准状况下测定)。回答下列问题;
(1)反应后溶液中的溶质为_______ (填写化学式)。
(2)反应后溶液中的溶质为_______ mol。
(3)原混合物中单质铁的质量为_______ g。
(1)反应后溶液中的溶质为
(2)反应后溶液中的溶质为
(3)原混合物中单质铁的质量为
您最近一年使用:0次
名校
7 . 向铁和氧化铁的固体混合物中加入500mL0.30mol·L-1稀盐酸后固体完全溶解,盐酸恰好完全反应,得到浅绿色溶液(只含一种金属阳离子),并收集到气体672mL(标准状况下测定),回答下列问题:
(1)实验室欲用浓度为10.0mol·L-1的浓盐酸配制500mL0.30mol·L-1的稀盐酸,则需要量取上述浓盐酸_______ mL。
(2)原混合物中氧化铁的质量为______ g。
(1)实验室欲用浓度为10.0mol·L-1的浓盐酸配制500mL0.30mol·L-1的稀盐酸,则需要量取上述浓盐酸
(2)原混合物中氧化铁的质量为
您最近一年使用:0次
8 . 称取8.00 g氧化铜和氧化铁固体混合物,加入100 mL2.00mol/L的硫酸充分溶解,往所得溶液中加11.2g铁粉,充分反应后,得固体的质量为6.08g。请计算:
(1)加入铁粉充分反应后,溶液中溶质的物质的量_______ 。
(2)固体混合物中氧化铜的质量_______ 。
(1)加入铁粉充分反应后,溶液中溶质的物质的量
(2)固体混合物中氧化铜的质量
您最近一年使用:0次
名校
解题方法
9 . 现有CuO和Fe2O3组成的混合物若干克,向其中加入一定浓度的硫酸溶液50.0mL,恰好完全反应。向反应后的溶液中不断加入铁粉,加入铁粉的质量与充分反应后剩余固体的质量关系如图所示。

试计算:
(1)固体混合物中CuO的质量分数为_______ %;
(2)硫酸溶液的物质的量浓度为_______ mol/L

试计算:
(1)固体混合物中CuO的质量分数为
(2)硫酸溶液的物质的量浓度为
您最近一年使用:0次
2021-01-30更新
|
364次组卷
|
5卷引用:浙江省嘉兴市2020-2021学年高一上学期期末测试化学试题
浙江省嘉兴市2020-2021学年高一上学期期末测试化学试题(已下线)【浙江新东方】在线化学60高一下(已下线)【浙江新东方】在线化学63高一下(已下线)【浙江新东方】在线化学52高一上浙江省湖州市安吉县高级中学等2021-2022学年高一下学期返校联考化学试题
解题方法
10 . 向200mLFeCl3与HCl的混合溶液中,分别加入一定量成分均匀的Fe、Cu混合固体,充分反应后剩余固体的质量及放出气体的体积(标准状况下测得)如下表所示。
试计算:
(1)原混合液中c(Cl-)=____ 。
(2)混合固体中n(Fe):n(Cu)=____ 。
| 加入固体质量/g | 9.00 | 18.0 | 27.0 |
| 剩余固体质量/g | 3.20 | 9.60 | 15.8 |
| 放出气体体积/L | 0 | 1.12 | 2.24 |
试计算:
(1)原混合液中c(Cl-)=
(2)混合固体中n(Fe):n(Cu)=
您最近一年使用:0次
2020-05-06更新
|
738次组卷
|
2卷引用:浙江省2020届高三选考模拟卷化学试题(一)



