解题方法
1 . “孤蓬自振”学习小组向一定质量的Fe、FeO、Fe2O3的混合物中,加入100mL1.0mol/L的盐酸,恰好使混合物完全溶解并放出约224mL(标准状况)气体,溶液体积仍为100mL,所得溶液中滴加几滴KSCN溶液,溶液未显红色。请回答:
(1)加盐酸后所得溶液的溶质是______ (填化学式),物质的量浓度是______ mol/L。
(2)若用足量的CO在高温下还原相同质量的该混合物,最多能得到单质铁的质量是______ g。
(3)该混合物中铁、氧两种元素的粒子个数比N(Fe):N(O)=______ 。
(1)加盐酸后所得溶液的溶质是
(2)若用足量的CO在高温下还原相同质量的该混合物,最多能得到单质铁的质量是
(3)该混合物中铁、氧两种元素的粒子个数比N(Fe):N(O)=
您最近半年使用:0次
名校
解题方法
2 . 某稀硫酸和稀硝酸混合溶液100 mL,逐渐加入铁粉,产生气体的量随铁粉加入量的变化如图所示,求原混合溶液 和
和 的浓度
的浓度___________ 。(需在答题纸上写出计算过程)

 和
和 的浓度
的浓度
您最近半年使用:0次
3 . 称取6.00g氧化铜和氧化铁固体混合物,加入75.0mL2.00mol/L的硫酸充分溶解,往所得溶液中加入8.40g铁粉,充分反应后,得固体的质量为4.56g。请计算:
(1)加入的铁粉的物质的量为___________ mol。
(2)加入铁粉充分反应后,溶液中溶质为___________ ,其物质的量浓度为___________ mol/L(不考虑体积变化)。
(3)固体混合物中氧化铜的质量百分比为___________ 。
(1)加入的铁粉的物质的量为
(2)加入铁粉充分反应后,溶液中溶质为
(3)固体混合物中氧化铜的质量百分比为
您最近半年使用:0次
22-23高一下·浙江·期中
4 . 将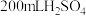 和
和 的混合溶液分成两等份。向其中一份中加入足量铁粉,充分反应后测的固体质量减少
的混合溶液分成两等份。向其中一份中加入足量铁粉,充分反应后测的固体质量减少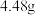 ;向另一份中加入足量
;向另一份中加入足量 溶液,经过滤、洗涤、干燥、称量,得到
溶液,经过滤、洗涤、干燥、称量,得到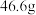 白色沉淀。请计算:
白色沉淀。请计算:
(1)其中一份溶液中加入足量的铁粉发生的反应有两个,写出对应的离子方程式:①___________ 、②___________ 。
(2)原溶液中
___________  ;
;
(3)原溶液中 和
和 的物质的量浓度之比为
的物质的量浓度之比为___________ 。
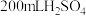 和
和 的混合溶液分成两等份。向其中一份中加入足量铁粉,充分反应后测的固体质量减少
的混合溶液分成两等份。向其中一份中加入足量铁粉,充分反应后测的固体质量减少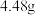 ;向另一份中加入足量
;向另一份中加入足量 溶液,经过滤、洗涤、干燥、称量,得到
溶液,经过滤、洗涤、干燥、称量,得到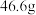 白色沉淀。请计算:
白色沉淀。请计算:(1)其中一份溶液中加入足量的铁粉发生的反应有两个,写出对应的离子方程式:①
(2)原溶液中

 ;
;(3)原溶液中
 和
和 的物质的量浓度之比为
的物质的量浓度之比为
您最近半年使用:0次
23-24高二上·浙江杭州·期末
5 . 将2.88gCu与Fe2O3的混合物加入40.0 mL2.00 mol/L的稀硫酸中,充分反应后剩余固体的质量为0.640 g。继续往溶液中加入一定质量的铁粉,溶液质量增加了1.54 g,请计算:
(1)混合物中Cu与Fe2O3物质的量之比为_______ 。
(2)继续加入铁粉的质量为_______ 。
(1)混合物中Cu与Fe2O3物质的量之比为
(2)继续加入铁粉的质量为
您最近半年使用:0次
解题方法
6 . (Ⅰ)把15.6gNa2O2放入100mL水中,充分反应后,计算:
(1)生成O2在标准状况的体积___________ mL;
(2)反应后所得NaOH的物质的量浓度___________ 。(反应前后溶液体积变化忽略不计)。
(Ⅱ)把含有氧化铁的铁片投入到足量的稀硫酸中,直到铁片完全溶解,经检验该溶液中无Fe3+,且生成的Fe2+与反应生成的H2的物质的量之比为4:1。
(3)检验该溶液中无Fe3+的方法及现象____________ 。
(4)则原混合物中Fe2O3与Fe的物质的量之比为___________ 。
(5)若原混合物中铁元素的总物质的量为6mol,则反应中生成H2的为_______ L(标准状况)。
(1)生成O2在标准状况的体积
(2)反应后所得NaOH的物质的量浓度
(Ⅱ)把含有氧化铁的铁片投入到足量的稀硫酸中,直到铁片完全溶解,经检验该溶液中无Fe3+,且生成的Fe2+与反应生成的H2的物质的量之比为4:1。
(3)检验该溶液中无Fe3+的方法及现象
(4)则原混合物中Fe2O3与Fe的物质的量之比为
(5)若原混合物中铁元素的总物质的量为6mol,则反应中生成H2的为
您最近半年使用:0次
解题方法
7 . 有一稀硫酸和硝酸铁的混合溶液,向其中加入铁粉,溶液中的Fe2+浓度如图所示(不考虑溶液体积的变化):
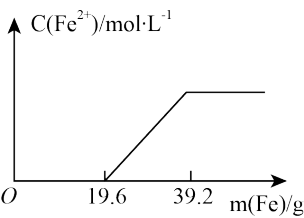
溶液中H2SO4与Fe(NO3)3的物质的量之比为_______

溶液中H2SO4与Fe(NO3)3的物质的量之比为
您最近半年使用:0次
8 . 有硫酸、硫酸亚铁、硫酸铁的混合溶液100 mL,已知溶液中各阳离子的物质的量浓度相等,SO 的物质的量浓度为3.0 mol·L−1。请计算:
的物质的量浓度为3.0 mol·L−1。请计算:
(1)SO 的物质的量为
的物质的量为_______ mol。
(2)理论上此溶液最多可溶解铁粉的质量为_______ g。
 的物质的量浓度为3.0 mol·L−1。请计算:
的物质的量浓度为3.0 mol·L−1。请计算:(1)SO
 的物质的量为
的物质的量为(2)理论上此溶液最多可溶解铁粉的质量为
您最近半年使用:0次
名校
9 . 完成下面有关计算,并在空白处填写结果。
(1)若将0.6mol钠、铁、铝分别投入100mL1mol·L-1盐酸中,在标准状况下,产生氢气的体积之比是___ 。
(2)一定量的苏打和小苏打固体分别与足量的稀盐酸反应,若产生的气体体积在标况下均为33.6L,则二者消耗HCl的物质的量之比为___ ,需要二者的固体质量之比为___ 。
(3)将6g铁粉加入200mLFe2(SO4)3和CuSO4的混合溶液中,充分反应得到200mL0.5mol/LFeSO4溶液和5.2g固体沉淀物。则反应后生成铜的质量为___ ,原Fe2(SO4)3溶液的物质的量浓度为____ 。
(1)若将0.6mol钠、铁、铝分别投入100mL1mol·L-1盐酸中,在标准状况下,产生氢气的体积之比是
(2)一定量的苏打和小苏打固体分别与足量的稀盐酸反应,若产生的气体体积在标况下均为33.6L,则二者消耗HCl的物质的量之比为
(3)将6g铁粉加入200mLFe2(SO4)3和CuSO4的混合溶液中,充分反应得到200mL0.5mol/LFeSO4溶液和5.2g固体沉淀物。则反应后生成铜的质量为
您最近半年使用:0次
名校
10 . 印刷电路板是由高分子材料和铜箔复合而成,刻制印刷电路时,要用FeCl3溶液作为“腐蚀液”,生成CuCl2和FeCl2。现有一包铁粉和铜粉的混合粉末17.6g,使其完全溶解恰好需要200mL3.0mol/L的FeCl3溶液。假设溶液反应前后体积不变,试计算:(注意:无计算过程不给分)
(1)混合粉末中铜的质量___________ ;
(2)反应后溶液中FeCl2的物质的量浓度___________ 。
(1)混合粉末中铜的质量
(2)反应后溶液中FeCl2的物质的量浓度
您最近半年使用:0次



