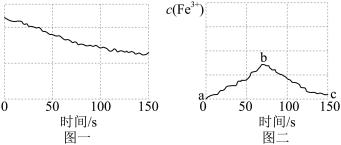
1 . 利用传感器和信息处理终端对氯水的实验进行数据采集与分析得到以下图像,图一表示氯水长时间放置在空气中,随着反应进行某种量的变化;图二表示将过量铁粉加入氯水中, 浓度的变化曲线。下列说法错误的是
浓度的变化曲线。下列说法错误的是
 浓度的变化曲线。下列说法错误的是
浓度的变化曲线。下列说法错误的是
A.图一可表示: 随光照时间的变化曲线 随光照时间的变化曲线 |
B.图一可表示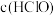 随光照时间的变化曲线 随光照时间的变化曲线 |
C.图二ab段测得有 ,可能是Fe与 ,可能是Fe与 反应生成的 反应生成的 |
D.图二bc段表明溶液中的反应以 为主 为主 |
您最近一年使用:0次
2 . 向400 mL稀硫酸和稀硝酸的混合溶液中逐渐加入铁粉,产生气体的量随铁粉质量的变化如图所示(已知硝酸只被还原为NO气体)。下列说法错误的是
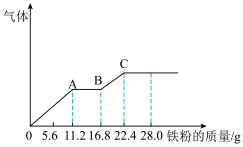

| A.A点溶液中的溶质为Fe2(SO4)3和H2SO4 |
| B.AB段的反应为Fe+2Fe3+ = 3Fe2+ |
| C.反应中生成的n(NO):n(H2) = 1:2 |
| D.最终溶液中溶质的物质的量浓度约为1.25 mol·L-1 |
您最近一年使用:0次
名校
解题方法
3 . 常温时,将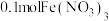 和
和 溶于水得2L混合溶液,然后向该溶液中投入mg铁粉,铁粉充分反应后(固体无剩余),该过程中收集到的气体的体积为VL(已换算成标准状况下的体积),往溶液中滴加
溶于水得2L混合溶液,然后向该溶液中投入mg铁粉,铁粉充分反应后(固体无剩余),该过程中收集到的气体的体积为VL(已换算成标准状况下的体积),往溶液中滴加 溶液,溶液不变红。下列有关说法正确的是
溶液,溶液不变红。下列有关说法正确的是
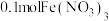 和
和 溶于水得2L混合溶液,然后向该溶液中投入mg铁粉,铁粉充分反应后(固体无剩余),该过程中收集到的气体的体积为VL(已换算成标准状况下的体积),往溶液中滴加
溶于水得2L混合溶液,然后向该溶液中投入mg铁粉,铁粉充分反应后(固体无剩余),该过程中收集到的气体的体积为VL(已换算成标准状况下的体积),往溶液中滴加 溶液,溶液不变红。下列有关说法正确的是
溶液,溶液不变红。下列有关说法正确的是A.由于氧化性 ,因此首先发生的反应是 ,因此首先发生的反应是 |
| B.V可能为11.2 |
C.在铁粉充分反应后的溶液中,铁元素以 和 和 的形式存在 的形式存在 |
D.反应过程中溶液的质量一直在增大,且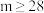 |
您最近一年使用:0次
解题方法
4 . 部分含铁物质的分类与相应化合价关系如图所示。下列说法不正确的是
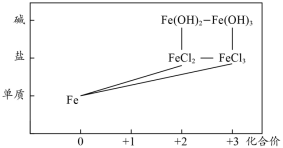

| A.Fe与盐酸反应生成FeCl3 |
| B.实验室制Fe(OH)3的胶体是将FeCl3加入浓NaOH溶液中 |
| C.FeCl2既有氧化性,又有还原性 |
| D.一定条件下存在FeCl2→Fe(OH)2→Fe(OH)3→FeCl3→FeCl2的转化关系 |
您最近一年使用:0次
2022-01-18更新
|
139次组卷
|
2卷引用:湖南省永州市2021-2022学年高一上学期期末质量监测化学试题
名校
解题方法
5 . 同一还原剂与多种氧化剂在一起时,先与氧化性强的粒子反应,待强的反应完后,再与氧化性弱的反应,称为反应先后规律。已知2Fe3++Fe=3Fe2+,且氧化性:Fe3+>Cu2+,在溶有Fe2(SO4)3和CuSO4的溶液中加入铁粉,下列说法中正确的是
| A.若铁粉有剩余,则不溶物中一定有铜 |
| B.若铁粉有剩余,则溶液中的金属阳离子有Fe2+和Cu2+ |
| C.若铁粉无剩余,且溶液中有Cu2+,则溶液中一定无Fe3+ |
| D.若铁粉无剩余,且溶液中无Cu2+,则溶液中一定有Fe2+,一定无Fe3+ |
您最近一年使用:0次
2021-10-15更新
|
401次组卷
|
2卷引用:湖南省长沙市第一中学2021-2022高一上学期第一次月考化学试卷
6 . 为将含有FeCl3、FeCl2、CuCl2的废液中的Cu2+还原回收,某同学在含有ag铁粉的容器中加入该废液,探究了加入废液体积与完全反应后体系中固体质量的关系,部分实验数据如表所示。已知:废液中c(Cu2+)=0.7mol•L-1;当废液体积为0.5L时,废液中Fe3+和Cu2+与铁粉恰好完全反应。
下列说法错误的是
| 废液体积/L | 0.5 | 1 | 2 | 3 | ≥4 |
| 固体质量/g | a | 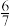 a a | 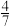 a a | 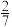 a a | 0 |
| A.当铁粉与0.25L废液反应完全后,固体成分为Fe与Cu |
| B.当铁粉与1L废液反应完全后,再加入废液时发生的离子反应为Fe+2Fe3+=3Fe2+ |
| C.废液中c(Fe3+)=0.4mol•L-1 |
| D.要将1L废液中的Cu2+全部还原,则至少需要铁粉44.8g |
您最近一年使用:0次
名校
解题方法
7 . 向100mL Fe2(SO4)3和CuSO4的混合溶液中逐渐加入铁粉,充分反应后溶液中固体剩余物的质量与加入铁粉的质量如图所示。忽略溶液体积的变化,下列说法不正确的是


| A.a点时溶液中阳离子有Cu2+、Fe2+、Fe3+ |
| B.b点时溶液中发生的反应为:Fe+Cu2+=Cu+Fe2+ |
| C.c点时溶液中溶质的物质的量浓度无法计算 |
| D.原溶液中Fe2(SO4)3和CuSO4的物质的量浓度之比为1∶1 |
您最近一年使用:0次
2021-01-25更新
|
681次组卷
|
3卷引用:江苏省无锡市锡山高级中学2020-2021学年高一上学期期末考试化学试题



