解题方法
1 . 富脂食品密封保存往往需要在包装袋内装一小包脱氧剂(有效成分是还原铁粉),某小组为探究脱氧剂中铁粉是否变质,取少量样品溶于稀盐酸,再进行下列实验,下列有关实验现象和结论的说法错误的是
| A.若加盐酸时有气体产生,不能证明脱氧剂未变质 |
| B.若滴加KSCN溶液,无明显变化,再滴加氯水显血红色,则证明脱氧剂未变质 |
| C.若滴加KSCN溶液,溶液显血红色,则证明脱氧剂已变质 |
| D.若加入铜粉充分反应后,溶液呈蓝色,则证明脱氧剂已变质 |
您最近一年使用:0次
2 . 下列说法正确的是
| A.FeCl3溶液需存放在加有少量铁粉的试剂瓶中,防止变质 |
| B.食盐水中Ca2+、SO42-等杂质的去除,应先加Na2CO3溶液,后加BaCl2溶液 |
| C.用四氯化碳来萃取碘水中的I2,有机层应从分液漏斗的下端放出 |
| D.用BaCl2溶液来检验暴露在空气中的Na2SO3样品是否变质 |
您最近一年使用:0次
2016-12-09更新
|
356次组卷
|
4卷引用:2015-2016学年江苏省宿迁市高一上学期期末考试化学试卷
名校
解题方法
3 . 回答下列问题:
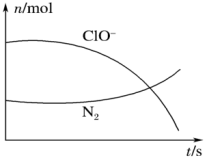
(1)某反应体系中有H2O、ClO-、NH 、OH-、N2、Cl-等微粒,其中N2、ClO-的物质的量随时间变化的曲线如图所示,写出该反应的离子方程式
、OH-、N2、Cl-等微粒,其中N2、ClO-的物质的量随时间变化的曲线如图所示,写出该反应的离子方程式_______ ,消耗1 mol还原剂,转移电子数为_______ 。
(2)Fe2+的还原性较强,实验室的氯化亚铁溶液常因氧化而变质,除去杂质的方法是_______ ,相关反应的离子方程式是_______ 。
(3)根据反应8NH3+3Cl2=6NH4Cl+N2,当有68 g NH3参加反应时,被氧化的物质为_______ ,生成的还原产物的质量为_______ g。
(4)K2FeO4(铁元素为+6价)可用作水处理剂,它可由以下反应制得,请配平下列离子方程式_____ 。
_______Cl2 + _______ Fe(OH)3+_______ OH- = _______ FeO + _______ Cl- +_______ H2O
+ _______ Cl- +_______ H2O
(1)某反应体系中有H2O、ClO-、NH
 、OH-、N2、Cl-等微粒,其中N2、ClO-的物质的量随时间变化的曲线如图所示,写出该反应的离子方程式
、OH-、N2、Cl-等微粒,其中N2、ClO-的物质的量随时间变化的曲线如图所示,写出该反应的离子方程式
(2)Fe2+的还原性较强,实验室的氯化亚铁溶液常因氧化而变质,除去杂质的方法是
(3)根据反应8NH3+3Cl2=6NH4Cl+N2,当有68 g NH3参加反应时,被氧化的物质为
(4)K2FeO4(铁元素为+6价)可用作水处理剂,它可由以下反应制得,请配平下列离子方程式
_______Cl2 + _______ Fe(OH)3+_______ OH- = _______ FeO
 + _______ Cl- +_______ H2O
+ _______ Cl- +_______ H2O
您最近一年使用:0次
名校
解题方法
4 . 5.76g某部分氧化的Fe、Cu合金样品(氧化产物为 、CuO),经如下处理,下列说法正确的是
、CuO),经如下处理,下列说法正确的是

 、CuO),经如下处理,下列说法正确的是
、CuO),经如下处理,下列说法正确的是
| A.V=448 |
| B.样品中Fe元素的质量为2.14g |
| C.未氧化前Fe元素的质量分数约为38.89% |
| D.样品中CuO的质量为3.52g |
您最近一年使用:0次
名校
5 . 部分被氧化的Fe-Cu合金样品(氧化产物为Fe2O3、CuO)共5.76g,经如下处理:
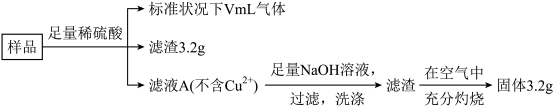
已知:氯化铁溶液用于腐蚀印刷电路铜板的离子反应为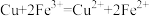 。下列说法正确的是
。下列说法正确的是
①滤液A中的阳离子为Fe2+、Fe3+、H+
②样品中氧原子的物质的量为0.02mol
③溶解样品的过程中消耗H2SO4的总物质的量为0.04mol④V=224⑤V=448

已知:氯化铁溶液用于腐蚀印刷电路铜板的离子反应为
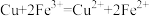 。下列说法正确的是
。下列说法正确的是①滤液A中的阳离子为Fe2+、Fe3+、H+
②样品中氧原子的物质的量为0.02mol
③溶解样品的过程中消耗H2SO4的总物质的量为0.04mol④V=224⑤V=448
| A.①③④ | B.②③④ | C.②③⑤ | D.①②⑤ |
您最近一年使用:0次
名校
解题方法
6 . 部分氧化的Fe—Cu合金样品(氧化产物为Fe2O3、CuO)共5.76g,经如图处理:

下列说法不正确的是

下列说法不正确的是
| A.样品中Fe元素的质量为2.24 g |
| B.V<896 |
| C.参与反应的n(H2SO4) = 0.04 mol |
| D.滤液A中的阳离子为Fe2+、Cu2+、H+ |
您最近一年使用:0次
名校
解题方法
7 . 部分氧化的Fe—Cu合金样品(氧化产物为Fe2O3、CuO)共5.76g,经如图处理:

下列说法不正确的是

下列说法不正确的是
| A.滤液A中的阳离子为Fe2+、Cu2+、H+ | B.样品中Fe元素的质量为2.24g |
| C.参与反应的n(H2SO4)=0.04mol | D.V<896 |
您最近一年使用:0次
2022-03-22更新
|
640次组卷
|
3卷引用:湖南省长沙市湖南师范大学附属中学2021-2022学年高一上学期期末考试化学试题
8 . 部分氧化的Fe-Cu合金样品(氧化产物为Fe2O3、CuO)共5.76 g,经如下处理:
下列说法正确的是

下列说法正确的是
| A.V=44.8 |
| B.原样品中铁元素的质量分数约为38.89% |
| C.滤液A中的阳离子为Fe2+、Fe3+、H+ |
| D.样品中CuO的质量为4.0 g |
您最近一年使用:0次
2016-05-04更新
|
332次组卷
|
4卷引用:2016届内蒙古赤峰市宁城县高三下学期第三次统一模拟考试化学试卷
2016届内蒙古赤峰市宁城县高三下学期第三次统一模拟考试化学试卷2017届辽宁省东北育才学校高三上学期第一次模拟化学试卷2017届辽宁省沈阳东北育才学校高三上模拟一化学试卷(已下线)2019年1月20日 《每日一题》 高考二轮复习-每周一测
9 . 有三份不同质量的铁粉样品①②③,甲、乙、丙三位同学各取一份样品分别与含有0.8molHNO3的稀硝酸反应,反应后硝酸和铁均无剩余,且硝酸的还原产物只有NO。据此回答下列问题:
(1)甲取样品①,反应后的溶液中铁只以 Fe3+离子的形式存在,则样品①的质量为_________g。
(2)乙取样品②,反应后的溶液中既含有Fe3+、又含有Fe2+离子,则样品②的质量 (设为ag)范围是________。
(3)丙取样品③,将其慢慢加入到稀硝酸中,并不断搅拌,反应过程中溶液里Fe3+、Fe2+、NO3⁻三种离子中的一种离子的物质的量的变化曲线如下图所示,则该曲线表示的是________物质的量变化的曲线,请你在此图中再画出另外两种离子的物质的量的变化曲线。

(1)甲取样品①,反应后的溶液中铁只以 Fe3+离子的形式存在,则样品①的质量为_________g。
(2)乙取样品②,反应后的溶液中既含有Fe3+、又含有Fe2+离子,则样品②的质量 (设为ag)范围是________。
(3)丙取样品③,将其慢慢加入到稀硝酸中,并不断搅拌,反应过程中溶液里Fe3+、Fe2+、NO3⁻三种离子中的一种离子的物质的量的变化曲线如下图所示,则该曲线表示的是________物质的量变化的曲线,请你在此图中再画出另外两种离子的物质的量的变化曲线。

您最近一年使用:0次



