名校
1 . 某化学兴趣小组利用废铁屑(含少量 )制备还原性铁粉,从而达到资源回收利用的目的,制备流程如图所示。
)制备还原性铁粉,从而达到资源回收利用的目的,制备流程如图所示。

请回答下列问题:
(1)“酸溶”时,搅拌的目的是_______ 。
(2)“操作Y”为_______ (填操作名称),经过“操作Y”得到了滤渣 ,则物质X可用于除去过量的稀硫酸和防止
,则物质X可用于除去过量的稀硫酸和防止 被氧化,可选择
被氧化,可选择_______ (填试剂名称),“转化2”发生反应的离子方程式为_______ 。
(3)“洗涤”时,能证明滤渣洗涤干净的操作及现象为_______ 。
(4)麦片中常添加微量还原性铁粉,用于补充入体所需的铁元素,这些铁粉在胃酸(主要成分为盐酸)的作用下发生反应变成人体容易吸收的铁元素,发生反应的化学方程式为_______ ;人体补铁时,同时服用维生素C能促进亚铁离子被吸收,说明维生素C具有_______ (填“氧化性”或“还原性”)。
 )制备还原性铁粉,从而达到资源回收利用的目的,制备流程如图所示。
)制备还原性铁粉,从而达到资源回收利用的目的,制备流程如图所示。
请回答下列问题:
(1)“酸溶”时,搅拌的目的是
(2)“操作Y”为
 ,则物质X可用于除去过量的稀硫酸和防止
,则物质X可用于除去过量的稀硫酸和防止 被氧化,可选择
被氧化,可选择(3)“洗涤”时,能证明滤渣洗涤干净的操作及现象为
(4)麦片中常添加微量还原性铁粉,用于补充入体所需的铁元素,这些铁粉在胃酸(主要成分为盐酸)的作用下发生反应变成人体容易吸收的铁元素,发生反应的化学方程式为
您最近一年使用:0次
2022-12-07更新
|
229次组卷
|
4卷引用:四川省成都市四校2022-2023学年高一上学期12月联考化学试题
四川省成都市四校2022-2023学年高一上学期12月联考化学试题四川省眉山市彭山区第一中学2022-2023学年高一上学期第二次模拟选科调考化学试题云南省楚雄彝族自治州2022-2023学年高一上学期期末教育学业质量监测化学试题(已下线)第13讲 铁和铁的氧化物-【暑假自学课】2023年新高一化学暑假精品课(人教版2019必修第一册)
解题方法
2 . 下列实验的“操作和现象”与“推测或结论”对应关系正确的是
选项 | 操作和现象 | 推测或结论 |
A | 向H2O2溶液中加入几滴FeCl3溶液,溶液中产生气泡 | 发生的离子反应为: |
B | 用铁丝蘸取少量某溶液进行焰色反应,火焰呈黄色 | 该溶液含有钠盐 |
C | 向Al与Fe2O3反应后的固体产物中先加稀硫酸溶解,再加入几滴KSCN溶液,溶液不变红 | 无法证明反应后固体产物中是否含有Fe2O3 |
D | 向无水乙醇中加入浓硫酸,加热至170℃,将产生的气体通入酸性高锰酸钾溶液,红色褪去 | 使溶液褪色的气体是乙烯 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
3 . 印刷电路的废腐蚀液含有大量CuCl2、FeCl2和FeCl3,任意排放将导致环境污染及资源的浪费。可从该废液中回收铜,并将铁的化合物全部转化为FeCl3溶液,作为腐蚀液原料循环使用。测得某废腐蚀液中含CuCl2 1.5 mol/L,FeCl2 3.0 mol/L,FeCl3 1.0 mol/L,HCl 3.0 mol/L。取废腐蚀液200 mL按如下流程在实验室进行实验:

回答下列问题:
(1)取少量废腐蚀液于试管中,滴入1~2滴KSCN溶液,若溶液显_______ (填“红色”或“蓝色”、“紫色”),证明废液含有FeCl3。
(2)上述方法获得的铜粉中含有杂质,除杂所需试剂是_______ (填化学式)。
(3)操作Ⅰ是_______ ,该操作需用到的玻璃仪器有烧杯、普通漏斗和_______ 。
(4)FeCl2溶液中通入氯气,发生反应的离子方程式为_______ 。
(5)已知氧化性:Fe3+>Cu2+ >H+>Fe2+;往上述200 mL废腐蚀液中加入20g铁粉,边加边搅拌,是否有氢气产生_______ (填“是”、“否”)。

回答下列问题:
(1)取少量废腐蚀液于试管中,滴入1~2滴KSCN溶液,若溶液显
(2)上述方法获得的铜粉中含有杂质,除杂所需试剂是
(3)操作Ⅰ是
(4)FeCl2溶液中通入氯气,发生反应的离子方程式为
(5)已知氧化性:Fe3+>Cu2+ >H+>Fe2+;往上述200 mL废腐蚀液中加入20g铁粉,边加边搅拌,是否有氢气产生
您最近一年使用:0次
4 . 下列方案设计、现象和结论都正确的是
| 目的 | 方案设计 | 现象和结论 | |
| A | 检验氯气输送管道是否漏气 | 在管道边喷洒浓氨水进行检验 | 若有氯气泄漏,则会在泄漏处附近产生白烟 |
| B | 探究金属铁在氯气中燃烧所得固体粉末的成分 | 取少量固体粉末加入5-7mL蒸馏水,振荡,迅速滴入5滴15%KSCN溶液 | 若溶液无红色,则固体粉末不为FeCl3 |
| C | 验证H2S与HI的酸性强弱 | 将AgI固体加入水中,再向其中滴入几滴H2S溶液 | 固体由黄色变为黑色,说明有Ag2S沉淀和HI生成,证明H2S酸性更强 |
| D | 验证NO2是一种酸性氧化物 | 将NO2通入蒸馏水中,检测反应所得溶液的pH | 红棕色气体溶于水得无色溶液,所得溶液的pH小于7,同时有无色气体产生,说明反应生成了HNO3和NO,由此证明NO2是酸性氧化物 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
5 . 某工厂废水中含大量 和少量的
和少量的 、
、 、
、 ,为减少污染变废为宝,实验小组设计了如图方案(其中每步加入试剂均过量):
,为减少污染变废为宝,实验小组设计了如图方案(其中每步加入试剂均过量):

(1)“试剂Ⅱ”为_______ ,与“试剂Ⅰ”反应的离子有_______
(2)“红褐色沉淀”为_______ ,“ ”的作用是
”的作用是_______
(3)“试剂Ⅲ”是沉淀“溶液B”中 ,证明“溶液B”中
,证明“溶液B”中 已经完全沉淀的试剂为
已经完全沉淀的试剂为_______ 。
(4)“溶液B”中残留 与“试剂Ⅲ”反应的化学方程式为
与“试剂Ⅲ”反应的化学方程式为_______ 。
(5)“溶液C”在空气中晾晒一段时间后,加盐酸调成弱酸性,蒸发可得工业食盐,但加盐酸时有少量气泡逸出,经检验为 ,则“溶液C”中碳酸盐形成的可能离子反应为(写出一个即可)
,则“溶液C”中碳酸盐形成的可能离子反应为(写出一个即可)_______
 和少量的
和少量的 、
、 、
、 ,为减少污染变废为宝,实验小组设计了如图方案(其中每步加入试剂均过量):
,为减少污染变废为宝,实验小组设计了如图方案(其中每步加入试剂均过量):
(1)“试剂Ⅱ”为
(2)“红褐色沉淀”为
 ”的作用是
”的作用是(3)“试剂Ⅲ”是沉淀“溶液B”中
 ,证明“溶液B”中
,证明“溶液B”中 已经完全沉淀的试剂为
已经完全沉淀的试剂为(4)“溶液B”中残留
 与“试剂Ⅲ”反应的化学方程式为
与“试剂Ⅲ”反应的化学方程式为(5)“溶液C”在空气中晾晒一段时间后,加盐酸调成弱酸性,蒸发可得工业食盐,但加盐酸时有少量气泡逸出,经检验为
 ,则“溶液C”中碳酸盐形成的可能离子反应为(写出一个即可)
,则“溶液C”中碳酸盐形成的可能离子反应为(写出一个即可)
您最近一年使用:0次
2022-01-17更新
|
697次组卷
|
2卷引用:四川省达州市2021-2022学年高一上学期期末监测化学试题
解题方法
6 . 电子工业常用FeCl3溶液腐蚀印刷电路板上的铜箔。某研究小组设计以下流程从腐蚀废液中回收铜,并重新获得FeCl3溶液。

(1)FeCl3溶液腐蚀铜箔的离子方程式为___ 。
(2)试剂①为___ (写化学式),试剂②需过量的原因是___ 。
(3)证明“滤液”中不含Fe3+的方法为___ 。
(4)“反应”步骤中的离子方程式为___ 。
(5)向沸水中加入1mol•L-1FeCl3溶液至液体呈透明的红褐色,该分散系具有的独特性质是___ (写出一条)。

(1)FeCl3溶液腐蚀铜箔的离子方程式为
(2)试剂①为
(3)证明“滤液”中不含Fe3+的方法为
(4)“反应”步骤中的离子方程式为
(5)向沸水中加入1mol•L-1FeCl3溶液至液体呈透明的红褐色,该分散系具有的独特性质是
您最近一年使用:0次
2021-01-28更新
|
190次组卷
|
2卷引用:四川省雅安市2021-2022学年高一上学期期末检测化学试题
解题方法
7 . 下列说法中不正确的是
| A.赤铁矿的主要成分与铁锈的主要成分相同 |
| B.Fe3O4可由单质直接化合而得到 |
| C.FeCl2、FeCl3、Fe(OH)3都可通过化合反应生成 |
| D.某溶液中滴加氯水,然后滴加KSCN溶液,溶液显红色,该溶液中一定含有Fe2+ |
您最近一年使用:0次
解题方法
8 . 下列指定物质之间的转化:
Fe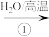

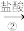 混合溶液
混合溶液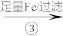
 溶液
溶液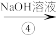

下列说法不正确 的是
Fe
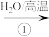

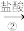 混合溶液
混合溶液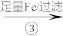
 溶液
溶液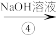

下列说法
| A.反应①属于置换反应 |
B.反应②所得混合溶液中 与 与 物质的量之比是1∶2 物质的量之比是1∶2 |
C.反应③的离子方程式为: |
D.利用反应④制备 时需要充分振荡反应液 时需要充分振荡反应液 |
您最近一年使用:0次
解题方法
9 . 下列有关金属及其化合物的说法不正确的是
| A.合金硬度比成分金属大是因为金属原子规则的层状排列被改变 |
B.金属镁性质活泼,制取镁粉时可将镁蒸气在保护气 中冷却 中冷却 |
C.将废铁屑加入 溶液中,可用于除去工业废气中的 溶液中,可用于除去工业废气中的 |
| D.熟石膏与水混合成糊状后能很快凝固,常用于制作模型和医疗石膏绷带 |
您最近一年使用:0次
名校
解题方法
10 . 工业废水中含有重铬酸根离子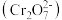 有毒,必须处理达标后才能排放。工业上常用绿矾
有毒,必须处理达标后才能排放。工业上常用绿矾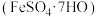 做处理剂,反应的离子方程式为:
做处理剂,反应的离子方程式为: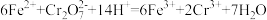 ,下列说法
,下列说法不正确 的是
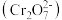 有毒,必须处理达标后才能排放。工业上常用绿矾
有毒,必须处理达标后才能排放。工业上常用绿矾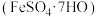 做处理剂,反应的离子方程式为:
做处理剂,反应的离子方程式为: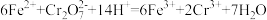 ,下列说法
,下列说法| A.将绿矾水溶液久置于空气中,滴加几滴KSCN溶液,溶液出现血红色 |
B.配制好的 溶液,为防止变质可向溶液中加入少量铁粉 溶液,为防止变质可向溶液中加入少量铁粉 |
C.每处理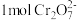 转移 转移 电子 电子 |
D.向 溶液中加入 溶液中加入 溶液一段时间后,沉淀会变成红褐色 溶液一段时间后,沉淀会变成红褐色 |
您最近一年使用:0次
2022-06-24更新
|
542次组卷
|
4卷引用:浙江省湖州市2021-2022学年高一下学期期末考试化学试题
浙江省湖州市2021-2022学年高一下学期期末考试化学试题浙江省舟山市普陀中学2023届高三返校考试化学试题(已下线)易错点06 铁及其化合物-备战2023年高考化学考试易错题云南省昭通市等4地2023-2024学年高二上学期12月月考化学试题




