名校
解题方法
1 . 推理是学习化学的重要方法,下列推理结果合理的是
A. 溶于盐酸生成 溶于盐酸生成 和 和 ,则 ,则 溶于氢碘酸生成 溶于氢碘酸生成 和 和 |
B. 的溶解度大于 的溶解度大于 ,推测 ,推测 的溶解度大于 的溶解度大于 |
C. 的与 的与 反应生成 反应生成 ,推测 ,推测 与 与 反应生成 反应生成 |
| D.常温下Na能与水反应,推测常温下Ca也能与水反应 |
您最近一年使用:0次
2023-12-05更新
|
279次组卷
|
3卷引用:河北省石家庄二中实验学校2023-2024学年高一上学期12月月考化学试题
名校
解题方法
2 . 13.6gFe和Fe2O3的混合物,加入150mL足量的稀硫酸,在标准状况下收集到1.12LH2,向反应后的溶液中滴入KSCN溶液不变红。为中和过量的H2SO4,并使Fe元素恰好全部转化为Fe(OH)2沉淀,恰好消耗了200mL3mol/L的NaOH溶液(忽略溶液体积变化)。下列说法正确的是
| A.混合物中Fe2O3的物质的量为0.1mol |
| B.混合物中Fe的物质的量为0.5mol |
| C.原硫酸的浓度为2mol/L |
| D.与固体粉末反应的硫酸的物质的量为0.6mol |
您最近一年使用:0次
2023-03-13更新
|
378次组卷
|
3卷引用:河北省保定市唐县第一中学2022-2023学年高一下学期5月月考化学试题
名校
3 . 将一定质量的 和
和 混合固体粉末溶于
混合固体粉末溶于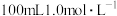 稀盐酸,恰好完全反应,生成标准状况下
稀盐酸,恰好完全反应,生成标准状况下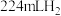 ,向反应后的溶液中加入
,向反应后的溶液中加入 溶液,溶液颜色无明显变化。则下列说法正确的是
溶液,溶液颜色无明显变化。则下列说法正确的是
A.反应后溶液中含有 |
B. 与稀盐酸发生氧化还原反应 与稀盐酸发生氧化还原反应 |
C.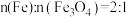 |
D.混合固体中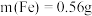 |
您最近一年使用:0次
2023-02-18更新
|
163次组卷
|
6卷引用:河北省郑口中学2023-2024学年高一上学期第四次质量检测化学试卷
4 . 下列各组物质中,物质之间通过一步反应能实现如图所示转化的是


| 选项 | a | b | c |
| A | Fe | Fe2O3 | Fe(OH)3 |
| B | Na | Na2O2 | Na2CO3 |
| C | Cl2 | HClO | HCl |
| D | Na | NaOH | NaHCO3 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-01-31更新
|
183次组卷
|
3卷引用:河北省石家庄市卓越中学2022-2023学年高一上学期期末考试化学试题
名校
解题方法
5 . 铁及其化合物与生产、生活息息相关。回答下列问题:
(1) 易被人体吸收,医生建议在服用该补铁剂时,同时服用维生素C.维生素C的作用是
易被人体吸收,医生建议在服用该补铁剂时,同时服用维生素C.维生素C的作用是_______ 。
(2)印刷电路板的制作原理是用足量的 溶液腐蚀覆铜板上不需要的铜箔。写出上述反应的化学方程式:
溶液腐蚀覆铜板上不需要的铜箔。写出上述反应的化学方程式:_______ 。
(3)生铁是通过高炉冶炼而得到的,以赤铁矿为例用 将其还原的化学方程式为
将其还原的化学方程式为_______ 。
(4)某废料铁泥的主要成分为 、
、 、
、 和杂质(杂质不与硫酸反应)。现取
和杂质(杂质不与硫酸反应)。现取 废料铁泥提取
废料铁泥提取 ,设计实验流程如下:
,设计实验流程如下:

①分离溶液A和沉淀C的操作中使用到的玻璃仪器有烧杯、_______ 、_______ 。
②能检验溶液A中含有 的试剂是
的试剂是_______ (填字母)。
A.铁粉 B.酸性 溶液 C.KSCN溶液
溶液 C.KSCN溶液
③步骤Ⅱ中发生反应的离子方程式为_______ 。
④若最终获得 ,则废料铁泥中铁元素的质量分数为
,则废料铁泥中铁元素的质量分数为_______ 。
(1)
 易被人体吸收,医生建议在服用该补铁剂时,同时服用维生素C.维生素C的作用是
易被人体吸收,医生建议在服用该补铁剂时,同时服用维生素C.维生素C的作用是(2)印刷电路板的制作原理是用足量的
 溶液腐蚀覆铜板上不需要的铜箔。写出上述反应的化学方程式:
溶液腐蚀覆铜板上不需要的铜箔。写出上述反应的化学方程式:(3)生铁是通过高炉冶炼而得到的,以赤铁矿为例用
 将其还原的化学方程式为
将其还原的化学方程式为(4)某废料铁泥的主要成分为
 、
、 、
、 和杂质(杂质不与硫酸反应)。现取
和杂质(杂质不与硫酸反应)。现取 废料铁泥提取
废料铁泥提取 ,设计实验流程如下:
,设计实验流程如下:
①分离溶液A和沉淀C的操作中使用到的玻璃仪器有烧杯、
②能检验溶液A中含有
 的试剂是
的试剂是A.铁粉 B.酸性
 溶液 C.KSCN溶液
溶液 C.KSCN溶液③步骤Ⅱ中发生反应的离子方程式为
④若最终获得
 ,则废料铁泥中铁元素的质量分数为
,则废料铁泥中铁元素的质量分数为
您最近一年使用:0次
2023-01-20更新
|
519次组卷
|
7卷引用:河北省保定市泽龙实验中学2022-2023学年高一下学期开学检测化学试题
解题方法
6 . 下列离子方程式正确的是
| A.氧化铁与盐酸反应:Fe2O3+6H+=2Fe2++3H2O |
| B.Fe与FeCl3溶液反应:Fe+Fe3+=2Fe2+ |
| C.Fe与盐酸反应:Fe+2H+=Fe2++H2↑ |
| D.Fe与CuSO4溶液反应:Fe+Cu2+=Fe3++Cu |
您最近一年使用:0次
7 . 结构决定性质,性质决定用途,下列对应关系错误的是
| A.铝的性质稳定,可以涂在暖气片表面防腐 |
| B.活性炭具有疏松多孔的结构,可用于制糖工业脱色 |
| C.稀盐酸能与金属氧化物反应,可以用于除铁锈 |
| D.石墨、金刚石的硬度不同,原因是碳原子排列方式不同 |
您最近一年使用:0次
名校
解题方法
8 . 在人类社会的发展进程中,金属起着重要的作用。请回答下列问题:
(1)人类最早使用的金属材料的主要成分是铜。下列有关铜元素的说法中,错误的是_______(填标号)。
(2)生铁中含有一种铁碳化合物X(Fe3C)。X在足量的空气中高温煅烧,生成有磁性的固体Y,将Y溶于过量盐酸后溶液中大量存在的阳离子是_______ (填离子符号)。
(3)铁及其化合物在生产生活中具有广泛应用。一定条件下,铁及其化合物之间发生相互转化。NaFeO2可完全溶于水且与水反应生成两种碱,写出发生反应的离子方程式:_______ 。
(4)某溶液中有Mg2+、Fe2+、Cu2+等离子,向其中加入过量的NaOH溶液后,过滤,将滤渣高温灼烧,并将灼烧后的固体投入过量的稀盐酸中,所得溶液与原溶液相比,溶液中大量减少的阳离子是_______ (填离子符号)。
(5)氧化铁是重要的工业颜料,用废铁屑制备它的流程如图:
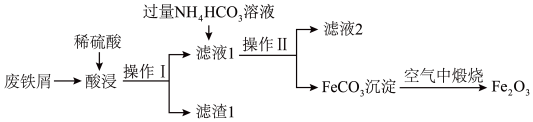
①完成“操作Ⅰ”所需要的玻璃仪器除烧杯外,还需要的是_______ 。
②加入稍过量NH4HCO3溶液时,不仅有沉淀生成,还有无色无味的气体生成,请写出生成FeCO3沉淀的离子方程式:_______ 。
③FeCO3在空气中加热反应生成Fe2O3时,氧化剂和还原剂的物质的量之比为_______ 。
(1)人类最早使用的金属材料的主要成分是铜。下列有关铜元素的说法中,错误的是_______(填标号)。
| A.青铜、不锈钢、硬铝都是合金 |
| B.铜表面易形成致密的氧化膜 |
| C.铜与O2反应可生成黑色的CuO |
D. 是一种混合物,加热后变为白色固体 是一种混合物,加热后变为白色固体 |
(3)铁及其化合物在生产生活中具有广泛应用。一定条件下,铁及其化合物之间发生相互转化。NaFeO2可完全溶于水且与水反应生成两种碱,写出发生反应的离子方程式:
(4)某溶液中有Mg2+、Fe2+、Cu2+等离子,向其中加入过量的NaOH溶液后,过滤,将滤渣高温灼烧,并将灼烧后的固体投入过量的稀盐酸中,所得溶液与原溶液相比,溶液中大量减少的阳离子是
(5)氧化铁是重要的工业颜料,用废铁屑制备它的流程如图:

①完成“操作Ⅰ”所需要的玻璃仪器除烧杯外,还需要的是
②加入稍过量NH4HCO3溶液时,不仅有沉淀生成,还有无色无味的气体生成,请写出生成FeCO3沉淀的离子方程式:
③FeCO3在空气中加热反应生成Fe2O3时,氧化剂和还原剂的物质的量之比为
您最近一年使用:0次
名校
9 . 图为铁及其化合物的“价—类”二维图。利用如图可以从不同角度研究含铁物质的性质及其转化关系。下列分析结果不正确的是


A.二维图缺失的类别①应填“单质”,化学式②应填“ ” ” |
B.从物质类别分析, 属于碱性氧化物,可以与稀HCl反应 属于碱性氧化物,可以与稀HCl反应 |
C.从化合价角度分析, 具有还原性,可以使酸性高锰酸钾溶液褪色 具有还原性,可以使酸性高锰酸钾溶液褪色 |
D.从物质转化角度分析, 和 和 都可以通过一步反应直接转化成② 都可以通过一步反应直接转化成② |
您最近一年使用:0次
2022-03-30更新
|
397次组卷
|
6卷引用:河北省河北正中实验中学2023-2024学年高一上学期月考三化学试题
名校
10 . 分类法是一种重要的学习方法,下列说法正确的是
| A.CO2溶于水形成的溶液能导电,所以CO2是电解质 |
| B.根据其化学成分,钢可分为高碳钢、中碳钢和低碳钢 |
| C.FeO和Fe2O3均不与H2O反应,故Fe(OH)2和Fe(OH)3都不能通过化合反应得到 |
| D.碱性氧化物一定是金属氧化物,酸性氧化物不一定是非金属氧化物 |
您最近一年使用:0次
2022-03-20更新
|
116次组卷
|
2卷引用:河北省三河市第二中学2021-2022学年高一上学期期末考试化学试题



