名校
解题方法
1 . 向200 mLFe2(SO4)3和CuSO4的混合溶液中逐渐加入铁粉,充分反应后溶液中固体剩余物的质量与加入铁粉的质量如图所示。忽略溶液体积的变化,下列说法正确的是


| A.a点时溶液中的阳离子仅为Cu2+和Fe2+ |
| B.b点时溶液中发生的反应为2Fe+3Cu2+=Cu+2Fe3+ |
| C.c点时溶液中溶质的物质的量浓度为0.2mol·L-1 |
| D.原溶液中Fe2(SO4)3和CuSO4的物质的量浓度之比为1:2 |
您最近一年使用:0次
2021-03-04更新
|
285次组卷
|
3卷引用:安徽省合肥市一中、六中、八中2020-2021学年高一上学期期末考试化学试题
名校
解题方法
2 . 电子工业制作印刷电路板常用FeCl3溶液腐蚀覆铜板,使用后的腐蚀液中加入一定量铁粉,充分反应。下列对反应后反应体系中成分分析合理的是
| A.若无固体剩余,则溶液中可能还有Fe3+ |
| B.若有固体存在,则该固体可能只有铁 |
| C.若溶液中有Cu2+,则一定没有固体析出 |
| D.若溶液中有Fe2+,则一定有Cu析出 |
您最近一年使用:0次
2020-11-24更新
|
465次组卷
|
6卷引用:安徽省芜湖市第一中学2020-2021学年高一上学期第二次月考化学试题
10-11高一下·广东深圳·期中
名校
3 . 将Fe、Cu、Fe2+、Fe3+和Cu2+盛于同一容器中充分反应,如Fe有剩余,则容器中只能有
| A.Cu、Fe2+、Fe | B.Fe2+、Fe3+ |
| C.Cu、Cu2+、Fe | D.Cu、Fe3+ |
您最近一年使用:0次
2020-05-22更新
|
178次组卷
|
22卷引用:2012-2013年黑龙江哈尔滨第十二中学高一上学期期末考试化学试卷
(已下线)2012-2013年黑龙江哈尔滨第十二中学高一上学期期末考试化学试卷2016-2017学年甘肃省嘉峪关市酒钢三中高一上学期期末考试化学试卷安徽省合肥市长丰县2020-2021学年高一上学期期末联考化学试题(已下线)2010-2011学年广东省深圳市高级中学高一下学期期中考试化学试卷(已下线)2011-2012学年天津市蓟县一中高一第二次月考化学试卷(已下线)2011-2012学年内蒙古巴彦淖尔市中学高三期中考试化学试卷(已下线)2012年鲁科版高中化学选修4 3.4离子反应练习卷2015-2016学年山西省怀仁一中高一12月月考化学试卷2015-2016学年陕西省西北农林科大附中高一上第二次月考化学试卷2016届贵州省务川民族中学高三上学期期中考试化学试卷2015-2016学年黑龙江省双鸭山一中高二6月月考化学试卷2016-2017学年河北石家庄辛集中学高一上阶段考二化学卷湖南省醴陵市第一中学2017-2018学年高一上学期第二次月考(12月)化学试题甘肃省嘉峪关市酒钢三中2017-2018学年高二上学期第二次月考化学试题甘肃省靖远县第四中学2018-2019学年高一上学期第二次月考化学试题河南省信阳市第六高级中学2018-2019学年高一上学期第三次(1月)月考化学试题湖南省张家界市民族中学2019-2020学年高一上学期第三次月考化学试题山东省济宁市微山县第二中学2019-2020学年高一上学期第三学段质量检测化学试题云南省昆明市农业大学附属中学2019-2020学年高一上学期第二次月考化学试题河北省泊头市第一中学2019-2020学年高一上学期第四次月考化学试题河南省焦作市沁阳市第一中学2019-2020学年高一上学期12月月考化学试题甘肃省白银市会宁县第一中学2020-2021学年高一上学期第二次月考化学试题
名校
解题方法
4 . 将2.8g铁粉加入50mL3mol·L-1的氯化铁溶液中,充分反应后,其结果是( )
| A.铁粉有剩余,溶液呈浅绿色 |
| B.往溶液中滴入KSCN溶液,不显血红色 |
| C.氧化产物和还原产物的物质的量之比为2∶1 |
| D.Fe2+和Fe3+物质的量之比为3∶1 |
您最近一年使用:0次
2020-04-27更新
|
216次组卷
|
5卷引用:浙江省丽水市2018-2019学年高一上学期期末教学质量监控化学试题
解题方法
5 . 化学与社会、生活密切相关,对下列现象或事实的解释正确的是( )
| 选项 | 现象或事实 | 解释 |
| A |  溶液可用于铜质印刷电路板刻制 溶液可用于铜质印刷电路板刻制 | Cu从 溶液中置换出铁 溶液中置换出铁 |
| B | 节日燃放的五彩缤纷的烟花 | 碱金属以及锶、钡等金属化合物的焰色反应 |
| C | 铝箔在酒精灯火焰上加热熔化但不滴落 | 氧化铝的熔点低于铝的熔点 |
| D | 氢氟酸可用于蚀刻玻璃 |  是碱性氧化物 是碱性氧化物 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
6 . 现有浓度均为1 mol/L的FeCl3、CuCl2的混合溶液100 mL,向该溶液中加入5.6 g铁粉充分反应(溶液的体积变化忽略不计)。已知,氧化性Fe3+> Cu2+下列有关叙述正确的是
| A.反应后的溶液中n(Fe2+)是0.15 mol | B.反应后的溶液中不存在Fe3+和Cu2+ |
| C.反应后残留固体为3.2 g | D.反应后残留固体中可能含有未反应的铁粉 |
您最近一年使用:0次
2020-02-14更新
|
331次组卷
|
5卷引用:安徽省合肥市第一、第六、第八中学2019-2020学年高一上学期期末考试化学试题
解题方法
7 . 我国古代许多著作在化学学科知识上都体现出了一定水平的认识。其中《管子•地数》中有记载:“上有丹沙者,下有黄金;上有慈石者,下有铜金。”
Ⅰ.“丹沙者丹砂也”,丹砂是古代炼丹的重要原料,也是实验室处理水银洒落后的产物。你认为丹砂主要成分是_____ ;(填化学式)“慈石者磁石也”,请写出磁石溶于盐酸的离子方程式:_____ ;
Ⅱ.“铜金者,斑岩铜矿也。”
安徽宣城茶亭铜金矿床是长江中下游成矿带中新发现的一个大型斑岩型矿床。斑岩铜矿中Cu主要以铜﹣铁硫化物(主要为CuFeS2)的形式存在。以黄铜矿(主要成分为CuFeS2,含少量杂质SiO2等)为原料,进行生物炼铜,同时得到副产品绿矾(FeSO4•7H2O)。其主要流程如图:
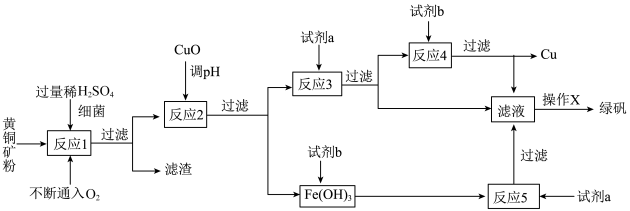
已知:①“反应1”:4CuFeS2 +2H2SO4 +17O2 ═4CuSO4 +2Fe2(SO4)3 +2H2O
②部分阳离子以氢氧化物形式开始沉淀和完全沉淀时溶液的pH如表:
(1)“反应1”中,每生成1 mol CuSO4转移电子数为_____ NA;
(2)“试剂a”是_____ ,“试剂b”是_____ ;
(3)“反应2”中加CuO调pH为3.7~4.7的目的是_____ ;
(4)“操作X”应为_____ 、_____ 、过滤、洗涤;请简述上述“操作X”中如何对所得 FeSO4•7H2O晶体进行洗涤_____ ;
(5)简述如何判断“反应5”已进行完全:_____ 。
Ⅰ.“丹沙者丹砂也”,丹砂是古代炼丹的重要原料,也是实验室处理水银洒落后的产物。你认为丹砂主要成分是
Ⅱ.“铜金者,斑岩铜矿也。”
安徽宣城茶亭铜金矿床是长江中下游成矿带中新发现的一个大型斑岩型矿床。斑岩铜矿中Cu主要以铜﹣铁硫化物(主要为CuFeS2)的形式存在。以黄铜矿(主要成分为CuFeS2,含少量杂质SiO2等)为原料,进行生物炼铜,同时得到副产品绿矾(FeSO4•7H2O)。其主要流程如图:

已知:①“反应1”:4CuFeS2 +2H2SO4 +17O2 ═4CuSO4 +2Fe2(SO4)3 +2H2O
②部分阳离子以氢氧化物形式开始沉淀和完全沉淀时溶液的pH如表:
沉淀物 | Cu(OH)2 | Fe(OH)3 | Fe(OH)2 |
开始沉淀pH | 4.7 | 2.7 | 7.6 |
完全沉淀pH | 6.7 | 3.7 | 9.6 |
(2)“试剂a”是
(3)“反应2”中加CuO调pH为3.7~4.7的目的是
(4)“操作X”应为
(5)简述如何判断“反应5”已进行完全:
您最近一年使用:0次
名校
8 . 18.4g由铁、铜组成的混合粉末加入100mL5.0mol•L﹣1FeCl3溶液中,充分反应后,剩余固体质量为3.2g。下列说法正确的是( )
| A.原固体混合物中:n(Cu):n(Fe)=2:1 |
| B.反应后溶液中的溶质有FeCl2、FeCl3、CuCl2 |
| C.反应后溶液中:n(Fe2+)+n(Cu2+)=0.8mol |
| D.剩余固体是铁 |
您最近一年使用:0次
2019-12-14更新
|
341次组卷
|
2卷引用:安徽省滁州市九校2019-2020学年高一上学期期末联考化学试题
9 . 化学使人们的生活越来越美好,下列过程没有涉及化学反应的是
| A.用四氯化碳萃取碘水中的碘 | B.用氯化铁溶液刻制印刷电路 |
| C.用漂白粉漂白纸张 | D.用油脂和氢氧化钠溶液制取肥皂 |
您最近一年使用:0次
名校
解题方法
10 . 铁是人类较早使用的金属之一。运用所学知识,回答下列问题。
(1)鉴别Fe(OH)3胶体和FeCl3溶液的方法是__________________________ 。
(2)电子工业用FeCl3溶液腐蚀敷在绝缘板上的铜,制造印刷电路板,请写出FeCl3溶液与铜反应的离子方程式:____________________ 。
(3)某研究性学习小组为测定FeCl3腐蚀铜后所得溶液的组成,进行了如下实验:
①取少量待测溶液,滴入KSCN溶液呈红色,则待测液中含有的金属阳离子是________ 。
②溶液组成的测定:取50.0mL待测溶液,加入足量的AgNO3溶液,得21.525 g白色沉淀,则溶液中c(Cl-)=________ mol·L-1。
③验证该溶液中含有Fe2+,正确的实验方法是______ 。
A.观察溶液是否呈浅绿色
B.取适量溶液,滴入酸性高锰酸钾溶液,若褪色,证明含有Fe2+
C.取适量溶液,滴入氯水,再滴入KSCN溶液,若显红色,证明原溶液中含有Fe2+
(1)鉴别Fe(OH)3胶体和FeCl3溶液的方法是
(2)电子工业用FeCl3溶液腐蚀敷在绝缘板上的铜,制造印刷电路板,请写出FeCl3溶液与铜反应的离子方程式:
(3)某研究性学习小组为测定FeCl3腐蚀铜后所得溶液的组成,进行了如下实验:
①取少量待测溶液,滴入KSCN溶液呈红色,则待测液中含有的金属阳离子是
②溶液组成的测定:取50.0mL待测溶液,加入足量的AgNO3溶液,得21.525 g白色沉淀,则溶液中c(Cl-)=
③验证该溶液中含有Fe2+,正确的实验方法是
A.观察溶液是否呈浅绿色
B.取适量溶液,滴入酸性高锰酸钾溶液,若褪色,证明含有Fe2+
C.取适量溶液,滴入氯水,再滴入KSCN溶液,若显红色,证明原溶液中含有Fe2+
您最近一年使用:0次



