20-21高一·全国·课时练习
解题方法
1 . 固体A由四种元素组成的化合物,为探究固体A的组成,设计并完成如下实验:
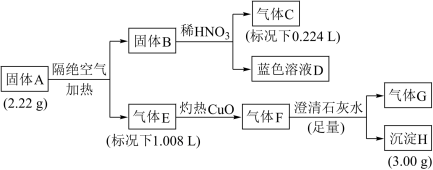
已知:固体B是一种单质,气体E、F都是G和另外一种气体组成。
请回答:
(1)组成A的四种元素是_____ ,气体E是____ 。
(2)固体A隔绝空气加热分解的化学方程式是______ 。
(3)蓝色溶液D和乙醇反应可获得固体A,同时还生成一种常见的温室气体,该反应的化学方程式为_____________________ 。

已知:固体B是一种单质,气体E、F都是G和另外一种气体组成。
请回答:
(1)组成A的四种元素是
(2)固体A隔绝空气加热分解的化学方程式是
(3)蓝色溶液D和乙醇反应可获得固体A,同时还生成一种常见的温室气体,该反应的化学方程式为
您最近一年使用:0次
名校
2 . Fe2O3、Cu2O都是红色粉末,常用作颜料。某校化学实验小组通过实验来探究一红色粉末是Fe2O3、Cu2O或二者混合物。探究过程如下:
查阅资料:Cu2O 溶于稀硫酸生成Cu和CuSO4;在空气中加热生成CuO.
提出假设:
假设1:红色粉末是Fe2O3
假设2:______ .
假设3:红色粉末是Cu2O和Fe2O3
(1)设计探究实验:取少量粉末放入足量稀硫酸中,在所得溶液中再滴加 KSCN 溶液。
(2)若假设1成立,则实验现象是______ .
(3)若滴加 KSCN 试剂后溶液不变红色,则证明原固体粉末中一定不含三氧化二铁。你认为这种说法合理吗?______ .简述你的理由______ .
(4)若固体粉末完全溶解无固体存在,滴加 KSCN 试剂时溶液不变红色,则证明假设______ 成立
(5)实验小组欲用加热法测定Cu2O的质量分数。取a g固体粉末在空气中充分加热,待质量不再变化时,称其质量为bg(b>a),则混合物中Cu2O的质量分数为______ .
查阅资料:Cu2O 溶于稀硫酸生成Cu和CuSO4;在空气中加热生成CuO.
提出假设:
假设1:红色粉末是Fe2O3
假设2:
假设3:红色粉末是Cu2O和Fe2O3
(1)设计探究实验:取少量粉末放入足量稀硫酸中,在所得溶液中再滴加 KSCN 溶液。
(2)若假设1成立,则实验现象是
(3)若滴加 KSCN 试剂后溶液不变红色,则证明原固体粉末中一定不含三氧化二铁。你认为这种说法合理吗?
(4)若固体粉末完全溶解无固体存在,滴加 KSCN 试剂时溶液不变红色,则证明假设
(5)实验小组欲用加热法测定Cu2O的质量分数。取a g固体粉末在空气中充分加热,待质量不再变化时,称其质量为bg(b>a),则混合物中Cu2O的质量分数为
您最近一年使用:0次
2020-06-06更新
|
246次组卷
|
2卷引用:甘肃省西北师范大学附属中学2019-2020学年高一上学期期末考试化学试题
名校
3 . 某铜制品在潮湿环境中发生的电化学腐蚀过程可表示为如图,腐蚀后有A物质生成,某小组为分析A物质的组成,进行了如下实验:
实验①:取A样品,加过量稀硝酸完全溶解后,再加入 溶液,有白色沉淀生成。
溶液,有白色沉淀生成。
实验②:另取A样品4.29g,加入含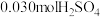 的稀硫酸溶液,恰好中和,生成两种盐的混合溶液。向所得混合溶液中加入适量的NaOH溶液,产生蓝色沉淀,经过滤、洗涤、灼烧得3.20g黑色固体。
的稀硫酸溶液,恰好中和,生成两种盐的混合溶液。向所得混合溶液中加入适量的NaOH溶液,产生蓝色沉淀,经过滤、洗涤、灼烧得3.20g黑色固体。
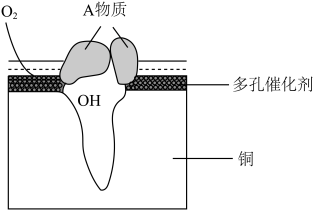
(1)该粉状锈中除了铜元素外还含有(写元素符号)___ 元素,该铜制品发生电化学腐蚀生成粉状锈时其正极电极反应式为____ 。
(2)写出该粉状锈溶于稀硫酸反应的离子方程式____ 。
(3)加热条件下,实验②中所得的黑色固体能与乙醇反应,化学方程式为____ 。
实验①:取A样品,加过量稀硝酸完全溶解后,再加入
 溶液,有白色沉淀生成。
溶液,有白色沉淀生成。实验②:另取A样品4.29g,加入含
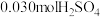 的稀硫酸溶液,恰好中和,生成两种盐的混合溶液。向所得混合溶液中加入适量的NaOH溶液,产生蓝色沉淀,经过滤、洗涤、灼烧得3.20g黑色固体。
的稀硫酸溶液,恰好中和,生成两种盐的混合溶液。向所得混合溶液中加入适量的NaOH溶液,产生蓝色沉淀,经过滤、洗涤、灼烧得3.20g黑色固体。
(1)该粉状锈中除了铜元素外还含有(写元素符号)
(2)写出该粉状锈溶于稀硫酸反应的离子方程式
(3)加热条件下,实验②中所得的黑色固体能与乙醇反应,化学方程式为
您最近一年使用:0次
解题方法
4 . 由两种元素组成的矿物A,测定A的组成流程如下:
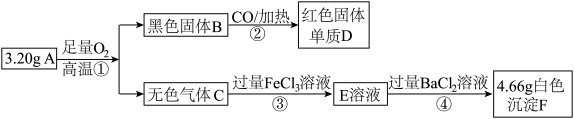
请回答:
(1)②反应中除了产生D外,还有一种气体生成,请写出该气体的电子式____________
(2)写出①的化学方程式:_______________________________________________________
(3)写出③的离子方程式:____________________________________________________
(4)检验E溶液中含有Fe2+ 的方法是:_____________________________

请回答:
(1)②反应中除了产生D外,还有一种气体生成,请写出该气体的电子式
(2)写出①的化学方程式:
(3)写出③的离子方程式:
(4)检验E溶液中含有Fe2+ 的方法是:
您最近一年使用:0次
2019-08-10更新
|
392次组卷
|
2卷引用:2019-2020学年新人教版必修2第5章第2节《氮及其化合物》作业
名校
解题方法
5 . 已知 为
为 和
和 的混合物,且知氧化性顺序:
的混合物,且知氧化性顺序: ,取
,取 样品进行如下图所示的实验:
样品进行如下图所示的实验:
(1)写出③步可能发生反应的3个离子方程式为________________________ 、________________________ 、________________________ 。
(2)若溶液E中只有一种金属离子,则一定是______ ;若D固体是纯净物,该固体是______ 。(填化学式)
(3)向溶液A中加入 粉,若会反应,则写出反应的离子方程式,若不会反应,则填“不能”在横线上
粉,若会反应,则写出反应的离子方程式,若不会反应,则填“不能”在横线上__________________________________________ 。
 为
为 和
和 的混合物,且知氧化性顺序:
的混合物,且知氧化性顺序: ,取
,取 样品进行如下图所示的实验:
样品进行如下图所示的实验:
(1)写出③步可能发生反应的3个离子方程式为
(2)若溶液E中只有一种金属离子,则一定是
(3)向溶液A中加入
 粉,若会反应,则写出反应的离子方程式,若不会反应,则填“不能”在横线上
粉,若会反应,则写出反应的离子方程式,若不会反应,则填“不能”在横线上
您最近一年使用:0次
2019-01-12更新
|
300次组卷
|
4卷引用:【全国百强校】江西省抚州市临川第一中学2018-2019学年高一上学期12月月考化学试题
【全国百强校】江西省抚州市临川第一中学2018-2019学年高一上学期12月月考化学试题四川省泸县第四中学2019-2020学年高一下学期第一次在线月考化学试题(已下线)第二章 元素与物质世界(能力提升)-2020-2021学年高一化学必修第一册单元测试定心卷 (鲁科版2019)山西省芮城中学2021-2022学年高一上学期阶段性月考化学试题
2019高三·全国·专题练习
解题方法
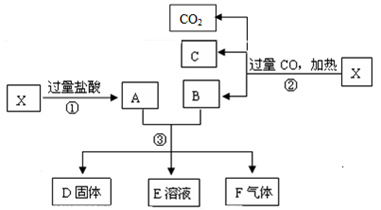
6 . 孔雀石的主要成分为Cu2(OH)2CO3。某同学设计的从孔雀石中冶炼铜的方案如下(假设孔雀石中杂质不溶于水和稀硫酸):

(1)反应①能观察到的现象是__________ ,有关反应的化学方程式为________ 。
(2)反应②加入的金属可能是______ ,有关反应的离子方程式为________ 。

(1)反应①能观察到的现象是
(2)反应②加入的金属可能是
您最近一年使用:0次
2011·内蒙古呼伦贝尔·二模
解题方法
7 . 用含少量铁的氧化铜制取氯化铜晶体(CuCl2·xH2O)。有如下操作:
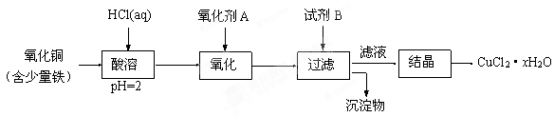
已知:在pH为4~5时,Fe3+几乎完全水解而沉淀,Cu2+却不水解。
(1)加热酸溶过程中发生反应的化学方程式有:____________ 。
(2)氧化剂A可选用_________ (填编号,下同)。
A.KMnO4 B. HNO3 C. Cl2
(3)要得到较纯的产品,试剂B可选用_________ 。
A. NaOH B. CuO C.FeO
(4)试剂B的作用是__________ 。
A. 使Cu2+完全沉淀 B. 使Fe3+完全沉淀
C. 降低溶液的pH D. 提高溶液的pH
(5)从滤液经过结晶得到氯化铜晶体的实验条件是___________ 。

已知:在pH为4~5时,Fe3+几乎完全水解而沉淀,Cu2+却不水解。
(1)加热酸溶过程中发生反应的化学方程式有:
(2)氧化剂A可选用
A.KMnO4 B. HNO3 C. Cl2
(3)要得到较纯的产品,试剂B可选用
A. NaOH B. CuO C.FeO
(4)试剂B的作用是
A. 使Cu2+完全沉淀 B. 使Fe3+完全沉淀
C. 降低溶液的pH D. 提高溶液的pH
(5)从滤液经过结晶得到氯化铜晶体的实验条件是
您最近一年使用:0次



