解题方法
1 . 实验室以废铜屑为原料制取碱式碳酸铜[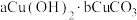 ]的流程如下:
]的流程如下:

已知:
①废铜屑的主要杂质有CuO、 、
、 、FeO和
、FeO和 ,“酸浸”使用的装置如图;
,“酸浸”使用的装置如图;
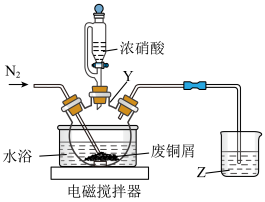
②相关数据见下表:
请回答:
(1)仪器Y的名称是___________ ,溶液Z的作用是___________ 。
(2)流程中需要对滤液加热至70℃但又不宜过高,理由是___________ 。
(3)下列有关说法正确的是___________ 。
A.“酸浸”装置鼓入的 也可用空气代替
也可用空气代替
B.物质X可能是CuO、NaOH溶液或浓氨水
C.滤渣的主要成分是 、
、 、
、 和
和
D.流程中两次对溶液调pH,其调节范围和操作目的均不相同
E.“系列操作”包括了充分搅拌、趁热过滤、蒸馏水洗和灼烧等步骤
(4)可采用滴定法、热重分析法分别对碱式碳酸铜[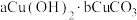 ]的组成进行分析。
]的组成进行分析。
①滴定法测定时需要用到酸式滴定管。其中,滴定步骤前可能需要的操作如下,请从中选出正确的操作并按序列出字母:______
向滴定管加蒸馏水并观察是否漏液______→______→______→______→______→______→在滴定管架上竖直放置,静置后读数
a.用蒸馏水洗涤滴定管,再用标准溶液润洗
b.将活塞旋转180°后静置观察
c.使滴定管略倾斜,捏住橡皮管内玻璃球赶走管尖气泡
d.向滴定管中加入标准液并高于“0”刻度
e.竖直滴定管,调整标准液液面低于“0”刻度
f.一手握住并倾斜滴定管,一手开关活塞赶走管尖气泡
②测得碱式碳酸铜[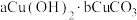 ]的热重分析结果如图所示,已知失重至65.7%时固体呈砖红色,则计算可知
]的热重分析结果如图所示,已知失重至65.7%时固体呈砖红色,则计算可知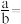
___________ (保留3位有效数字)。

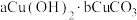 ]的流程如下:
]的流程如下:
已知:
①废铜屑的主要杂质有CuO、
 、
、 、FeO和
、FeO和 ,“酸浸”使用的装置如图;
,“酸浸”使用的装置如图;
②相关数据见下表:
| 物质 |  |  |  |  |
| 开始沉淀pH | 1.9 | 6.5 | 4.2 | 3.4 |
| 沉淀完全pH | 3.2 | 9.7 | 6.7 | 4.0 |
(1)仪器Y的名称是
(2)流程中需要对滤液加热至70℃但又不宜过高,理由是
(3)下列有关说法正确的是
A.“酸浸”装置鼓入的
 也可用空气代替
也可用空气代替B.物质X可能是CuO、NaOH溶液或浓氨水
C.滤渣的主要成分是
 、
、 、
、 和
和
D.流程中两次对溶液调pH,其调节范围和操作目的均不相同
E.“系列操作”包括了充分搅拌、趁热过滤、蒸馏水洗和灼烧等步骤
(4)可采用滴定法、热重分析法分别对碱式碳酸铜[
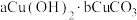 ]的组成进行分析。
]的组成进行分析。①滴定法测定时需要用到酸式滴定管。其中,滴定步骤前可能需要的操作如下,请从中选出正确的操作并按序列出字母:
向滴定管加蒸馏水并观察是否漏液______→______→______→______→______→______→在滴定管架上竖直放置,静置后读数
a.用蒸馏水洗涤滴定管,再用标准溶液润洗
b.将活塞旋转180°后静置观察
c.使滴定管略倾斜,捏住橡皮管内玻璃球赶走管尖气泡
d.向滴定管中加入标准液并高于“0”刻度
e.竖直滴定管,调整标准液液面低于“0”刻度
f.一手握住并倾斜滴定管,一手开关活塞赶走管尖气泡
②测得碱式碳酸铜[
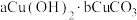 ]的热重分析结果如图所示,已知失重至65.7%时固体呈砖红色,则计算可知
]的热重分析结果如图所示,已知失重至65.7%时固体呈砖红色,则计算可知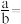

您最近一年使用:0次
2 . 氯化亚铜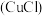 是一种重要的化工产品,它难溶于水和乙醇,可溶于浓
是一种重要的化工产品,它难溶于水和乙醇,可溶于浓 与氨水形成的混合物,置于潮湿空气中迅速氧化为
与氨水形成的混合物,置于潮湿空气中迅速氧化为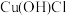 而变为绿色。实验室用酸性蚀刻液(含
而变为绿色。实验室用酸性蚀刻液(含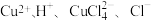 )和碱性蚀刻液[含
)和碱性蚀刻液[含 ]来制备
]来制备 ,实验过程的流程如下:
,实验过程的流程如下:
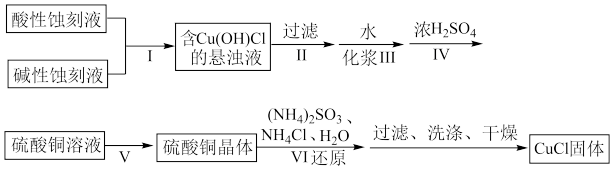
(1)步骤Ⅳ需要控制 为1~2、
为1~2、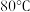 下进行,合适的加热方式是
下进行,合适的加热方式是_______ 。
(2)步骤Ⅴ为了得到较为纯净的硫酸铜晶体,根据下表中物质的溶解度(单位为g)随温度的变化,写出步骤Ⅴ得到硫酸铜晶体的操作:_______ 。
(3)写出还原过程中发生主要反应的离子方程式:_______ 。
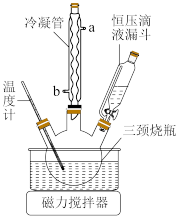
(4)步骤Ⅵ在图装置中进行,启动磁力撒搅拌器,使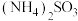 和
和 混合液缓慢滴入三颈烧瓶(提前装入硫酸铜晶体)中,控制滴加混合液速度,使所需时间不低于1小时。加完后,继续搅拌10分钟。将三颈烧瓶中的混合物进行一系列操作即可得粗产品。下列有关说法正确的是_______。
混合液缓慢滴入三颈烧瓶(提前装入硫酸铜晶体)中,控制滴加混合液速度,使所需时间不低于1小时。加完后,继续搅拌10分钟。将三颈烧瓶中的混合物进行一系列操作即可得粗产品。下列有关说法正确的是_______。
(5) 的定量分析,称取样品
的定量分析,称取样品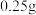 置于预先放入玻璃珠和过量
置于预先放入玻璃珠和过量 溶液的锥形瓶中,不断摇动,待样品全部溶解后,加入
溶液的锥形瓶中,不断摇动,待样品全部溶解后,加入 水、邻菲罗啉指示剂2滴,立即用
水、邻菲罗啉指示剂2滴,立即用 的硫酸铈标准液滴定至绿色出现为终点,消耗标准液
的硫酸铈标准液滴定至绿色出现为终点,消耗标准液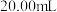 ,发生的反应为
,发生的反应为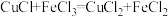 ,
, ,则
,则
①加入玻璃珠的作用是_______ 。
②下列有关上述滴定操作的说法正确的是_______ 。
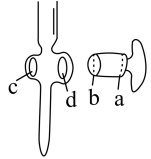
A.滴定管活塞涂凡士林:取下活塞,用滤纸擦干,用手指蘸取少量凡士林涂抹一薄层在活塞a、c(如图)处的四周,平行插入活塞槽中,然后朝同一个方向转动
B.滴定开始时可以将液体成线状快速流下,接近终点时减慢滴加速度,必要时采用半滴操作
C.读数时可将滴定管从架上取下,捏住管上端无刻度处,使滴定管保持垂直
D.第一次滴定终点时,若测得消耗标准液体积小于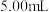 ,则第二次滴定时可稀释待测液后重新滴定来减小误差
,则第二次滴定时可稀释待测液后重新滴定来减小误差
③样品的 的质量分数为
的质量分数为_______ 。
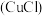 是一种重要的化工产品,它难溶于水和乙醇,可溶于浓
是一种重要的化工产品,它难溶于水和乙醇,可溶于浓 与氨水形成的混合物,置于潮湿空气中迅速氧化为
与氨水形成的混合物,置于潮湿空气中迅速氧化为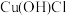 而变为绿色。实验室用酸性蚀刻液(含
而变为绿色。实验室用酸性蚀刻液(含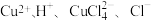 )和碱性蚀刻液[含
)和碱性蚀刻液[含 ]来制备
]来制备 ,实验过程的流程如下:
,实验过程的流程如下:
(1)步骤Ⅳ需要控制
 为1~2、
为1~2、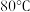 下进行,合适的加热方式是
下进行,合适的加热方式是(2)步骤Ⅴ为了得到较为纯净的硫酸铜晶体,根据下表中物质的溶解度(单位为g)随温度的变化,写出步骤Ⅴ得到硫酸铜晶体的操作:
| 温度 物质 |  | 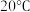 | 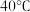 | 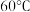 | 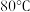 | 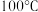 |
| 氯化铜 | 75 | 80 | 85 | 90 | 100 | 108 |
| 硫酸铜 | 12 | 18 | 30 | 50 | 60 | 87 |
(4)步骤Ⅵ在图装置中进行,启动磁力撒搅拌器,使
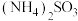 和
和 混合液缓慢滴入三颈烧瓶(提前装入硫酸铜晶体)中,控制滴加混合液速度,使所需时间不低于1小时。加完后,继续搅拌10分钟。将三颈烧瓶中的混合物进行一系列操作即可得粗产品。下列有关说法正确的是_______。
混合液缓慢滴入三颈烧瓶(提前装入硫酸铜晶体)中,控制滴加混合液速度,使所需时间不低于1小时。加完后,继续搅拌10分钟。将三颈烧瓶中的混合物进行一系列操作即可得粗产品。下列有关说法正确的是_______。
| A.装置中的温度计显示温度会迅速升高 |
B.滴加太快容易发生其他副反应,而使制得的 产品纯度下降 产品纯度下降 |
C.冷凝管上口排出的气体主要是 |
| D.该兴趣小组制备过程中产生滤液、洗涤液等要进行无害化处理后才能排放 |
 的定量分析,称取样品
的定量分析,称取样品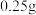 置于预先放入玻璃珠和过量
置于预先放入玻璃珠和过量 溶液的锥形瓶中,不断摇动,待样品全部溶解后,加入
溶液的锥形瓶中,不断摇动,待样品全部溶解后,加入 水、邻菲罗啉指示剂2滴,立即用
水、邻菲罗啉指示剂2滴,立即用 的硫酸铈标准液滴定至绿色出现为终点,消耗标准液
的硫酸铈标准液滴定至绿色出现为终点,消耗标准液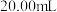 ,发生的反应为
,发生的反应为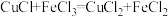 ,
, ,则
,则①加入玻璃珠的作用是
②下列有关上述滴定操作的说法正确的是

A.滴定管活塞涂凡士林:取下活塞,用滤纸擦干,用手指蘸取少量凡士林涂抹一薄层在活塞a、c(如图)处的四周,平行插入活塞槽中,然后朝同一个方向转动
B.滴定开始时可以将液体成线状快速流下,接近终点时减慢滴加速度,必要时采用半滴操作
C.读数时可将滴定管从架上取下,捏住管上端无刻度处,使滴定管保持垂直
D.第一次滴定终点时,若测得消耗标准液体积小于
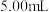 ,则第二次滴定时可稀释待测液后重新滴定来减小误差
,则第二次滴定时可稀释待测液后重新滴定来减小误差③样品的
 的质量分数为
的质量分数为
您最近一年使用:0次
解题方法
3 . 现有一种以黄铜矿和硫磺为原料制取铜和其他产物的新工艺,原料的综合利用率较高。其主要流程如下:
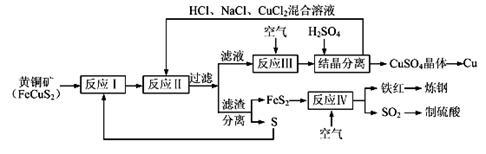
注:反应Ⅱ的离子方程式为Cu2++CuS+4Cl—=2[CuCl2]-+S
请回答下列问题:
(1)从黄铜矿冶炼粗铜的传统工艺是将精选后的富铜矿砂与空气在高温下煅烧,使其转变为铜。这种方法的缺点是_____________ 、_____________ 。
(2)反应Ⅰ的产物为(填化学式)_____________ 。
(3)反应Ⅲ的离子方程式为_____________ 。
(4)一定温度下,在反应Ⅲ所得的溶液中加入稀硫酸,可以析出硫酸铜晶体,其原因是_____________ 。
(5)黄铜矿中Fe的化合价为+2,对于反应:8CuFeS2+21O2 8Cu+4FeO+2Fe2O3+16SO2,下列有关该反应的说法正确的是
8Cu+4FeO+2Fe2O3+16SO2,下列有关该反应的说法正确的是_____________ (填字母)。
(6)某硫酸厂为测定反应Ⅳ所得气体中SO2的体积分数,取280mL(已折算成标准状况)气体样品与足量Fe2(SO4)3溶液完全反应后,用浓度为0.02000 mol/L的K2Cr2O7标准溶液滴定至终点,消耗K2Cr2O7溶液25.00 mL 。
已知:Cr2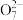 + Fe2++ H+→Cr3++ Fe3++ H2O(未配平)
+ Fe2++ H+→Cr3++ Fe3++ H2O(未配平)
①SO2通入Fe2(SO4)3溶液,发生反应的离子方程式为_____________ 。
②反应Ⅳ所得气体中SO2的体积分数为_____________ 。

注:反应Ⅱ的离子方程式为Cu2++CuS+4Cl—=2[CuCl2]-+S
请回答下列问题:
(1)从黄铜矿冶炼粗铜的传统工艺是将精选后的富铜矿砂与空气在高温下煅烧,使其转变为铜。这种方法的缺点是
(2)反应Ⅰ的产物为(填化学式)
(3)反应Ⅲ的离子方程式为
(4)一定温度下,在反应Ⅲ所得的溶液中加入稀硫酸,可以析出硫酸铜晶体,其原因是
(5)黄铜矿中Fe的化合价为+2,对于反应:8CuFeS2+21O2
 8Cu+4FeO+2Fe2O3+16SO2,下列有关该反应的说法正确的是
8Cu+4FeO+2Fe2O3+16SO2,下列有关该反应的说法正确的是| A.反应中被还原的元素只有氧 |
| B.反应生成的SO2直接排放会污染环境 |
| C.SO2既是氧化产物又是还原产物 |
| D.当有8mol铜生成时,转移电子数目为100NA |
已知:Cr2
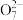 + Fe2++ H+→Cr3++ Fe3++ H2O(未配平)
+ Fe2++ H+→Cr3++ Fe3++ H2O(未配平)①SO2通入Fe2(SO4)3溶液,发生反应的离子方程式为
②反应Ⅳ所得气体中SO2的体积分数为
您最近一年使用:0次



